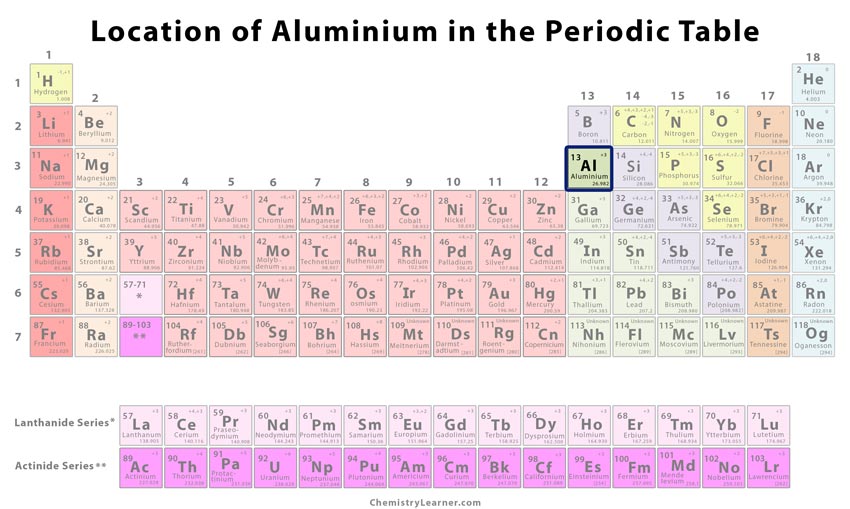
Co je to hliník
Hliník (vyslovuje se jako ah-LOO-men-em) je měkký a lehký kov, chemicky označovaný Al. Existuje ve formě několika minerálních sloučenin, které mají široké komerční využití díky své netoxičnosti a vysoké odolnosti proti korozi. Má 15 izotopů s hmotnostními čísly od 22 do 35, z nichž pouze Al-26 je radioaktivní s poločasem rozpadu 7,17×105let a Al-27 existuje přirozeně.

Kde ho lze nalézt
Prvek tvoří asi 8,1 % zemské kůry, což z něj činí jeden z nejrozšířenějších kovů. Lze jej nalézt v kombinaci s jinými kovy ve formě křemičitanových minerálů, jako je kryolit a bauxit. Jeho výroba v komerčním měřítku se provádí nákladným chemickým procesem zvaným Hall-Heroultův proces, který vyžaduje velké množství energie.
Historie
Původ jeho názvu:
Kdo ho objevil:
Kdy, kde a jak byl objeven
V průběhu 3. století se v Číně předpokládalo, že hrobka vojevůdce Čou-čou obsahuje asi 85 % hliníku. V roce 1700 se také objevila domněnka o přítomnosti oxidu tohoto kovu, ale žádnou další analýzu se nepodařilo provést. Cornwallský chemik Henry Davy se totiž pokusil extrahovat sodík a draslík z jejich příslušných oxidů, ale Al se nepodařilo získat.
Teprve v roce 1825 Oersted v dánské Kodani zahřál chlorid hlinitý s draslíkem a extrahoval nečistou formu kovu. V roce 1827 německý chemik Friedrich Wohler konečně zopakoval metodu s použitím sodíku a získal čistý vzorek .

Klasifikace, vlastnosti a charakteristika hliníku
Všeobecné vlastnosti |
|
| Relativní/průměrná atomová hmotnost | 26.982 |
| Atomová hmotnost/hmotnost | 26,982 atomových hmotnostních jednotek |
| Molární hmotnost/molekulová hmotnost | 26.982 g/mol |
| Masové číslo | 27 |
Fyzikální vlastnosti |
|
| Barva/fyzikální vzhled | Stříbřitě bílá |
| Teplota tání/teplota tuhnutí | 660.323°C (1220.581°F) |
| Teplota varu | 2519°C (4566°F) |
| Hustota | 2.70 g/cm3 |
| Standardní/fyzikální stav při normální pokojové teplotě (pevná látka/kapalina/plyn) | Tvrdá látka |
| Tvrdost | Ano |
| Malátnost | Ano |
| Tvrdost | 2.9 Mohs |
| Elektrická vodivost | 37.6676 x 106 Sm-1 |
| Tepelná vodivost | 237 Wm-1K-1 |
| Měrná tepelná kapacita | 0.90 Jg-1K-1 |
| Specifická hmotnost | 2,8 |
| Resistivita | 2.65 x10-8ρ (ohm m) |
| Pevnost v tahu | 90 Mpa |
| Teplotní koeficient | 0.00393 α/°C |
| Mez pevnosti v tahu | 276 Mpa |
| Koeficient lineární tepelné roztažnosti/přestupu tepla | 23,1 10-6K-1 |
| Koeficient tření | 1.35 |
Chemické vlastnosti |
|
| Hořlavost | Hořlavý |
| Oxidační stavy (čísla) | 3 |
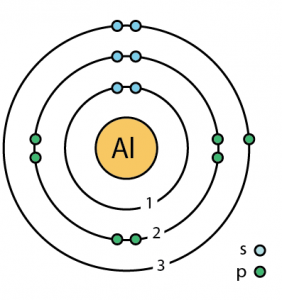
Atomové údaje hliníku
| Valenční elektrony | 1 | 1 | |||||
| Elektronová konfigurace (konfigurace vzácných plynů) | 3s23p1 | ||||||
| Struktura krystalu | Obličej-centrovaná kubická | ||||||
| Mřížková konstanta/parametr | 0.405 nm | ||||||
| Energetické hladiny | |||||||
| První energetická hladina | 2 | ||||||
| Druhá. energetická hladina | 8 | ||||||
| Třetí energetická hladina | 3 | ||||||
| Atomová struktura | |||||||
| – Počet elektronů | 13 | ||||||
| – Počet neutronů | 14 | ||||||
| – Počet protonů | 13 | ||||||
| Poloměr atomu | |||||||
| – Atomový poloměr | 1.84 Å | ||||||
| – Kovalentní poloměr | 1,24 Å | ||||||
| Elektronegativita | 1.61 | ||||||
| Náboj iontu | +1 | ||||||
| Ionizační energie
(kJmol-1) |
1. | 2. | 3. | 4. | 5. | 6. | 7. |
| 577.539 | 1816.679 | 2744.781 | 11577.469 | 14841.857 | 18379.49 | 23326.3 | |
K čemu se hliník běžně používá
- Používá se v široké škále výrobků, například v panelech plotových bran, vlečky, plechovky, trubky, trubky, dráty, fólie, střešní krytiny, smažení, pánve, zábradlí, nátěry, kryty teras, kola, pájecí tyče, sítové dveře, radiátory, nádrže na plyn a sloupy .
- Al je dobrým vodičem elektřiny a představuje ideální náhradu mědi z hlediska nákladů a hmotnosti pro výrobu elektrických přenosových vedení .
- Hliník se leguje s jinými kovy, jako je měď, hořčík, křemík a mangan, k výrobě kuličkových ložisek, automobilových dílů, raket a letadel .
- Kov se často používá jako reflexní povlak na zrcadlech dalekohledů, hračkách, obalech, dekorativních a ozdobných papírech na ochranu před světlem a teplem .
- Alternativou k drahým bateriím a kapalným palivům jsou vzduchové články/baterie s hliníkovými palivovými ionty, které jsou pro použití pohodlnější a přenosnější .

Má prvek nějaké toxické účinky
Vdechování prachu nebo výparů obsahujících Al ovlivňuje dýchací systém a způsobuje kašel a další poruchy související s plícemi. Dlouhodobé požití kovu ve formě některých perorálních výrobků může být škodlivé pro ledviny a také zvyšuje možnost vzniku Alzheimerovy choroby .

Zajímavá fakta
- Před objevem Hall-Heroultova procesu byl čistý Al dražší než zlato, a proto se mu říkalo “král kovů” .
- Kov lze několikrát recyklovat, aniž by byla snížena jeho kvalita .

Cena hliníku
Cena čistého se může pohybovat někde mezi 0,9 a 1 USD.
- http://www.rsc.org/periodic-table/element/13/aluminium
- https://education.jlab.org/itselemental/ele013.html
- https://pubchem.ncbi.nlm.nih.gov/compound/aluminum#section=Computed-Properties
- https://www.chemicool.com/elements/aluminum.html
- http://hyperphysics.phy-astr.gsu.edu/hbase/Tables/rstiv.html
- https://www.tedpella.com/company_html/hardness.htm
- http://asm.matweb.com/search/SpecificMaterial.asp?bassnum=ma6061t6
- https://study.com/academy/answer/how-many-valence-electrons-does-aluminum-have.html
- http://www.chemicalelements.com/elements/al.html
- https://www.sciencedirect.com/science/article/pii/S0378775307002236
- https://www.atsdr.cdc.gov/phs/phs.asp?id=1076&tid=34