- Was ist Aluminium
- Wo kann es gefunden werden
- Geschichte
- Klassifizierung, Eigenschaften und Merkmale von Aluminium
- Allgemeine Eigenschaften
- Physikalische Eigenschaften
- Chemische Eigenschaften
- Atomische Daten von Aluminium
- Wofür wird Aluminium üblicherweise verwendet
- Hat das Element toxische Wirkungen
- Interessante Fakten
- Aluminium Preis
Was ist Aluminium
Aluminium (ausgesprochen als ah-LOO-men-em) ist ein weiches und leichtes Metall, das durch die chemische Bezeichnung Al dargestellt wird. Es kommt in Form verschiedener mineralischer Verbindungen vor und hat aufgrund seiner Ungiftigkeit und hohen Korrosionsbeständigkeit eine breite Palette kommerzieller Anwendungen. Es hat 15 Isotope mit Massenzahlen zwischen 22 und 35, von denen nur Al-26 mit einer Halbwertszeit von 7,17×105 Jahren radioaktiv ist und Al-27 natürlich vorkommt.

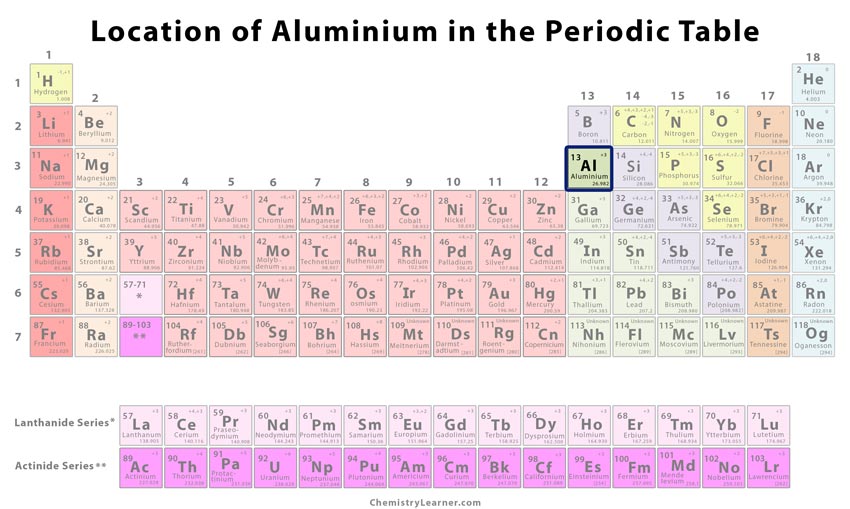
Wo kann es gefunden werden
Das Element macht etwa 8,1 % der Erdkruste aus und ist damit eines der häufigsten Metalle. Man findet es in Verbindung mit anderen Metallen in Form von Silikatmineralien wie Kryolith und Bauxit. Seine Herstellung in kommerziellem Maßstab erfolgt durch ein teures chemisches Verfahren, das Hall-Heroult-Verfahren, das eine große Menge an Energie erfordert.
Geschichte
Herkunft des Namens: Der Name leitet sich von dem lateinischen Wort für Alaun “alumen” ab, was so viel wie “bitteres Salz” bedeutet.
Wer hat es entdeckt: Hans Oersted
Wann, wo und wie wurde es entdeckt
Im 3. Jahrhundert glaubte man in China, dass das Grab eines Militärführers namens Chou-Chu etwa 85% Aluminium enthielt. In den 1700er Jahren wurde das Vorhandensein von Oxid des Metalls ebenfalls vermutet, aber es konnte keine weitere Analyse durchgeführt werden. Der Chemiker Henry Davy aus Cornwall versuchte, Natrium und Kalium aus ihren jeweiligen Oxiden zu extrahieren, aber das Aluminium konnte nicht gewonnen werden.
Erst 1825 erhitzte Oersted in Kopenhagen, Dänemark, Aluminiumchlorid mit Kalium und extrahierte eine unreine Form des Metalls. 1827 wiederholte der deutsche Chemiker Friedrich Wohler schließlich die Methode mit Natrium und erhielt eine reine Probe.

Klassifizierung, Eigenschaften und Merkmale von Aluminium
Allgemeine Eigenschaften |
|
| Relative/mittlere Atommasse | 26.982 |
| Atommasse/Gewicht | 26.982 Atommasseneinheiten |
| Molmasse/Molekulargewicht | 26.982 g/mol |
| Massenzahl | 27 |
Physikalische Eigenschaften |
|
| Farbe/physikalisches Aussehen | Silberweiß |
| Schmelzpunkt/Gefrierpunkt | 660.323°C (1220.581°F) |
| Siedepunkt | 2519°C (4566°F) |
| Dichte | 2.70 g/cm3 |
| Standard/Physikalischer Zustand der Materie bei normaler Raumtemperatur (fest/flüssig/gasförmig) | Fest |
| Duktilität | Ja |
| Mischbarkeit | Ja |
| Härte | 2.9 Mohs |
| Elektrische Leitfähigkeit | 37.6676 x 106 Sm-1 |
| Wärmeleitfähigkeit | 237 Wm-1K-1 |
| Spezifische Wärmekapazität | 0.90 Jg-1K-1 |
| Spezifische Schwerkraft | 2,8 |
| Widerstand | 2.65 x10-8ρ (Ohm m) |
| Zugfestigkeit | 90 Mpa |
| Temperaturkoeffizient | 0.00393 α/°C |
| Zugfestigkeit | 276 Mpa |
| Koeffizient der linearen Wärmeausdehnung/Wärmeübertragung | 23,1 10-6K-1 |
| Reibungskoeffizient | 1.35 |
Chemische Eigenschaften |
|
| Entflammbarkeit | Entflammbar |
| Oxidationsstufen (Zahlen) | 3 |
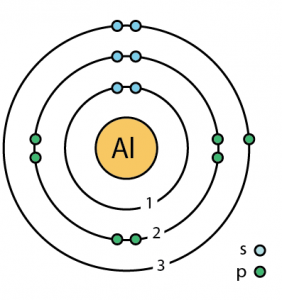
Atomische Daten von Aluminium
| Valenz-Elektronen | 1 | ||||||
| Elektronenkonfiguration (Edelgaskonfiguration) | 3s23p1 | ||||||
| Kristallstruktur | Flächen-zentriert kubisch | ||||||
| Gitterkonstante/Parameter | 0.405 nm | ||||||
| Energieniveaus | |||||||
| Erstes Energieniveau | 2 | ||||||
| Zweites Energieniveau | 8 | ||||||
| Drittes Energieniveau | 3 | ||||||
| Atomstruktur | |||||||
| – Anzahl der Elektronen | 13 | ||||||
| – Anzahl der Neutronen | 14 | ||||||
| – Anzahl der Protonen | 13 | ||||||
| Atomradius | |||||||
| – Atomradius | 1.84 Å | ||||||
| – Kovalenter Radius | 1.24 Å | ||||||
| Elektronengativität | 1.61 | ||||||
| Ladung des Ions | +1 | ||||||
| Ionisierungsenergie
(kJmol-1) |
1. | 2. | 3. | 4. | 5. | 6. | 7. |
| 577.539 | 1816.679 | 2744.781 | 11577.469 | 14841.857 | 18379.49 | 23326.3 | |
Wofür wird Aluminium üblicherweise verwendet
- Es wird in einer Vielzahl von Produkten wie Zauntorplatten, Abstellgleise, Dosen, Rohre, Drähte, Folien, Bedachungen, Braten, Pfannen, Geländer, Beschichtungen, Terrassenüberdachungen, Räder, Hartlötstäbe, Bildschirmtüren, Heizkörper, Gastanks und Masten.
- Als guter Stromleiter ist Al ein idealer Ersatz für Kupfer in Bezug auf Kosten und Gewicht, um elektrische Übertragungsleitungen zu bauen.
- Aluminium wird mit anderen Metallen wie Kupfer, Magnesium, Silizium und Mangan legiert, um Kugellager, Autoteile, Raketen und Flugzeuge herzustellen.
- Das Metall wird oft als reflektierende Beschichtung auf Teleskopspiegeln, Spielzeug, Verpackungen, Dekorations- und Schmuckpapieren verwendet, um vor Licht und Hitze zu schützen.
- Als Alternative zu teuren Batterien und flüssigen Brennstoffen sind Aluminium-Brennstoff-Ionen-Luft-Zellen/Batterien bequemer und tragbarer im Gebrauch.

Hat das Element toxische Wirkungen
Das Einatmen von Al-haltigen Stäuben oder Dämpfen wirkt sich auf das Atmungssystem aus und verursacht Husten und andere lungenbedingte Störungen. Längerer Verzehr des Metalls in Form von einigen oralen Produkten kann die Nieren schädigen und die Wahrscheinlichkeit der Alzheimer-Krankheit erhöhen.

Interessante Fakten
- Vor der Entdeckung des Hall-Heroult-Verfahrens war reines Aluminium teurer als Gold und wurde daher als “König der Metalle” bezeichnet.
- Das Metall kann mehrmals recycelt werden, ohne seine Qualität zu beeinträchtigen.

Aluminium Preis
Die Kosten für reines kann irgendwo zwischen $ 0,9 und $ 1 variieren.
- http://www.rsc.org/periodic-table/element/13/aluminium
- https://education.jlab.org/itselemental/ele013.html
- https://pubchem.ncbi.nlm.nih.gov/compound/aluminum#section=Computed-Properties
- https://www.chemicool.com/elements/aluminum.html
- http://hyperphysics.phy-astr.gsu.edu/hbase/Tables/rstiv.html
- https://www.tedpella.com/company_html/hardness.htm
- http://asm.matweb.com/search/SpecificMaterial.asp?bassnum=ma6061t6
- https://study.com/academy/answer/how-many-valence-electrons-does-aluminum-have.html
- http://www.chemicalelements.com/elements/al.html
- https://www.sciencedirect.com/science/article/pii/S0378775307002236
- https://www.atsdr.cdc.gov/phs/phs.asp?id=1076&tid=34