Ez egy rövid áttekintés az FDA által a termék forgalomba hozatalának jóváhagyásával kapcsolatos információkról. A termékkel, a felhasználási javallatokkal és az FDA jóváhagyásának alapjával kapcsolatos teljesebb információkért lásd az alábbi linkeket: a biztonsági és hatékonysági adatok összefoglalója (SSED) és a termék címkéje.
Termék neve: Axonics Sacralis Neuromodulációs Rendszer
PMA kérelmező: Axonics Modulation Technologies, Inc: 26 Technology Drive, Irvine, CA 92618
Az engedélyezés dátuma: November 13, 2019
Jóváhagyó levél: Jóváhagyási végzés
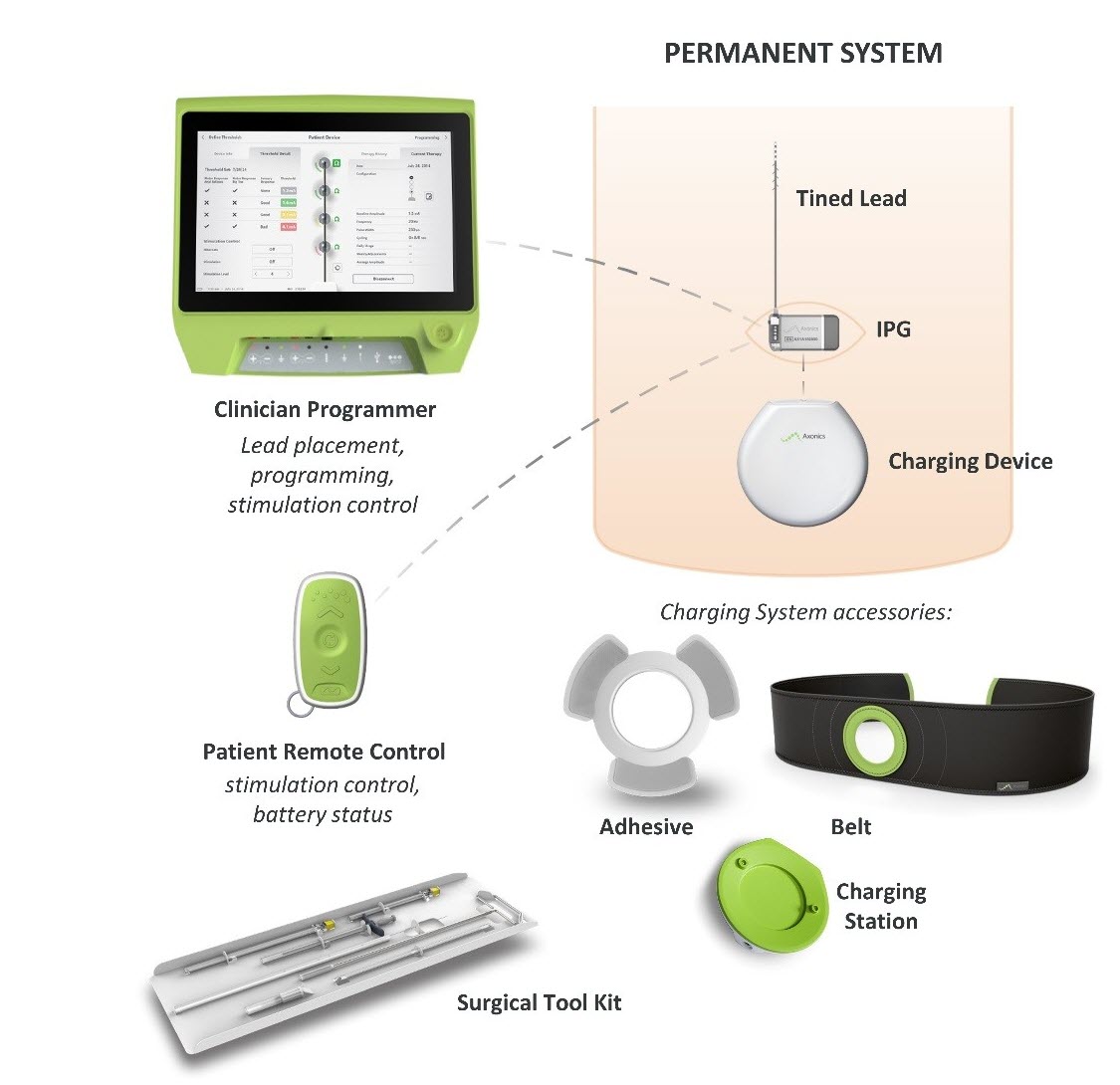
Miről van szó? Az Axonics Sacralis Neuromodulációs (SNM) rendszer egy szakrális idegstimulációs (SNS) rendszer, amely a vizeletvisszatartás és a túlműködő hólyag tüneteinek kezelésére szolgál. Egy beültetett stimulátort használ, amely elektromos impulzusokat juttat egy vezetéken keresztül a keresztcsonti ideg közelében található elektródákhoz.
Hogyan működik? A beültethető impulzusgenerátort (IPG) műtéti úton a bőr alá helyezik a felső fenéktájékon, és egy vezetékes vezetékhez csatlakoztatják, amely a medence csípőcsontjai között halad, és a keresztcsonti idegnél végződik. Az IPG elektromos impulzusokat küld az ólomkábelen keresztül a keresztcsonti idegnek, amely a gerincvelőből a hólyagba jut, hogy segítsen a vizeletszabályozás javításában.
Mikor alkalmazzák? Az Axonics SNM rendszert vizeletszabályozásra a vizeletvisszatartás és a túlműködő hólyag tüneteinek kezelésére használják olyan betegeknél, akiknél más kezelések, például életmódváltás, medencefenékgyakorlatok vagy gyógyszeres kezelés sikertelen volt vagy nem tolerálták azokat. Kezelés nélkül a vizeletvisszatartás és a túlműködő hólyag csökkentheti a páciens életminőségét, és jelentős kihívásokat okozhat a mindennapi életvitel fenntartásában.
Mit ér el? Az Axonics SNM rendszerrel végzett klinikai vizsgálat eredményei, valamint a hasonló SNM eszközzel kapcsolatban rendelkezésre álló szakirodalom szisztematikus áttekintéséből összeállított további klinikai adatok azt mutatják, hogy a vizeletvisszatartásban és a túlműködő hólyag tüneteiben szenvedő legtöbb olyan beteg számára, akiknél más kezelések sikertelenek voltak vagy nem tolerálták azokat, előnyösek. A sürgősségi inkontinenciában szenvedő betegek körében végzett Axonics klinikai vizsgálatban a beültetett SNM rendszerrel ellátott betegek 90%-ánál (116/129) 6 hónap alatt legalább 50%-kal csökkent a sürgősségi szivárgások száma az SNM rendszer nélküli sürgősségi szivárgások számához képest. Egy hosszabb távú vizsgálatban (van Kerrebroeck, 2007) 152, hasonló SNM eszközzel beültetett beteget követtek 5 éven keresztül. Az 5 év elteltével a sürgősségi inkontinenciában szenvedő betegek 58%-ánál (56/96) legalább 50%-os javulás volt tapasztalható (a napi szivárgások számában mérve). Továbbá 5 év elteltével a sürgősségi inkontinenciában szenvedő betegek 40%-ánál (10/25) legalább 50%-os javulás volt tapasztalható (a napi ürítések számában mérve), és a vizeletvisszatartásban szenvedő betegek 58%-ánál (18/31) legalább 50%-os javulás volt tapasztalható (a napi katéterezések számában mérve). Tekintettel a kialakítás, a technológia, a teljesítmény, a felhasználási javallatok, a kimeneti jellemzők és a kezelendő betegpopuláció hasonlóságára, az FDA úgy véli, hogy az Axonics SNM rendszer hasonló teljesítményt nyújt, mint a kereskedelmi forgalomban kapható SNM rendszer, amelyet a közzétett vizsgálatokban értékeltek.
Mikor nem szabad használni? Az Axonics SNM rendszer nem alkalmazható:
- Pácienseknél, akik nem mutattak megfelelő választ a tesztstimulációra; vagy
- Pácienseknél, akik nem képesek az Axonics SNM rendszer kezelésére
Kiegészítő információk (beleértve a figyelmeztetéseket, óvintézkedéseket és mellékhatásokat):
- A biztonságossági és hatásossági adatok összefoglalása
- Páciensek címkézése
- Az orvosok címkézése
- PMA adatbázisba történő bejegyzés
.