US Pharm. 2012;37(6):26-29.
La malattia renale cronica (CKD) è definita come un danno renale persistente accompagnato da una riduzione del tasso di filtrazione glomerulare (GFR) e la presenza di albuminuria. La prevalenza della CKD è aumentata costantemente negli ultimi due decenni ed è stata riportata come affetta da oltre il 13% della popolazione statunitense nel 2004.1 Nel 2009, più di 570.000 persone negli Stati Uniti sono state classificate come affette da malattia renale allo stadio terminale (ESRD), compresi quasi 400.000 pazienti in dialisi e oltre 17.000 destinatari di trapianto.2 Un paziente è determinato ad avere ESRD quando richiede una terapia sostitutiva, compresa la dialisi o il trapianto di rene. L’aumento dell’incidenza della CKD è attribuito all’invecchiamento della popolazione e all’aumento dell’ipertensione (HTN), del diabete e dell’obesità nella popolazione statunitense. CKD è associato con una serie di complicazioni tra cui squilibri elettrolitici, minerali e disturbi ossei, anemia, dislipidemia e HTN. È noto che la CKD è un fattore di rischio per le malattie cardiovascolari (CVD), e che un ridotto GFR e l’albuminuria sono indipendentemente associati a un aumento della mortalità cardiovascolare e di tutte le cause.3,4
HTN è stato segnalato per verificarsi in 85% al 95% dei pazienti con CKD (fasi 3-5).5 La relazione tra HTN e CKD è ciclica in natura. L’HTN incontrollata è un fattore di rischio per lo sviluppo della CKD, è associata a una più rapida progressione della CKD ed è la seconda causa principale di ESRD negli Stati Uniti.6,7 Nel frattempo, la malattia renale progressiva può esacerbare l’HTN incontrollata a causa dell’espansione del volume e dell’aumento della resistenza vascolare sistemica.Molteplici linee guida discutono l’importanza di abbassare la pressione sanguigna (BP) per rallentare la progressione della malattia renale e ridurre la cardiovasculmorbilità e la mortalità.8-10 Tuttavia, per raggiungere e mantenere un adeguato controllo della pressione, la maggior parte dei pazienti con CKD richiedono combinazioni di agenti antipertensivi; spesso possono essere necessarie fino a tre o quattro classi di farmaci.11
Patofisiologia
L’ipertensione è una delle cause principali della CKD a causa degli effetti deleteri che l’aumento della pressione ha sulla vascolarizzazione renale. I danni ai glomeruli portano a un aumento della filtrazione delle proteine, con conseguente aumento della quantità di proteine nelle urine (microalbuminuria o proteinuria).12,13 La microalbuminuria è la presentazione di piccole quantità di albumina nelle urine ed è spesso il primo segno di CKD. La proteinuria (rapporto proteine/creatinina ≥200 mg/g) si sviluppa con il progredire della CKD ed è associata a una prognosi sfavorevole sia per la malattia renale che per la CVD.3,4,14
Come discusso in precedenza, la relazione tra CKD e HTN è ciclica, poiché la CKD può contribuire o causare la HTN. L’elevata pressione sanguigna porta al danneggiamento dei vasi sanguigni all’interno del rene, così come in tutto il corpo. Questo danno compromette la capacità del rene di filtrare il fluido e i rifiuti dal sangue, portando a un aumento del volume del fluido nel sangue, causando così un aumento della BP.
Staging della CKD
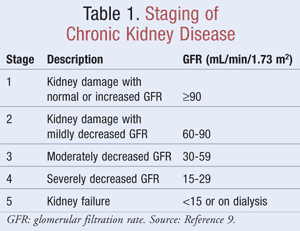
Il GFR stimato, che aiuta i medici a determinare quanto bene i reni stanno filtrando i rifiuti, è usato nella staging della CKD. La National Kidney Foundation definisce la CKD come un danno renale, identificato da marcatori nelle urine o nel sangue o da immagini, con o senza cambiamenti nel GFR, o un GFR <60 mL/min/1.73 m2 per un minimo di 3 mesi.9 La TABELLA 1 illustra i criteri di stadiazione secondo le linee guida della Kidney Disease Outcomes Quality Initiative (K/DOQI).9
Obiettivi della terapia
I pazienti con CKD non diabetica e diabetica dovrebbero avere un obiettivo di pressione sanguigna <130/80 mmHg.8-10Mantenere il controllo della BP e ridurre al minimo la proteinuria nei pazienti con CKD e HTN è essenziale per la prevenzione della progressione della malattia renale e lo sviluppo o il peggioramento della CVD.8,9
La letteratura recente suggerisce che gli obiettivi della BP nella CKD diabetica e non diabetica possono aver bisogno di essere individualizzati in base alla presenza di proteinuria. Alcuni studi non hanno dimostrato una riduzione degli esiti cardiovascolari o renali nei pazienti diabetici e non diabetici con CKD quando si raggiunge un obiettivo di BP di <130/80 mmHg rispetto all’abbassamento della BP a <140/90 mmHg.15,16 Tuttavia, i pazienti che hanno proteinuria hanno meno probabilità di sperimentare un declino della funzione renale, insufficienza renale o morte quando si raggiunge l’obiettivo di BP inferiore.15,17È probabile che le linee guida future possano includere un obiettivo di pressione più basso, <130/80 mmHg, per i pazienti con proteinuria, ma mantenere un obiettivo di<140/90 mmHg per i pazienti senza proteinuria.
Trattamento
Gli agenti che non solo abbassano la pressione ma riducono anche la proteinuria sono raccomandati come terapia di prima linea per la maggior parte dei pazienti con CKD eHTN; i dati indicano che ci possono essere significativi benefici a lungo termine in entrambi gli esiti cardiovascolari e renali quando la proteinuria è diminuita.9Diverse classi di agenti antipertensivi possono avere un ruolo nel trattamento di CKD e HTN. Gli agenti che mirano al sistema renina-angiotensina-aldosterone (RAAS), come gli inibitori dell’enzima di conversione dell’angiotensina (ACE) o i bloccanti del recettore dell’angiotensina (ARB), sono generalmente considerati la terapia antipertensiva di prima linea per questa popolazione di pazienti.8,9,18 La TABELLA 2 fornisce indicazioni sugli agenti antipertensivi raccomandati per i pazienti con CKD con o senza diabete e con o senza proteinuria.
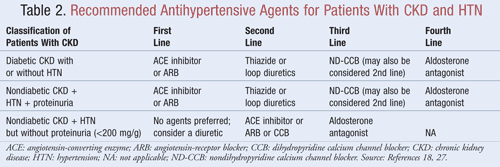
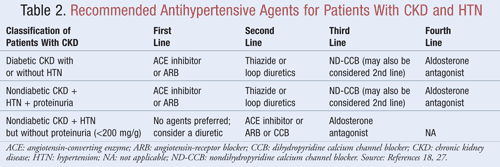
Inibitori dell’ACE o ARB: Gli studi hanno dimostrato che gli agenti antipertensivi che hanno come bersaglio il sistema renina-angiotensina prevengono il declino renale più di altri agenti, anche quando si raggiungono obiettivi BP simili.19 Questi risultati sono stati trovati principalmente nei pazienti con proteinuria, mentre il beneficio era meno sostanziale per quelli senza proteinuria. Sulla base di questi risultati, le linee guida raccomandano la terapia con ACE-inibitori o ARB come trattamento di prima linea per i pazienti con diabete o quelli che presentano una malattia renale non diabetica, HTN e proteinuria. I dati indicano che gli ACE inibitori e gli ARB sono ugualmente efficaci nell’abbassare la pressione sanguigna e nel ridurre la proteinuria.20 Una recente meta-analisi suggerisce che la terapia con ACE inibitore può fornire un beneficio superiore alla terapia ARB per il trattamento dell’HTN grazie a una riduzione del 10% della mortalità per tutte le cause.21 Questi risultati sono stati determinati per i pazienti con HTN e non si applicano ai pazienti con ulteriori comorbidità come la CKD. Pertanto, la selezione di un agente rispetto a un altro dipenderà da fattori specifici del paziente come i potenziali effetti collaterali e il costo. Il trattamento con un ACE inibitore e un ARB non è raccomandato, poiché è stato dimostrato che questa combinazione peggiora la funzione renale. La terapia combinata di ACE-inibitore e ARB non ha ridotto la mortalità o la morbilità cardiovascolare rispetto alla monoterapia di un ACE-inibitore.20,21
Gli ACE-inibitori e gli ARB sono generalmente ben tollerati. Gli ACEinibitori possono causare una tosse secca, che purtroppo spesso richiede un cambiamento della terapia. Gli ARB non sono associati a tosse secca. L’angioedema è molto raro; tuttavia, i pazienti iniziati con ACE inibitori o ARB devono essere informati dei segni e dei sintomi che possono presentarsi con l’angioedema. Informare i pazienti che l’angioedema è improbabile, ma se si sperimenta il dolore al viso (spesso comprese le palpebre) e/o alle estremità, devono interrompere il trattamento e cercare un medico immediatamente.18
Thiazide vs. Diuretici ad anello: Per i pazienti senza proteinuria, una terapia di prima linea preferita non è stata chiaramente stabilita, e altri agenti, come una tiazide, possono essere presi in considerazione. I pazienti con CKD e HTN spesso sperimentano ritenzione di liquidi o sovraccarico di liquidi. Di conseguenza, i diuretici sono spesso necessari nel loro regime di trattamento. I tiazidici sono raccomandati per i pazienti con CKD di stadio da 1 a 3 (GFR ≥30 mL/min), e sono stati stabiliti come agenti efficaci per la riduzione della BP e del rischio CVD.22 I diuretici dell’ansa sono raccomandati per i pazienti con CKD di stadio 4 o 5 (GFR <30 mL/min), poiché hanno dimostrato di essere più efficaci nel ridurre il volume del fluido extracellulare nei pazienti con GFR gravemente ridotto.18 Tuttavia, l’effetto a lungo termine dei diuretici dell’ansa sugli esiti cardiovascolari non è stato chiaramente stabilito.23
I diuretici taizidici (clortalidone, idroclorotiazide) e i diuretici dell’ansa (bumetanide, furosemide, torsemide) causano tutti iperuricemia (aumento della minzione). Questo aumento della perdita di liquidi può portare a uno squilibrio elettrolitico. È importante per i pazienti su theseagents per avere loro elettroliti monitorati per garantire che essi notexperience anomalie elettrolitiche come iperkalemia orhypomagnesemia. L’ipotensione ortostatica può verificarsi in risposta a qualsiasi agenti antipertensivi; tuttavia, è comune con i diuretici. È importante consigliare i pazienti che iniziano la terapia diuretica sulla necessità di alzarsi lentamente da una posizione seduta o sdraiata.24,25
Bloccanti del canale del calcio: I calcioantagonisti (CCB) sono considerati una terapia di seconda o terza linea nel trattamento dell’HTN in pazienti con CKD.8,9 Anche se non ci può essere alcuna differenza nell’effetto sull’abbassamento della pressione tra i CCB nondiidropiridinici (ND-CCB; ad esempio, diltiazem, verapamil) e i CCB diidropiridinici (ad esempio amlodipina, nifedipina), gli ND-CCB hanno dimostrato di ridurre significativamente la proteinuria sia quando usati da soli che in combinazione con un ACE inibitore o un ARB.26 A causa del loro potenziale di ridurre la proteinuria, oltre ai loro effetti antipertensivi, gli ND-CCB dovrebbero essere considerati come terapia di seconda o terza linea nei pazienti con CKD diabetica o non diabetica con proteinuria. I CCB diidropiridinici possono essere usati come agenti di seconda linea in pazienti con CKD non diabetica senza proteinuria. Gli effetti avversi comuni includono edema e costipazione con ND-CCBs (specialmenteverapamil) e vampate di calore ed edema periferico con dihydropyridineagents.18
Antagonisti dell’aldosterone: L’aldosterone gioca un ruolo gravemente deleterio nella progressione della CKD. Gli antagonisti del recettore dell’aldosterone (ad esempio, spironolattone, eplerenone) possono avere un posto nel ruolo della terapia CKD quando gli obiettivi di BP non sono stati raggiunti con la terapia di prima e seconda linea. Questi agenti hanno dimostrato negli studi clinici di fornire una riduzione della proteinuria se aggiunti a un ACE-inibitore o ARB.27,28
Gli antagonisti dell’aldosterone sono diuretici risparmiatori di potassio, che aumentano il rischio di iperkaliemia, in particolare se assunti con unACE-inibitore o ARB. È importante che i pazienti iniziati con diuretici risparmiatori di potassio abbiano i loro livelli di potassio controllati per assicurarsi di non avere anomalie elettrolitiche. Sintomi di iperkaliemia includono aritmia cardiaca e grave debolezza muscolare. Purtroppo, iperkaliemia può presentare asintomatico, che sottolinea l’importanza del monitoraggio.18,27
Inibitore della renina: Aliskiren è l’unico inibitore della renina attualmente disponibile sul mercato. È indicato per il trattamento dell’HTN come monoterapia o come terapia combinata con il valsartan. I dati recenti del trial ALTITUDE hanno portato alla controindicazione del suo uso con ACE inibitori o ARB in pazienti con diabete o insufficienza renale (GFR <60 mL/min) a causa dell’aumentato rischio di insufficienza renale, ipotensione e iperkaliemia.29 Aliskiren può essere considerato se il paziente non può assumere un ACE inibitore o un ARB; tuttavia, il suo uso non può essere raccomandato in pazienti con insufficienza renale di stadio 4 o 5.30
Beta-Bloccanti: I dati che valutano l’effetto dei beta-bloccanti sulla progressione della CKD e della proteinuria sono limitati.27 Mentre i beta-bloccanti non sono inclusi nella TABELLA 2, questi agenti possono essere considerati come terapia di seconda o terza linea se il paziente ha un’indicazione convincente per un beta-bloccante come la malattia coronarica o l’insufficienza cardiaca cronica.18
Consigli non farmacologici
Cronoterapia: Questo tipo di terapia prende in considerazione i modelli circadiani della pressione, e istituisce la somministrazione di farmaci antipertensivi rispetto ai modelli giornalieri, allontanandosi dalla somministrazione di tutti i farmaci antipertensivi al mattino. Gli studi hanno dimostrato un migliore controllo della pressione nelle 24 ore nei pazienti che somministrano CCB la sera piuttosto che la mattina.31,32 Altri studi hanno identificato un beneficio dalla somministrazione notturna di altri farmaci antipertensivi come gli ACEinibitori o gli ARB.33,34 La cronoterapia può giustificare qualche considerazione per coloro che non riescono a raggiungere il loro obiettivo di pressione quando si somministrano tutti gli agenti antipertensivi al mattino. Se patientsare su più di due agenti antipertensivi, può essere opportuno per somministrare due agenti al mattino e gli agenti aggiuntivi in theevening.
Modificazione dello stile di vita: Maggiore attività fisica, perdita di peso e modifiche della dieta sono raccomandati per tutti i pazienti con HTN.8La modifica dello stile di vita rimane una componente critica della terapia per HTN, indipendentemente dal fatto che i pazienti richiedono farmaci per raggiungere il loro BPgoal. La dieta Dietary Approaches to Stop Hypertension (DASH) enfatizza un maggiore consumo di frutta e verdura, l’inclusione di latticini a basso contenuto di grassi e proteine magre, e una restrizione dei grassi saturi; questo piano alimentare ha dimostrato di abbassare significativamente la pressione sistolica quasi equivalente alla riduzione ottenuta dalla monoterapia antipertensiva.35 Inoltre, la diminuzione dell’assunzione di sodio e alcol è stato stabilito come un intervento efficace per diminuire la pressione.8L’avvio di queste pratiche dietetiche sane mentre si aumenta l’attività quotidiana aumenta il beneficio ricevuto dalla terapia antipertensiva e può svolgere un ruolo essenziale nel raggiungimento degli obiettivi della BP.
Sommario
L’interrelazione di CKD e HTN porta a sottolineare ulteriormente l’importanza di raggiungere il controllo della BP e di diminuire la proteinuria, se presente. Gli agenti che riducono la proteinuria oltre alla BP sono generalmente di prima linea, ma i pazienti possono spesso richiedere da tre a quattro agenti antipertensivi per raggiungere i loro obiettivi e minimizzare il loro rischio di CVD e ESRD. Inoltre, le modifiche dello stile di vita sano dovrebbero sempre essere considerate come una componente vitale di qualsiasi regime di terapia antipertensiva.
1. Coresh J, Selvin E, Stevens LA, et al. Prevalenza della malattia renale cronica negli Stati Uniti. JAMA. 2007;298:2038-2047.
2. Collins AJ, Foley RN, Chavers B, et al. U.S. renal data system 2011 annual data report. Am J Kidney Dis. 2012;59(suppl 1):evii.
3. Matsushita K, van der Velde M, Astor BC, et al.Association of estimated glomerular filtration rate and albuminuria withall-cause and cardiovascular mortality in general population cohorts: acollaborative meta-analysis. Lancet. 2010;375:2073-2081.
4. Rashidi A, Sehgal AR, Rahman M, O’Connor AS. La malattia renale cronica, il diabete mellito e l’infarto miocardico sono fattori di rischio equivalenti per la mortalità cardiovascolare in pazienti di età superiore ai 65 anni. Am J Cardiol. 2008;102:1668-1673.
5. Rao MV, Qiu Y, Wang C, Bakris G. Ipertensione e CKD: Kidney Early Evaluation Program (KEEP) e National Health and NutritionExamination Survey (NHANES), 1999-2004. Am J Kidney Dis. 2008;51(suppl 2):S30-S37.
6. Botdorf J, Chaudhary K, Whaley-Connell A. Ipertensione nella malattia cardiovascolare e renale. Cardiorenal Med. 2011;1:183-192.
7. Segura J, Ruilope L. Ipertensione nei pazienti non diabetici CKD moderati-gravi. Adv Chronic Kidney Dis. 2011;18:23-27.
8. Chobanian AV, Bakris GL, Black HR, et al. Il settimo rapporto del comitato nazionale congiunto sulla prevenzione, rilevamento, valutazione e trattamento di alta pressione sanguigna: il rapporto JNC 7. JAMA. 2003;289:2560-2572.
9. Fondazione Nazionale del Rene. K/DOQI clinical practiceguidelines for chronic kidney disease: evaluation, classification, andstratification. Am J Kidney Dis. 2002;39(suppl 1):S1-S266.
10. Associazione americana del diabete. Standard di assistenza medica nel diabete-2012. Cura del diabete. 2012;35(suppl 1):S1-S63.
11. Bakris GL, Williams M, Dworkin L, et al. Preservare la funzione renale negli adulti con ipertensione e diabete: un approccio di consenso. Gruppo di lavoro del National Kidney Foundation Hypertension and Diabetes ExecutiveCommittees. Am J Kidney Dis. 2000;36:646-661.
12. Keane WF, Eknoyan G. Proteinuria, albuminuria, rischio, valutazione, rilevamento, eliminazione (PARADE): un documento di posizione per la National Kidney Foundation. Am J Kidney Dis. 1999;33:1004-1010.
13. Yoshioka T, Rennke HG, Salant DJ, et al. Role ofabnormally high transmural pressure in the permselectivity defect ofglomerular capillary wall: a study in early passive Heymann nephritis. Circ Res. 1987:61:531-538.
14. Sarnak M, Levey A, Schoolwerth A, et al. Kidneydisease come fattore di rischio per lo sviluppo di malattie cardiovascolari: astatement dall’American Heart Association Councils on Kidney inCardiovascular Disease, High Blood Pressure Research, ClinicalCardiology ed Epidemiologia e Prevenzione. Circolazione. 2003;108:2154-2169.
15. Upadhyay A, Earley A, Haynes SM, Uhlig K. Systematicreview: obiettivo di pressione sanguigna nella malattia renale cronica e proteinuriaas un modificatore di effetto. Ann Intern Med. 2011;154:541-548.
16. Cushman C, Evan GW Byington RP, et al. The ACCORDstudy group. Controllo intensivo della pressione sanguigna nel diabete mellito tipo 2. N Engl J Med. 2010;363:1575-1585.
17. Brenner BM, Cooper ME, De Zeeuw D, et al. Effetti dellosartan sugli esiti renali e cardiovascolari nel diabete di tipo 2 e nefropatia. N Engl J Med. 2001;345:861-869.
18. Kidney Disease Outcomes Quality Initiative (K/DOQI).K/DOQI clinical practice guidelines on hypertension and antihypertensiveagents in chronic kidney disease. Am J Kidney Dis. 2004;43(suppl 1):S1-S290.
19. Remuzzi G, Chiurchiu C, Ruggenenti P. Proteinuria predicting outcome in renal disease: nefropatie non diabetiche (REIN). Kidney Int Suppl. 2004;66:S90-S96.
20. Sharma P, Blackburn RC, Parke CL, et al.Angiotensin-converting enzyme inhibitors and angiotensin receptorblockers for adults with early (stage 1 to 3) non-diabetic chronickidney disease. Cochrane Database Syst Rev. 2011;(10):CD007751.
21. van Vark LC, Bertrand M, Akkerhuis KM, et al.Angiotensin-converting enzyme inhibitors reduce mortality inhypertension: a meta-analysis of randomized clinical trials ofrenin-angiotensin-aldosterone system inhibitors involving 158,998patients. Eur Heart J. 2012 Apr 17; Epub ahead of print.
22. Risultati principali in pazienti ipertesi ad alto rischio randomizzati a inibitore dell’enzima di conversione dell’angiotensina o calcio-antagonista vs diuretico: il Antihypertensive and Lipid-Lowering Treatmentto Prevent Heart Attack Trial (ALLHAT). JAMA. 2002;288:2981-2997.
23. Musini VM, Wright JM, Bassett K, Jauca CD. Efficacia dell’abbassamento della pressione sanguigna dei diuretici dell’ansa per l’ipertensione primaria. Cochrane Database Syst Rev. 2009;(4):CD003825.
24. Microzide (idroclorotiazide capsule orali) foglietto illustrativo. Watson Pharma, Inc: Morristown, NJ; 2011.
25. Clortalidone compresse orali foglietto illustrativo. Mylan Pharmaceuticals, Inc: Morgantown, WV; 2006.
26. Bakris GL, Weir MR, Secic M, et al. Differentialeffetti di sottoclassi di calcio antagonista su marcatori di nefropatiaprogressione. Rene Int. 2004; 65: 1991-2002.
27. Navaneethan SD, Nigwekar SU, Sehgal AR, et al.Aldosterone antagonisti per prevenire la progressione del kidneydisease cronica. Clin J Am Soc Nephrol. 2009;4:542-551.
28. Mehdi UF, Adams-Huet B, Raskin P, et al. Aggiunta di blocco del recettore dell’angiotensina o antagonismo mineralocorticoide alla massima inibizione dell’enzima di conversione dell’angiotensina nella nefropatia diabetica. J Am Soc Nephrol. 2009;20:2641-2650.
29. Farmaci contenenti aliskiren: comunicazione sulla sicurezza del farmaco-nuovo avviso e controindicazione. MedWatch.April 20, 2012.www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm301120.htm?source=govdelivery;4/20/2012.Accessed May 1, 2012.
30. Trimarchi H. Ruolo dell’aliskiren nel controllo della pressione sanguigna e nella renoprotezione. Int J Nephrol Renovasc Dis. 2011;4:41-48.
31. Portaluppi F, Vergnani L, Manfredini R, et al.Effetto tempo-dipendente di isradipina sull’ipertensione notturna inchronica insufficienza renale. Am J Hypertens. 1995;8:719-726.
32. Hermida RC, Calvo C, Ayala DE, et al. Effetti dipendenti dalla dose e dal tempo di somministrazione della nifedipina GITS sulla pressione sanguigna ambulatoriale in soggetti ipertesi. Chronobiol Int. 2007;24:471-493.
33. Hermida RC, Ayala DE. Cronoterapia con l’inibitore dell’enzima di conversione dell’angiotensina ramipril nell’ipertensione essenziale: controllo della pressione sanguigna migliorato con il dosaggio di notte. Ipertensione. 2009;54:40-46.
34. Hermida RC, Calvo C, Ayala DE, et al. Effetti dipendenti dal tempo di somministrazione di valsartan sulla pressione sanguigna ambulatoriale in soggetti ipertesi. Ipertensione. 2003;42:283-290.
35. Sacks FM, Svetkey LP, Vollmer WM, et al. Effetti sulla pressione sanguigna di ridotto sodio dietetico e la dieta Dietary Approaches toStop Hypertension (DASH). DASH-Sodium Collaborative Research Group.N Engl J Med. 2001;344:3-10.