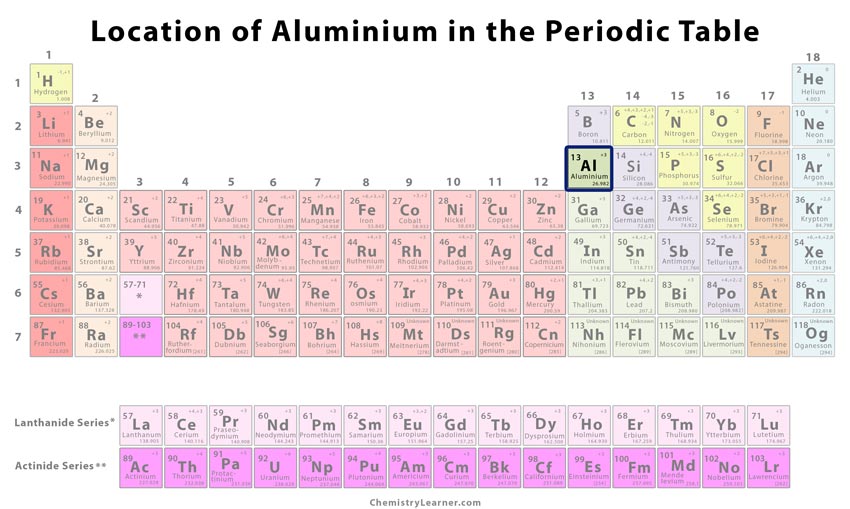
Che cos’è l’alluminio
L’alluminio (pronunciato come ah-LOO-men-em) è un metallo morbido e leggero, rappresentato dalla sostanza chimica Al. Esiste sotto forma di diversi composti minerali, avendo una vasta gamma di usi commerciali grazie alla sua natura non tossica e all’alta resistenza alla corrosione. Ha 15 isotopi con numeri di massa che vanno da 22 a 35 di cui solo l’Al-26 è radioattivo con un’emivita di 7,17×105 anni e l’Al-27 esiste naturalmente.

Dove si può trovare
L’elemento costituisce circa l’8,1% della crosta terrestre rendendolo uno dei metalli più abbondanti. Si può trovare combinato con altri metalli sotto forma di minerali di silicato come la criolite e la bauxite. La sua produzione su scala commerciale è fatta da un processo chimico costoso chiamato processo Hall-Heroult che implica una grande quantità di energia.
Storia
Origine del suo nome: Il suo nome deriva dalla parola latina per allume chiamata ‘alumen’ che significa sale amaro.
Chi l’ha scoperto: Hans Oersted
Quando, dove e come fu scoperto
Si credeva che durante il 3° secolo in Cina la tomba di un capo militare chiamato Chou-Chu contenesse circa l’85% di alluminio. Nel 1700 fu anche coniata la presenza dell’ossido del metallo, ma non fu possibile fare ulteriori analisi. Infatti, il chimico della Cornovaglia Henry Davy cercò di estrarre il sodio e il potassio dai loro rispettivi ossidi, ma l’Al non poté essere ottenuto.
Solo nel 1825 Oersted a Copenhagen, Danimarca, riscaldò il cloruro di alluminio con il potassio ed estrasse una forma impura del metallo. Nel 1827 Friedrich Wohler, il chimico tedesco, ripeté finalmente il metodo usando il sodio e ottenne un campione puro.

Classificazione, proprietà e caratteristiche dell’alluminio
Proprietà generali |
|
| Massa atomica relativa/media | 26.982 |
| Massa atomica/peso | 26.982 unità di massa atomica |
| Massa molecolare/peso molecolare | 26.982 g/mol |
| Numero di massa | 27 |
Proprietà fisiche |
|
| Colore/aspetto fisico | Bianco argento |
| Punto di fusione/congelamento | 660.323°C (1220.581°F) |
| Punto di ebollizione | 2519°C (4566°F) |
| Densità | 2.70 g/cm3 |
| Standard/stato fisico della materia alla normale temperatura ambiente (solido/liquido/gas) | Solido |
| Duttilità | Sì |
| Malleabilità | Sì |
| Durezza | 2.9 Mohs |
| Conducibilità elettrica | 37.6676 x 106 Sm-1 |
| Conducibilità termica | 237 Wm-1K-1 |
| Capacità termica specifica | 0.90 Jg-1K-1 |
| Gravità specifica | 2.8 |
| Restività | 2.65 x10-8ρ (ohm m) |
| Resistenza alla trazione | 90 Mpa |
| Coefficiente di temperatura | 0.00393 α/°C |
| Resistenza alla trazione | 276 Mpa |
| Coefficiente di espansione termica lineare/trasferimento del calore | 23,1 10-6K-1 |
| Coefficiente di attrito | 1.35 |
Proprietà chimiche |
|
| Infiammabilità | Infiammabile |
| Stati di ossidazione (numeri) | 3 |
Dati atomici dell’alluminio
| Elettroni di valenza | 1 | ||||||
| Configurazione degli elettroni (configurazione dei gas nobili) | 3s23p1 | ||||||
| Struttura del cristallo | Cubico centrato sulla facciacubica centrata sulla faccia | ||||||
| Costante di lattice/parametro | 0.405 nm | ||||||
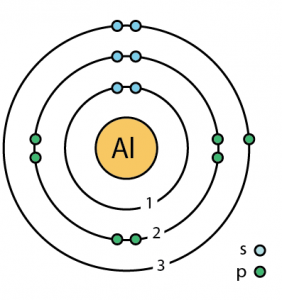
| Livelli energetici | |||||||
| Primo livello energetico | 2 | ||||||
| Secondo livello energetico | 8 | ||||||
| Terzo livello energetico | 3 | ||||||
| Struttura atomica | |||||||
| – Numero di elettroni | 13 | ||||||
| – Numero di neutroni | 14 | ||||||
| – Numero di protoni | 13 | ||||||
| Raggio dell’atomo | |||||||
| – Raggio atomico | 1.84 Å | ||||||
| – Raggio covalente | 1,24 Å | ||||||
| Elettronegatività | 1.61 | ||||||
| Carica dello ione | +1 | ||||||
| Energia di ionizzazione
(kJmol-1) |
1° | 2° | 3° | 4° | 5° | 6° | 7° |
| 577.539 | 1816.679 | 2744.781 | 11577.469 | 14841.857 | 18379.49 | 23326.3 | |
A cosa serve comunemente l’alluminio
- E’ usato in una vasta gamma di prodotti come pannelli per recinzioni, pannelli per cancelli di recinzione, lattine, tubi, cablaggi, lamine, coperture, friggitrici, padelle, ringhiere, rivestimenti, coperture per patio, ruote, bacchette per brasatura, porte per schermi, radiatori, serbatoi per gas e pali.
- Buon conduttore di elettricità, Al fa un sostituto ideale per il rame in termini di costo e peso per fare linee di trasmissione elettrica.
- L’alluminio è legato con altri metalli come il rame, il magnesio, il silicio e il manganese per fare cuscinetti a sfera, parti di automobili, razzi e aeroplani.
- Il metallo è spesso usato come rivestimento riflettente su specchi per telescopi, giocattoli, pacchetti, decorativi e carte decorative per proteggere dalla luce e dal calore.
- Come alternativa alle batterie costose e ai combustibili liquidi, le celle/batterie ad aria a ioni di alluminio sono più convenienti e portatili per l’uso .

L’elemento ha effetti tossici
L’inalazione di polveri o fumi contenenti Al colpisce il sistema respiratorio, causando tosse e altri disturbi legati ai polmoni. L’ingestione prolungata del metallo sotto forma di alcuni prodotti orali può essere dannosa per i reni e aumentare la possibilità del morbo di Alzheimer.

Fatti interessanti
- Prima della scoperta del processo di Hall-Heroult, l’Al puro era più costoso dell’oro e per questo chiamato il ‘Re dei metalli’
- Il metallo può essere riciclato più volte senza compromettere la sua qualità.

Prezzo dell’alluminio
Il costo del puro può variare da qualche parte tra 0,9 e 1 dollaro.
- http://www.rsc.org/periodic-table/element/13/aluminium
- https://education.jlab.org/itselemental/ele013.html
- https://pubchem.ncbi.nlm.nih.gov/compound/aluminum#section=Computed-Properties
- https://www.chemicool.com/elements/aluminum.html
- http://hyperphysics.phy-astr.gsu.edu/hbase/Tables/rstiv.html
- https://www.tedpella.com/company_html/hardness.htm
- http://asm.matweb.com/search/SpecificMaterial.asp?bassnum=ma6061t6
- https://study.com/academy/answer/how-many-valence-electrons-does-aluminum-have.html
- http://www.chemicalelements.com/elements/al.html
- https://www.sciencedirect.com/science/article/pii/S0378775307002236
- https://www.atsdr.cdc.gov/phs/phs.asp?id=1076&tid=34