Questa è una breve panoramica delle informazioni relative all’approvazione della FDA alla commercializzazione di questo prodotto. Vedere i link sottostanti al Riassunto dei dati di sicurezza ed efficacia (SSED) e all’etichettatura del prodotto per informazioni più complete su questo prodotto, sulle sue indicazioni d’uso e sulla base dell’approvazione della FDA.
Nome del prodotto: Axonics Sacral Neuromodulation System
PMA Richiedente: Axonics Modulation Technologies, Inc.
Indirizzo: 26 Technology Drive, Irvine, CA 92618
Data di approvazione: 13 novembre 2019
Lettera di approvazione: Approval Order
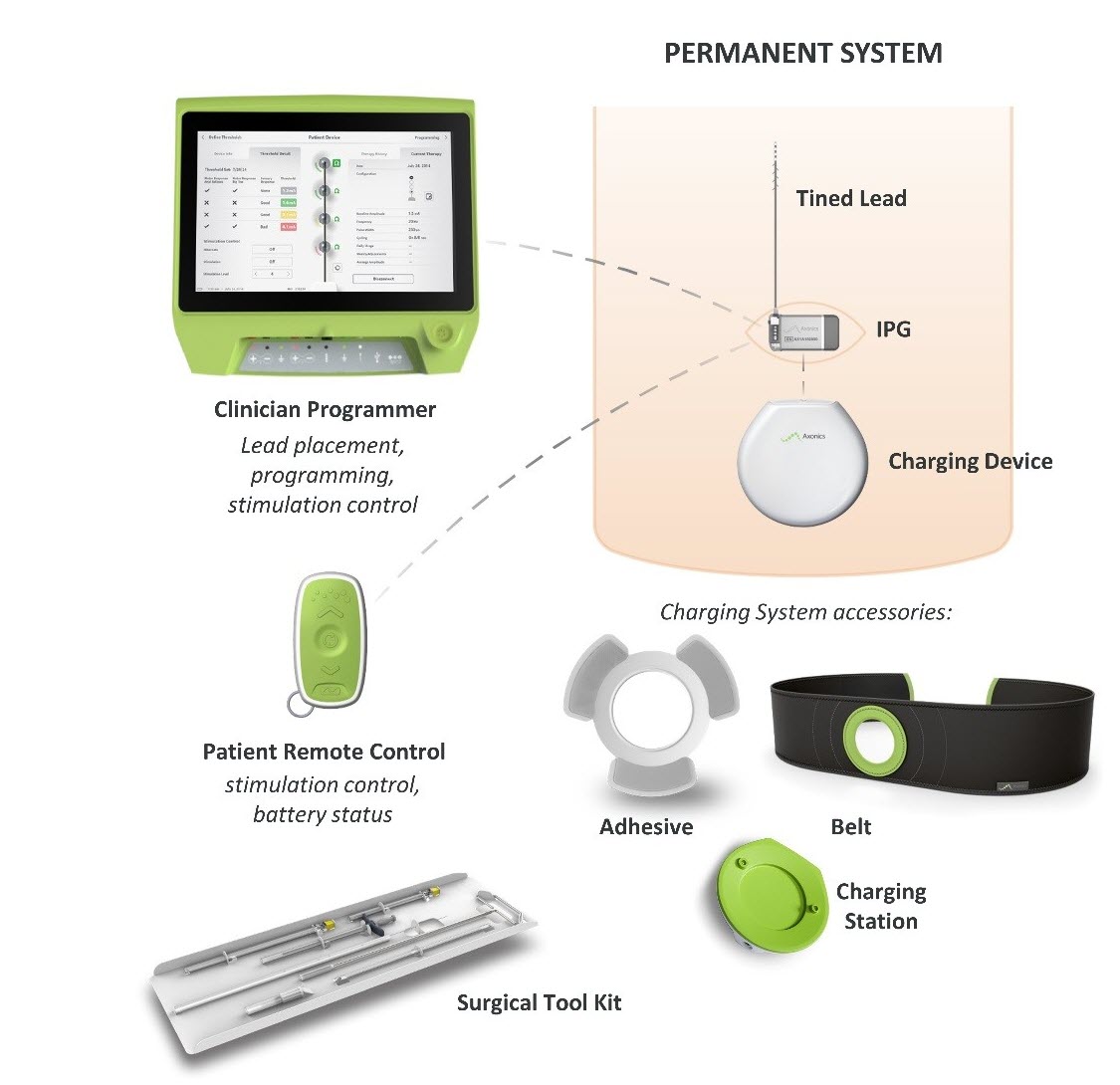
Che cos’è? Il sistema di neuromodulazione sacrale (SNM) Axonics è un sistema di stimolazione del nervo sacrale (SNS) destinato a trattare la ritenzione urinaria e i sintomi della vescica iperattiva. Utilizza uno stimolatore impiantato per fornire impulsi elettrici attraverso un filo di piombo ad elettrodi situati vicino al nervo sacrale.
Come funziona? Un generatore di impulsi impiantabile (IPG) viene posizionato chirurgicamente sotto la pelle nella zona superiore della natica e collegato a un filo di piombo che passa tra le ossa dell’anca del bacino e termina al nervo sacrale. L’IPG invia impulsi elettrici attraverso il cavo al nervo sacrale che viaggia dal midollo spinale alla vescica per aiutare a migliorare il controllo urinario.
Quando si usa? Il sistema Axonics SNM per il controllo urinario è utilizzato per il trattamento della ritenzione urinaria e dei sintomi della vescica iperattiva in pazienti che hanno fallito o non hanno potuto tollerare altri trattamenti, come cambiamenti dello stile di vita, esercizi del pavimento pelvico o farmaci. Se non trattata, la ritenzione urinaria e la vescica iperattiva possono ridurre la qualità della vita di un paziente e possono comportare sfide significative nel mantenimento delle attività della vita quotidiana.
Cosa si ottiene? I risultati di uno studio clinico del sistema Axonics SNM, combinati con ulteriori dati clinici compilati da una revisione sistematica della letteratura disponibile per un dispositivo SNM simile, mostrano che esiste un beneficio per la maggior parte dei pazienti con ritenzione urinaria e i sintomi della vescica iperattiva che hanno fallito o non hanno potuto tollerare altri trattamenti. Nello studio clinico Axonics su pazienti con incontinenza urinaria da urgenza, il 90% (116/129) dei pazienti con il sistema SNM impiantato ha ottenuto almeno una riduzione del 50% del numero di perdite da urgenza a 6 mesi rispetto al numero di perdite da urgenza senza il sistema SNM. In uno studio a lungo termine (van Kerrebroeck, 2007), 152 pazienti impiantati con un dispositivo SNM simile sono stati seguiti per 5 anni. A 5 anni, il 58% (56/96) dei pazienti con incontinenza urinaria da urgenza aveva almeno il 50% di miglioramento (misurato in termini di numero di perdite al giorno). Inoltre, dopo 5 anni, il 40% (10/25) dei pazienti con urgenza-frequenza aveva almeno il 50% di miglioramento (misurato in termini di numero di vuoti al giorno), e il 58% (18/31) dei pazienti con ritenzione urinaria aveva almeno il 50% di miglioramento (misurato in termini di numero di cateterismi al giorno). Date le somiglianze nel design, nella tecnologia, nelle prestazioni, nelle indicazioni per l’uso, nelle caratteristiche di uscita e nella popolazione di pazienti che è destinata a trattare, la FDA ritiene che il sistema Axonics SNM avrà prestazioni simili al sistema SNM disponibile in commercio valutato negli studi pubblicati.
Quando non dovrebbe essere usato? Il sistema Axonics SNM non deve essere usato in:
- Pazienti che non hanno dimostrato una risposta appropriata alla stimolazione del test; o
- Pazienti che non sono in grado di utilizzare il sistema Axonics SNM
Informazioni aggiuntive (incluse avvertenze, precauzioni ed eventi avversi):
- Sommario dei dati di sicurezza ed efficacia
- Etichettatura per il paziente
- Etichettatura per il medico
- Inserimento nel database della PMA