アルミニウムとは
アルミニウム(発音は ah-LOO-men-em )は、化学名Alで表される軟くて軽い金属である。 いくつかの鉱物化合物の形で存在し、毒性がなく、耐食性に優れているため、幅広い商業的用途を持っています。 質量数22~35の15の同位体があり、そのうち半減期7.17×105年の放射性物質であるAl-26と天然に存在するAl-27のみです。

Where Can it Be Found
地殻の約8.1%を占める最もありふれた金属元素の1つであり、その存在範囲は広い。 他の金属と一緒に、氷晶石やボーキサイトのような珪酸塩鉱物の形で見つけることができます。 商業規模での生産は、大量のエネルギーを必要とするホール・ヘロルト法と呼ばれる高価な化学プロセスによって行われます。
誰が発見したのか。 ハンス・エルステッド
いつ、どこで、どのように発見されたか
3世紀の中国で、周瑜という武将の墓に約85%のアルミニウムが含まれていると信じられていました。 1700年代には、この金属の酸化物の存在も造語されましたが、それ以上の分析ができなかったのです。 実際、コーンウォールの化学者ヘンリー・デイヴィーは、ナトリウムとカリウムをそれぞれの酸化物から抽出しようとしたが、アルミニウムは得られなかった。
1825年にデンマークのコペンハーゲンでエルステッドが塩化アルミニウムとカリウムを加熱して、この金属の不純物を抽出したのが最初である。 1827年、ドイツの化学者フリードリッヒ・ヴォーラーは、ナトリウムを使ってこの方法を繰り返し、ついに純度の高い試料を得た。

アルミニウムの分類、性質、特徴
General Properties |
|||||||||||
| 相対/平均原子質量 | 26.1Kg | 2.0Kg | 3.0Kg | 3.0Kg | 3.0Kg | 3.0Kg> | 3.2Kg982 | ||||
| 原子質量/重量 | 26.982 原子質量単位 | ||||||||||
| モル質量/分子量 | 26.982 g/mol | ||||||||||
| 質量数 | 27 | ||||||||||
物理的性質 |
|||||||||||
| 色/物理的外観 | シルバーホワイト | ||||||||||
| -660.323℃ | |||||||||||
| 沸点 | 2519℃ | ||||||||||
| 密度 | 2.70g/cm3 | ||||||||||
| 標準/常温における物理状態(固体/液体/気体) | Solid | ||||||||||
| 延性 | 有 | ||||||||||
| 成形性 | 有 | ||||||||||
| 硬度 | 2.9 Mohs | ||||||||||
| 電気伝導度 | 37.6676×106 Sm-1 | ||||||||||
| 熱伝導率 | 237 Wm-1K-1 | ||||||||||
| 比熱容量 | 0.90 Jg-1K-1 | ||||||||||
| 比重 | |||||||||||
| 抵抗率 | 2.65 x10-8ρ (Ω m) | ||||||||||
| 引張強さ | 90 Mpa | ||||||||||
| 温度係数 | 0.1 Kg | 0.00393 α/℃ | |||||||||
| 引張降伏強さ | 276 Mpa | ||||||||||
| 線膨張係数/熱伝導率 | |||||||||||
| 摩擦係数 | 1.1 10-6K-1 | ||||||||||
| 1.35 | |||||||||||
化学的性質 |
|||||||||||
| 燃焼性 | |||||||||||
| 酸化状態(番号) | 3 |
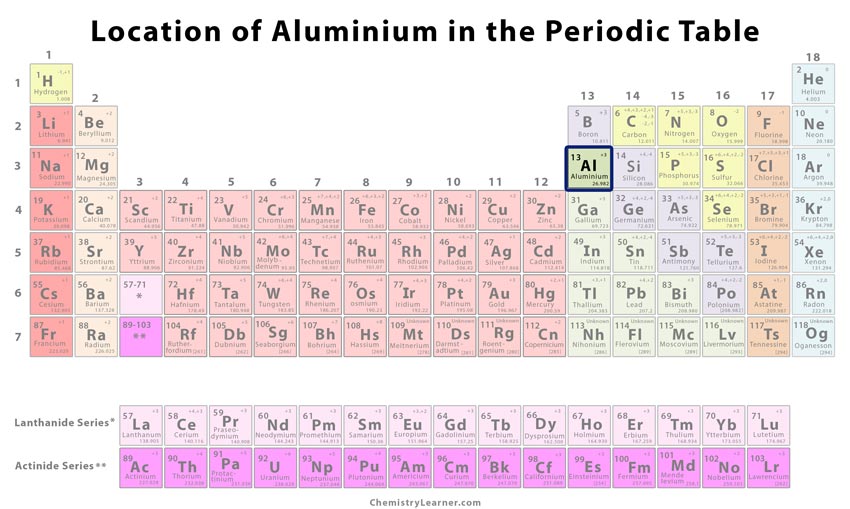
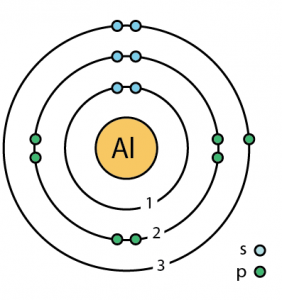
アルミニウムの原子データ
| 価電子 | 1 | 電子配置(希ガス配置) | 3s23p1 | |||||||||||
| 結晶構造 | Face-…センタード・キュービック | |||||||||||||
| 格子定数/パラメータ | 0.405 nm | |||||||||||||
| エネルギー準位 | ||||||||||||||
| 第一エネルギー準位 | 2 | |||||||||||||
| 第二エネルギー準位 | 2 | 8 | ||||||||||||
| 第3エネルギー準位 | 3 | |||||||||||||
| 原子構造 | ||||||||||||||
| – 電子数 | 13 | |||||||||||||
| – 中性子数 | 14 | |||||||||||||
| – (順不同 陽子の数 | 13 | |||||||||||||
| 原子の半径 | ||||||||||||||
| – 原子の半径 | 1.84 Å | |||||||||||||
| – 共有結合半径 | 1.24 Å | |||||||||||||
| 電子陰性度 | 1.0 Å | |||||||||||||
| – 電子陰性度 | 1.2 Å | – 共有結合半径 | ||||||||||||
| イオン電荷 | +1 | |||||||||||||
| イオン化エネルギー
(kJmol-) |
1.24Å | |||||||||||||
| イオン電荷 | +1.1) | 1st | 2nd | 3rd | 4th | 5th | 6th | 7th | ||||||
| 577.1 | 1th | 2rd | 3rd | 1st | 3rd | 4th | 1816.679 | 2744.781 | 11577.469 | 14841.857 | 18379.49 | 23326.3 | ||
アルミニウムは何に使われるか
- それは、フェンスのゲートパネルなどの製品の広い範囲で使用されています。 サイディング、缶、チューブ、パイプ、配線、ホイル、屋根、フライパン、手すり、コーティング、パティオカバー、ホイール、ろう付け棒、網戸、ラジエーター、ガス燃料タンク、電柱。
- 電気をよく通すので、コストと重量の点で、銅の代わりに送電線を作るのに理想的です。
- アルミニウムは、銅、マグネシウム、シリコン、マンガンなどの他の金属と合金化し、ボールベアリング、自動車部品、ロケット、飛行機を作ります。
- この金属は、光や熱から保護するために、望遠鏡の鏡、おもちゃ、パッケージ、装飾、化粧紙などに反射コーティングとしてよく使用されています。
- 高価な電池や液体燃料の代替として、アルミニウム燃料イオン空気電池/バッテリーは、より便利で携帯に便利です。

元素に毒性はあるか
アルミニウム含有塵やガスの吸入が呼吸システムに影響を与え、せきや他の肺関連障害を引き起こします。 また、経口摂取の場合、腎臓にダメージを与え、アルツハイマー病の可能性を高めると言われています。

興味深い事実
- ホール-ヘロルト法の発見以前、純粋なアルミニウムは金より高価だったため、「金属の王」と呼ばれました。

アルミニウム価格
純粋のコストは$ 0.9 と $ 1の間のどこかに異なる場合があります。
- http://www.rsc.org/periodic-table/element/13/aluminium
- https://education.jlab.org/itselemental/ele013.html
- https://pubchem.ncbi.nlm.nih.gov/compound/aluminum#section=Computed-Properties
- https://www.chemicool.com/elements/aluminum.html
- http://hyperphysics.phy-astr.gsu.edu/hbase/Tables/rstiv.html
- https://www.tedpella.com/company_html/hardness.htm
- http://asm.matweb.com/search/SpecificMaterial.asp?bassnum=ma6061t6
- https://study.com/academy/answer/how-many-valence-electrons-does-aluminum-have.html
- http://www.chemicalelements.com/elements/al.html
- https://www.sciencedirect.com/science/article/pii/S0378775307002236
- https://www.atsdr.cdc.gov/phs/phs.asp?id=1076&tid=34