US Pharm. 2012;37(6):26-29.
慢性腎臓病(CKD)は、糸球体濾過量(GFR)の低下とアルブミン尿の存在を伴う腎臓障害の持続と定義されています。 2009年、米国では57万人以上が腎臓病末期患者(ESRD)と分類され、そのうち約40万人が透析患者、約1万7000人が移植患者でした2。 CKDの発症率の増加は、人口の高齢化、高血圧(HTN)、糖尿病、肥満の増加に起因していると言われています。 CKDは、電解質の不均衡、ミネラルや骨の障害、貧血、脂質異常症、高血圧症などの多くの合併症と関連しています。 CKDは心血管疾患(CVD)の危険因子であり、GFRの低下とアルブミン尿は、心血管疾患および全死因死亡率の上昇と独立して関連していることがよく知られています3、4
高血圧はCKD(ステージ3~5)患者の85~95%に見られると報告されています5 高血圧とCKDの関係は周期的に生じると考えられています。 コントロールされていない高血圧はCKD発症の危険因子であり、CKDのより急速な進行と関連し、米国におけるESRDの第2位の原因となっています6,7。一方、進行性の腎疾患は、容積拡大と全身血管抵抗の増加によりコントロールされていない高血圧を悪化させることがあります。複数のガイドラインでは、腎疾患の進行を遅らせ、心血管疾患と死亡率を減らすために血圧を下げることの重要性が述べられています8~10。 しかし、適切な血圧コントロールを達成し維持するためには、ほとんどのCKD患者は降圧剤の組み合わせを必要とし、しばしば3つまたは4つの薬物クラスを採用する必要があります11。
病態生理
高血圧は、血圧上昇が腎臓の血管系に悪影響を及ぼすため、CKDの主要原因の1つです。長期にわたりコントロールされていない高血圧は、糸球体内圧を高くし、糸球体のろ過を損ないます12、13。 微量アルブミン尿は、尿中に少量のアルブミンが含まれる症状で、CKDの最初の兆候となることが多い。 タンパク尿(タンパク/クレアチニン比200mg/g以上)はCKDの進行とともに発症し、腎臓病およびCVDの予後不良と関連しています3、4、14
先に述べたように、CKDがHTNの原因となり、またはCKDとHTNは周期的に関係しあっています。 血圧の上昇は、腎臓内の血管だけでなく、全身の血管の損傷を引き起こします。 この損傷は、血液から水分と老廃物をろ過する腎臓の能力を損ない、血液中の水分量の増加、つまり血圧の上昇を引き起こします。
CKDの病期分類
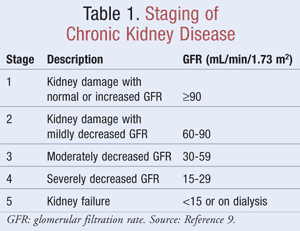
CKDの病期分類には、腎臓が老廃物をどれだけろ過できているかを臨床家が判断できる推定GFRが使用されています。 全米腎臓財団は、尿や血液中のマーカー、または画像診断によって特定される腎障害、GFRの変化の有無、または最低3ヵ月間のGFR <60 mL/min/1.73 m2のいずれかをCKDと定義している9。 表1は、K/DOQI(Kidney Disease Outcomes Quality Initiative)ガイドラインによる病期分類の基準を示している9
治療の目標
糖尿病以外のCKD患者および糖尿病患者は<130/80mmHgを目標血圧とするべきである8-10。最終的に、すべてのCKD患者の血圧を下げる根拠は、腎臓と心血管の両方の罹患率と死亡率を減らすことです。CKDと高血圧の患者における血圧制御の維持とタンパク尿の最小化は、腎臓病の進行とCVDの発症または悪化の予防に不可欠です8、9
最近の文献では、糖尿病および非糖尿病CKDにおける血圧目標は、タンパク尿の存在に基づいて個別に決める必要があるかもしれないと示唆されています。 いくつかの試験では、糖尿病および非糖尿病CKD患者において、<130/80mmHgの血圧目標を達成した場合、<140/90mmHgに血圧を下げた場合と比較して、心血管または腎臓の転帰の低下を示すことができなかった15、16しかし、タンパク尿を有する患者は、低い血圧目標を達成すると腎機能低下、腎不全または死亡を経験しにくくなる15、17。今後のガイドラインでは、蛋白尿のある患者にはより低い血圧の目標値である<130/80mmHgが含まれ、蛋白尿のない患者には<140/90mmHgの目標値が維持される可能性があります。
治療
ほとんどのCKDおよび高血圧患者には、血圧を下げるだけでなく、タンパク尿を減らす薬剤が第一選択薬として推奨される;データによると、タンパク尿が減少すると、心血管と腎の両方のアウトカムにおいて長期的に大きな利益がある可能性がある9。いくつかの種類の降圧剤は、CKDおよび高血圧の治療において役割を果たす可能性があります。 アンジオテンシン変換酵素(ACE)阻害薬やアンジオテンシン受容体遮断薬(ARB)など、レニン-アンジオテンシン-アルドステロン系(RAAS)を標的とする薬剤は、この患者集団に対する第一選択の高血圧治療と一般に考えられています8,9,18。 表2は、糖尿病の有無、タンパク尿の有無にかかわらず、CKD患者に推奨される降圧剤のガイダンスを示しています
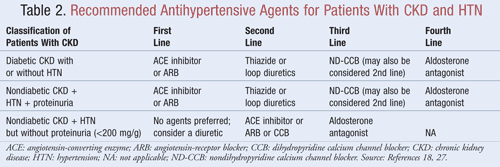
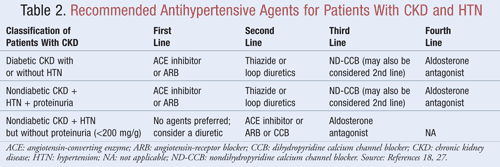
ACE Inhibitors or ARBs: レニン-アンジオテンシン系を標的とする降圧剤は、同じような血圧目標を達成した場合でも、他の薬剤よりも腎臓の機能低下を防ぐことが研究で示されている19。この結果は主にタンパク尿のある患者で見られ、一方、タンパク尿のない患者ではその効果はそれほど大きくはなかった。 これらの知見に基づき、ガイドラインでは、糖尿病患者や非糖尿病性腎疾患、高血圧、タンパク尿を有する患者に対する第一選択薬としてACE阻害薬またはARB療法を推奨しています。 最近のメタアナリシスでは、ACE阻害剤はARBよりも全死亡を10%減少させるため、高血圧治療において優れた効果を発揮することが示唆されています21。 したがって、副作用の可能性やコストなど、患者固有の要因によって、1つの薬剤を他の薬剤と区別して選択する必要があります。 ACE阻害剤とARBの併用は、腎機能を悪化させることが示されているため、推奨されません。 ACE阻害剤とARBの併用療法は、ACE阻害剤の単剤療法と比較して、心血管死亡率または罹患率を低下させませんでした20,21
ACE 阻害剤とARBは一般に忍容性が高いです。 ACE阻害剤は乾いた咳を引き起こすことがあり、残念ながら治療法の変更を余儀なくされることが多い。 ARBは乾いた咳とは無縁である。 血管浮腫は非常にまれであるが、ACE阻害剤またはARBの投与を開始した患者には、血管浮腫を呈する可能性のある徴候および症状について説明する必要がある。血管浮腫は起こりにくいことを患者に伝えるが、顔(しばしばまぶたを含む)および/または四肢に腫れを感じた場合は、治療を中止し、直ちに医師の診察を受けてほしい18
ティアジドとループ利尿剤の比較。 タンパク尿のない患者にとって、望ましい第一選択療法は明確に確立されておらず、サイアザイドなどの他の薬剤が検討されるかもしれない。 CKDと高血圧の患者は、しばしば体液貯留や体液過多を経験する。 その結果、利尿剤が治療レジメンに必要となることが多い。 チアジド系薬剤は、CKDステージ1~3(GFR≧30mL/min)の患者に推奨され、血圧およびCVDリスクの低減に有効な薬剤として確立されている22。ループ利尿薬は、GFRが著しく低下した患者の細胞外液量を減らすのに効果的であることが示されており、CKDステージ4または5(GFR<9225>30mL/min)の患者にも推奨されている18。 しかし、ループ利尿薬の心血管予後に対する長期的な効果は明確に確立されていない23
チアジド系利尿薬(クロルタリドン、ヒドロクロロチアジド)およびループ利尿薬(ブメタニド、フロセミド、トルセミド)はいずれも高尿症(尿量増加)の原因となる。 この水分損失の増加は、電解質の不均衡を引き起こす可能性があります。 これらの薬剤を使用している患者は、高カリウム血症や低マグネシウム血症などの電解質異常を経験しないように、電解質をモニターすることが重要です。 起立性低血圧は、あらゆる降圧剤に反応して起こる可能性がありますが、利尿剤でよく見られます。 利尿剤治療を開始する患者には、座った状態または横になった状態からゆっくり体を起こす必要性について、カウンセリングを行うことが重要である24,25
カルシウムチャンネル遮断薬 カルシウム拮抗薬(CCB)は、CKD患者の高血圧治療における第二選択薬または第三選択薬と考えられている。8,9非ヒドロピリジン系CCB(ND-CCB;例えば、ジルチアゼム、ベラパミル)とジヒドロピリジン系CCB(例えば, ND-CCBは、単独またはACE阻害薬やARBとの併用により、蛋白尿を有意に減少させることが示されている26。降圧作用に加えて、蛋白尿を減少させる可能性があるため、蛋白尿を有する糖尿病性CKDまたは非糖尿病性CKD患者のセカンドラインまたはサードラインの治療として考慮される必要がある。 ジヒドロピリジン系CCBは、蛋白尿のない非糖尿病性CKD患者の二次治療薬として使用することができる。 一般的な副作用は、ND-CCB(特にベラパミル)による浮腫と便秘、ジヒドロピリジン系薬剤による潮紅と末梢浮腫である18
アルドステロン拮抗薬。 アルドステロン拮抗薬:アルドステロンはCKDの進行に深刻な悪影響を及ぼす。 アルドステロン受容体拮抗薬(例、スピロノラクトン、エプレレノン)は、第一選択薬および第二選択薬で血圧目標が達成されない場合、CKD治療の役割を果たす可能性がある。 これらの薬剤は、ACE阻害剤またはARBに追加した場合、蛋白尿の減少をもたらすことがヒト試験で示されている27,28
アルドステロン拮抗薬はカリウムを節約する利尿薬であり、特にACE阻害剤またはARBと併用すると高カリウム血症のリスクを増加させる。 高カリウム血症のリスクを高めるため、カリウムを節約する利尿剤を使用する患者には、電解質異常がないことを確認するために、カリウム値をチェックすることが重要です。 高カリウム血症の症状には、不整脈や重度の筋力低下が含まれます。残念ながら、高カリウム血症は無症状で現れることがあるため、モニタリングの重要性がますます高まっています18、27
レニン阻害剤 レニン阻害剤:アリスキレンは、現在市販されている唯一のレニン阻害剤である。 高血圧症治療薬として、単剤またはバルサルタンとの併用療法が適応となる。 ALTITUDE試験の最近のデータから、糖尿病または腎障害(GFR <60 mL/min)のある患者では、腎障害、低血圧、高カリウム血症のリスクが高まるため、ACE阻害薬またはARBとの併用は禁忌とされた。29 アリスキレンは、患者がACE阻害薬またはARBを服用できない場合に検討することができるが、ステージ4または5の腎不全患者ではその使用を推奨できない30
β-blockers: β遮断薬は表2に含まれていないが、冠動脈疾患や慢性心不全など、β遮断薬のやむを得ない適応がある場合は、第2、第3選択薬として検討できる18
非薬物療法の推奨
クロノセラピー: このタイプの治療は、概日リズムを考慮し、1日のパターンに合わせて降圧剤を投与し、すべての降圧剤を午前中に投与することから脱却するものである。 31,32 また、ACE阻害薬やARBなどの他の降圧薬の夜間投与が有効であることを示す研究もあります。 2種類以上の降圧剤を使用している場合は、2種類の降圧剤を朝に投与し、追加の降圧剤を夕方に投与することが適切な場合があります。 8生活習慣の改善は、患者が血圧目標を達成するために薬物を必要とするかどうかにかかわらず、高血圧治療の重要な要素であることに変わりはない。 高血圧を止めるための食事療法(DASH)」は、果物と野菜の消費量を増やし、低脂肪乳製品と低脂肪タンパク質を取り入れ、飽和脂肪を制限することを強調しています。この食事計画は、降圧剤の単独療法で得られる低下とほぼ同等の収縮期血圧を著しく低下させることが示されています35 。毎日の活動量を増やしながら、これらの健康的な食事習慣を開始することは、降圧療法から得られる利益を増大させ、BP目標の達成に不可欠な役割を果たすことができる」
まとめ
CKDとHTNの相互関係から、BPコントロールとタンパク尿がある場合はそれを減らすことの重要性がさらに重視されるようになった。 一般に、血圧に加えてタンパク尿を減少させる薬剤が第一選択薬となるが、患者は目標を達成し、CVDおよびESRDのリスクを最小限に抑えるために、しばしば3~4種類の降圧剤を必要とする。 さらに、健康的なライフスタイルの見直しは、降圧療法に不可欠な要素として常に考慮されるべきです。 Coresh J, Selvin E, Stevens LA, et al.米国における慢性腎臓病の有病率. JAMA. 2007;298:2038-2047.
2. Collins AJ, Foley RN, Chavers B, et al. U.S. renal data system 2011 annual data report.米国腎臓データシステム2011年年次データ報告書。 Am J Kidney Dis. 2012;59(suppl 1):evii.
3. Matsushita K, van der Velde M, Astor BC, et al.Association of estimated glomerular filtration rate and albuminuria withall-cause and cardiovascular mortality in general population cohorts: acollaborative meta-analysis.The Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts.All rights reserved. Lancet. 2010;375:2073-2081.
4. Rashidi A, Sehgal AR, Rahman M, O’Connor AS.(ラシディ A、セガール AR、ラーマン M、オコナー AS)。 65歳以上の患者において、慢性腎臓病、糖尿病、心筋梗塞が心血管系死亡のリスク因子として同等であることの事例。 Am J Cardiol. 2008;102:1668-1673.
5. Rao MV, Qiu Y, Wang C, Bakris G. Hypertension and CKD:Kidney Early Evaluation Program (KEEP) and National Health and NutritionExamination Survey (NHANES), 1999-2004(高血圧と慢性腎臓病:腎臓早期評価プログラムおよび全国健康栄養調査(NHANES))。 を参照。 2008;51(suppl 2):S30-S37.
6. Botdorf J, Chaudhary K, Whaley-Connell A. Hypertension in cardiovascular and kidney disease.高血圧と腎臓病の関係. Cardiorenal Med. 2011;1:183-192.
7. Segura J, Ruilope L. Hypertension in moderate-to-severe nondiabetic CKD patients. Adv Chronic Kidney Dis. 2011;18:23-27.
8. Chobanian AV, Bakris GL, Black HR, et al. The seventhreport of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 report(高血圧の予防、検出、評価、治療に関する全米合同委員会の第7次報告書). JAMA。 2003;289:2560-2572.
9. 全米腎臓財団。 このような状況下で、「慢性腎臓病に対する K/DOQI 臨床実践ガイドライン:評価、分類、および層別化」。 Am J Kidney Dis。 2002;39(suppl 1):S1-S266.
10. 米国糖尿病協会。 糖尿病における診療の基準-2012 年。 Diabetes Care. 2012;35(suppl 1):S1-S63.
11. Bakris GL, Williams M, Dworkin L, et al. Preservingrenal function in adults with hypertension and diabetes: a consensusapproach(高血圧と糖尿病の成人患者における腎機能の維持:コンセンサスアプローチ). 全米腎臓財団高血圧・糖尿病執行委員会作業部会。 Am J Kidney Dis. 2000;36:646-661.
12. Am J Kidney Dis. 1999;33:1004-1010.
13. 吉岡敏明、Rennke HG、Salant DJ、他:糸球体毛細血管壁の順選択性障害における通常より高い透過圧の役割:初期受動性Heymann腎炎での研究。 1987:61:531-538.
14.Circ研究。 このような場合、「腎臓病は心血管系疾患発症の危険因子である」とする米国心臓協会評議会からの声明が発表された。 Circulation. 2003;108:2154-2169.
15. アンインターンメド。 2011;154:541-548.
16. Cushman C, Evan GW Byington RP, et al.ACCORD研究グループ。 2型糖尿病における血圧の集中的なコントロール。 N Engl J Med。 2010;363:1575-1585.
17. 2型糖尿病と腎症におけるロサルタンの腎臓と心血管系の転帰に対する効果。 N Engl J Med. 2001;345:861-869.
18. 腎臓病アウトカム品質イニシアチブ(K/DOQI).K/DOQI臨床実践ガイドライン慢性腎臓病における高血圧と降圧剤について. Am J Kidney Dis. 2004;43(suppl 1):S1-S290.
19. 腎臓病の転帰を予測するタンパク尿:非糖尿病性腎症(REIN). Kidney Int Suppl. 2004;66:S90-S96.
20. Sharma P, Blackburn RC, Parke CL, et al.Angiotensin-converting enzyme inhibitors and angiotensin receptorblockers for adults with early (stage 1 to 3) nondiabetic chronickidney disease.アンジオテンシン変換酵素阻害薬とアンジオテンシン受容体遮断薬による早期糖尿病性慢性腎臓病の治療。 Cochrane Database Syst Rev. 2011;(10):CD007751.
21. van Vark LC, Bertrand M, Akkerhuis KM, et al.Angiotensin-converting enzyme inhibitors reduce mortality inhypertension: a meta-analysis of randomized clinical trials ofrenin-angiotensin-aldosterone system inhibitors involving 158,998 patients.高血圧症の患者においてアンジオテンシン変換酵素阻害薬が死亡率を減少させた。 Eur Heart J. 2012 Apr 17; Epub ahead of print.
22. アンジオテンシン変換酵素阻害薬またはカルシウム拮抗薬と利尿薬に無作為に割り付けられた高リスク高血圧患者における主要転帰:抗高血圧および脂質低下治療による心臓発作予防試験(ALLHAT).2012.4.17. JAMA. 2002;288:2981-2997.
23. ムシーニVM、ライトJM、バセットK、ジャウカCD. 一次性高血圧に対するループ利尿薬の血圧低下効果。 Cochrane Database Syst Rev. 2009;(4):CD003825.
24. マイクロジド(ヒドロクロロチアジド経口カプセル)添付文書. Watson Pharma, Inc: Morristown, NJ; 2011.
25. クロルタリドン経口錠の添付文書。 マイラン・ファーマシューティカルズ,Inc. マイラン・ファーマシューティカルズ社:ウィスコンシン州モーガンタウン;2006.
26. このような状況下、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」を行うこととした。 腎臓学会誌2004;65:1991-2002.
27. このような状況下において、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」の一環として、「震災復興に向けた取り組み」を行うこととした。 臨床 J Am Soc Nephrol。 2009;4:542-551.
28. 糖尿病性腎症における最大限のアンジオテンシン変換酵素阻害に、アンジオテンシン受容体遮断またはミネラルコルチコイド拮抗を追加すること。 J Am Soc Nephrol. 2009;20:2641-2650.
29. アリスキレン含有薬:医薬品安全性情報-新しい警告と禁忌。 MedWatch.April 20, 2012.www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm301120.htm?source=govdelivery;4/20/2012.Accessed May 1, 2012.
30.アリスキレン含有薬:医薬品安全性情報-新しい警告と禁忌。 Trimarchi H. 血圧コントロールと腎保護におけるアリスキレンの役割。 Int J Nephrol Renovasc Dis. 2011;4:41-48.
31. Portaluppi F, Vergnani L, Manfredini R, et al.夜間高血圧inchronic腎不全に対するイズラジピンの時間依存的効果。 Am J Hypertens. 1995;8:719-726.
32. 2007;24:471-493.
33.Chronobiol Int. Hermida RC, Ayala DE. 本態性高血圧症におけるアンジオテンシン変換酵素阻害薬ラミプリルによる時間療法:就寝時投与による血圧コントロールの改善。 高血圧。 2009;54:40-46.
34. 高血圧患者におけるバルサルタンの外来血圧に対する投与時間依存的な影響。 Hypertension. 2003;42:283-290.
35. Sacks FM, Svetkey LP, Vollmer WM, et al. Effects onblood pressure of reduced dietary sodium and the Dietary Approaches toStop Hypertension (DASH) diet.高血圧症に対する食事療法とナトリウムの減少の効果. DASH-ナトリウム共同研究グループ.N Engl J Med. 2001;344:3-10.