本製品の販売承認に関連する情報を簡単に説明します。 本製品、その適応症、FDAの承認の根拠に関するより詳細な情報については、以下の安全性・有効性データの概要(SSED)および製品の添付文書へのリンクをご覧ください。 Axonics Sacral Neuromodulation System
PMA 出願人: Axonics Modulation Technologies, Inc.
住所: 26 Technology Drive, Irvine, CA 92618
Approval Date: 2019年11月13日
Approval Letter: Approval Order
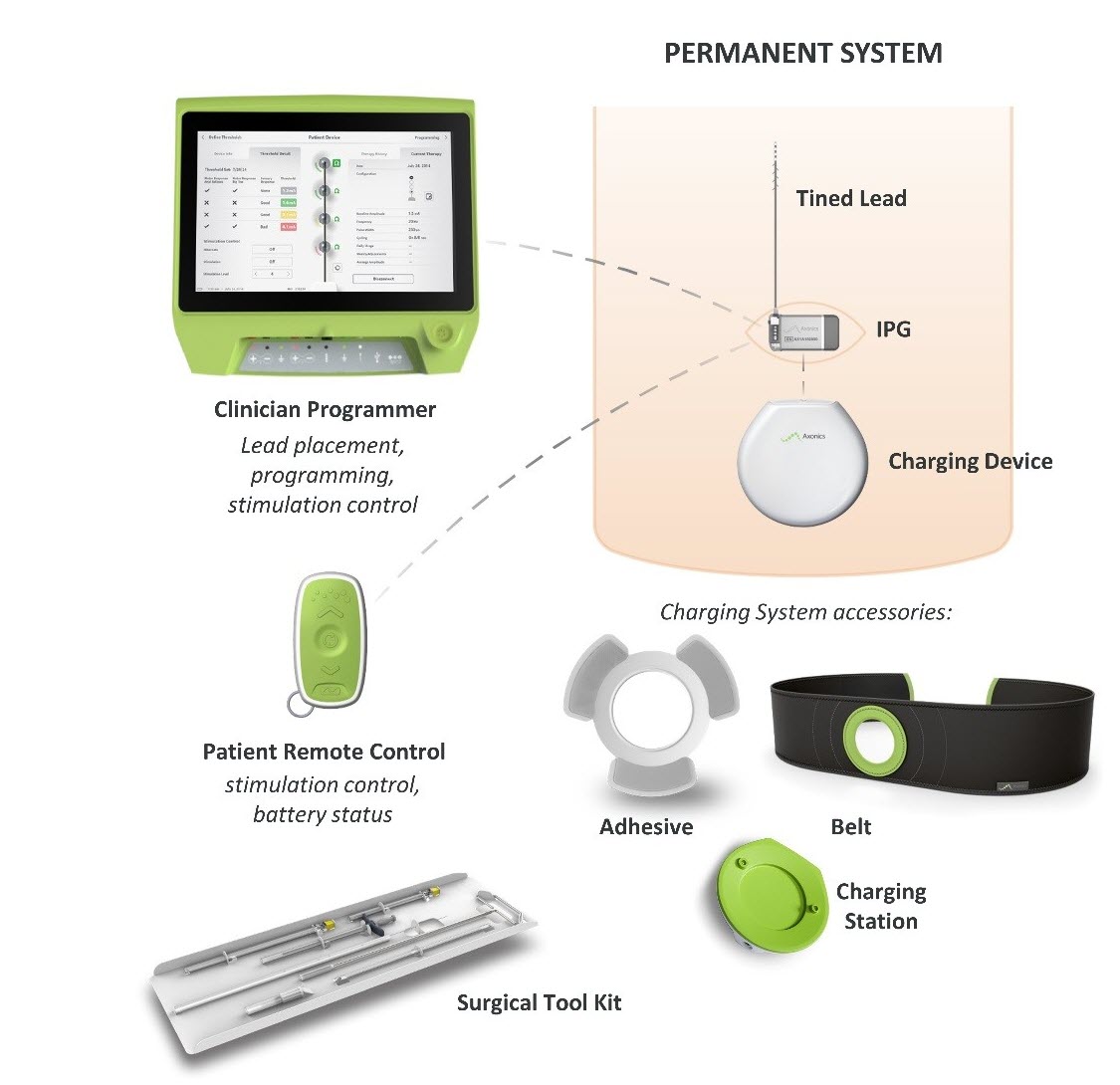
What is it? Axonics Sacral Neuromodulation (SNM) Systemは、尿閉および過活動膀胱の症状の治療を目的とした仙骨神経刺激(SNS)システムである。 植え込み型刺激装置を使用し、リード線を介して仙骨神経近傍の電極に電気パルスを送ります
どのように機能しますか? 植込み型パルスジェネレーター(IPG)を臀部上部の皮下に手術で設置し、骨盤の腰骨の間を通って仙骨神経に至るリード線に取り付けます。 IPGは、リード線を通して脊髄から膀胱に伝わる仙骨神経に電気パルスを送り、排尿コントロールを改善します
どのような時に使用するのですか? 排尿コントロールのためのアクソニックスSNMシステムは、生活習慣の改善、骨盤底筋運動、投薬などの他の治療法に失敗した、あるいは耐えられなかった患者さんの尿閉および過活動膀胱の症状の治療に使用されます。 尿閉および過活動膀胱を治療せずに放置すると、患者さんの生活の質を低下させ、日常生活動作の維持に大きな困難をもたらす可能性があります
どのような効果が期待できますか? アクソニックスSNMシステムの臨床試験の結果と、同様のSNMデバイスについて利用可能な文献の系統的レビューからまとめられた追加の臨床データから、他の治療法が無効または耐えられなかった尿閉および過活動膀胱の症状を持つほとんどの患者さんに有益であることが示されました。 切迫性尿失禁患者を対象としたアクソニックスの臨床試験では、SNMシステムを植え込んだ患者の90%(116/129)が、植え込んでいない患者と比較して6ヶ月後の切迫性尿漏れの回数を少なくとも50%減少させることに成功しました。 より長期の研究(van Kerrebroeck, 2007)では、同様のSNM装置を植え込まれた152人の患者を5年間追跡調査した。 5年後、切迫性尿失禁患者の58%(56/96人)が少なくとも50%の改善(1日の漏れの数で測定)を示しています。 さらに5年後、緊急頻尿の患者様の40%(10/25)が50%以上改善し(1日あたりの排泄回数で測定)、尿閉の患者様の58%(18/31)が50%以上改善しました(1日あたりのカテーテル挿入数で測定)。 デザイン、技術、性能、適応症、出力特性、治療対象となる患者層が類似していることから、FDAは、Axonics SNMシステムが、公表された研究で評価された市販のSNMシステムと同様の性能を有すると考えています
どんな場合に使用してはいけないのですか?
- 試験刺激に対して適切な反応を示さない患者、または
- Axonics SNM Systemを操作できない患者
その他の情報(警告、注意、有害事象など)については、Axonics SNM Systemを使用しないで下さい。
- 安全性および有効性データの概要
- 患者への表示
- 医師への表示
- PMAデータベースへの登録