Sublimação é o processo em que um material muda de um sólido congelado para um gás sem passar pelo estado líquido intermediário.
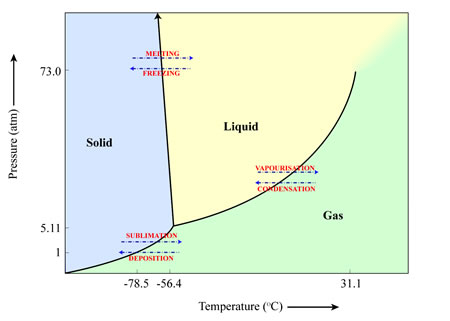
Se um material irá sublimar (sólido para gás), fundir (sólido para líquido) ou vaporizar (líquido para gás) depende da temperatura e pressão do ambiente em que se encontra. Isto pode ser ilustrado num ‘diagrama de fases’, como o que se segue para a água. Neste caso, e com as pressões (1 atmosfera) e temperaturas (25 graus Celsius) a que estamos habituados na Terra, o gelo da água derreterá para formar água líquida, que depois se vaporizará para formar vapor de água. Entretanto, se as pressões forem suficientemente baixas (por exemplo, as pressões que encontramos em outro lugar no Sistema Solar), o gelo de água se transformará diretamente em vapor de água conforme a temperatura aumenta, contornando o estágio de água líquida.
Sublimação ocorre em muitos lugares no Sistema Solar. Dois exemplos são:
- A sublimação da água dos núcleos cometários à medida que o cometa se aproxima do Sol’
- A sublimação das calotas polares de gelo em Marte durante o Verão Marciano.
Um exemplo de material que sublima aqui na Terra é o dióxido de carbono congelado (CO2) – mais comumente conhecido como ‘gelo seco’. Quando exposto ao ar à temperatura ambiente a pressões de 1 atmosfera, o CO2 congelado transforma-se directamente em CO2 gasoso.