Este es un breve resumen de la información relacionada con la aprobación de la FDA para comercializar este producto. Consulte los enlaces siguientes al Resumen de Datos de Seguridad y Eficacia (SSED) y al etiquetado del producto para obtener información más completa sobre este producto, sus indicaciones de uso y la base de la aprobación de la FDA.
Nombre del producto: Sistema de Neuromodulación Sacra de Axonics
Solicitante de la PMA: Axonics Modulation Technologies, Inc.
Dirección: 26 Technology Drive, Irvine, CA 92618
Fecha de aprobación: 13 de noviembre de 2019
Carta de aprobación: Orden de aprobación
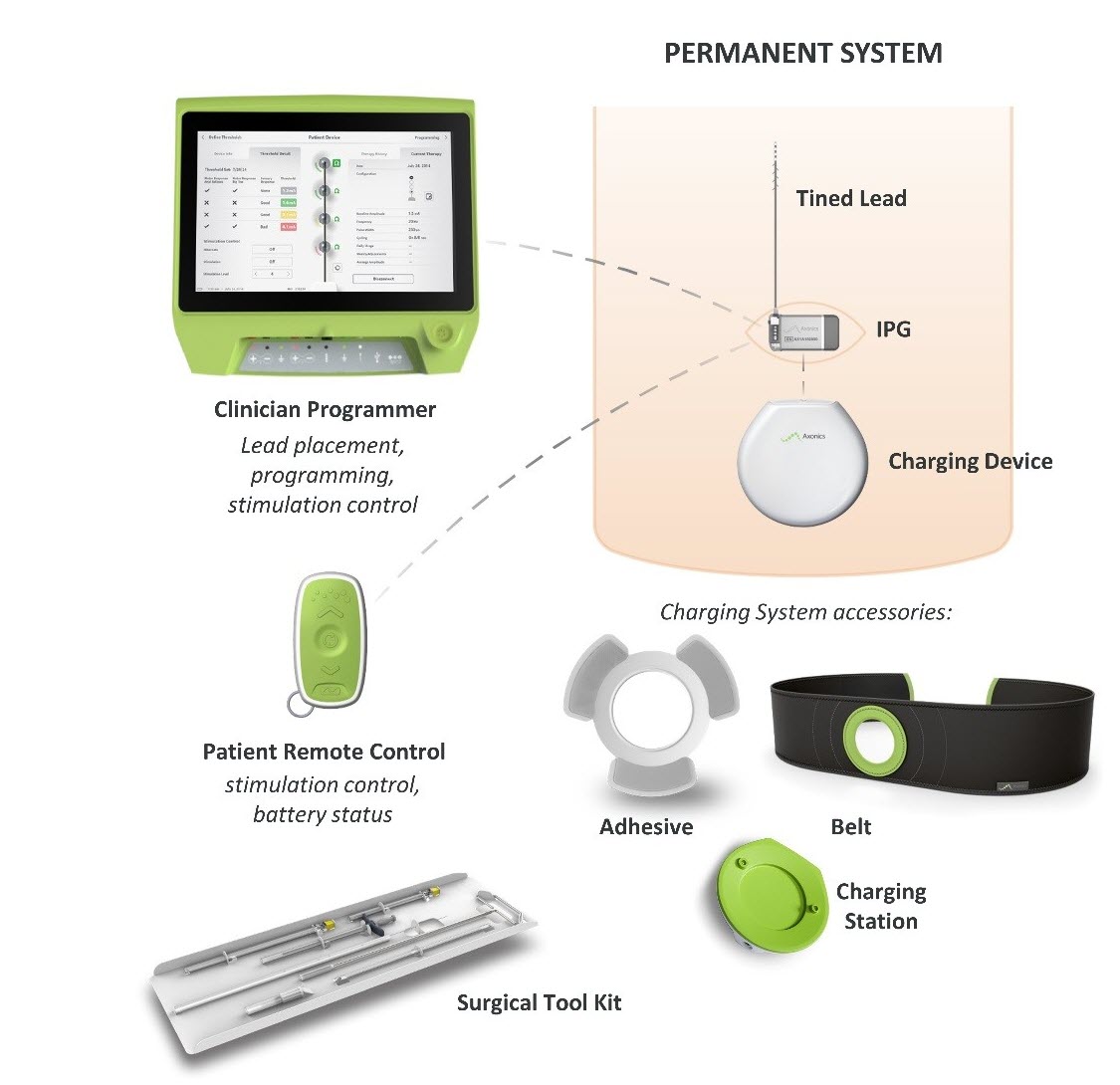
¿Qué es? El sistema de neuromodulación sacra (SNM) de Axonics es un sistema de estimulación del nervio sacro (SNS) que está destinado a tratar la retención urinaria y los síntomas de la vejiga hiperactiva. Utiliza un estimulador implantado para enviar pulsos eléctricos a través de un cable conductor a los electrodos situados cerca del nervio sacro.
¿Cómo funciona? Un generador de impulsos implantable (IPG) se coloca quirúrgicamente bajo la piel en la zona superior de las nalgas y se conecta a un cable conductor que pasa entre los huesos de la cadera de la pelvis y termina en el nervio sacro. El IPG envía impulsos eléctricos a través del cable conductor al nervio sacro que viaja desde la médula espinal hasta la vejiga para ayudar a mejorar el control urinario.
¿Cuándo se utiliza? El sistema SNM de Axonics para el control urinario se utiliza para el tratamiento de la retención urinaria y los síntomas de la vejiga hiperactiva en pacientes que han fracasado o no han podido tolerar otros tratamientos, como los cambios en el estilo de vida, los ejercicios del suelo pélvico o la medicación. Si no se trata, la retención urinaria y la vejiga hiperactiva pueden reducir la calidad de vida del paciente y provocar dificultades importantes para mantener las actividades de la vida diaria.
¿Qué se consigue? Los resultados de un estudio clínico del sistema SNM de Axonics, combinados con datos clínicos adicionales recopilados a partir de una revisión sistemática de la literatura disponible para un dispositivo SNM similar, muestran que existe un beneficio para la mayoría de los pacientes con retención urinaria y los síntomas de la vejiga hiperactiva que han fracasado o no han podido tolerar otros tratamientos. En el estudio clínico de Axonics sobre pacientes con incontinencia urinaria de urgencia, el 90% (116/129) de los pacientes con el sistema SNM implantado lograron una reducción de al menos el 50% en el número de fugas de urgencia a los 6 meses en comparación con el número de fugas de urgencia sin el sistema SNM. En un estudio a más largo plazo (van Kerrebroeck, 2007), 152 pacientes implantados con un dispositivo SNM similar fueron seguidos durante 5 años. A los 5 años, el 58% (56/96) de los pacientes con incontinencia urinaria de urgencia presentaban una mejora de al menos el 50% (medida en términos de número de fugas diarias). Además, al cabo de 5 años, el 40% (10/25) de los pacientes con urgencia-frecuencia habían mejorado al menos un 50% (medido en términos de número de vaciados al día), y el 58% (18/31) de los pacientes con retención urinaria habían mejorado al menos un 50% (medido en términos de número de sondajes al día). Dadas las similitudes en el diseño, la tecnología, el rendimiento, las indicaciones de uso, las características de salida y la población de pacientes que debe tratar, la FDA cree que el sistema SNM de Axonics tendrá un rendimiento similar al sistema SNM disponible en el mercado evaluado en los estudios publicados.
¿Cuándo no debe utilizarse? El sistema SNM de Axonics no debe utilizarse en:
- Pacientes que no hayan demostrado una respuesta adecuada a la estimulación de la prueba; o
- Pacientes que no puedan manejar el sistema SNM de Axonics
Información adicional (incluyendo advertencias, precauciones y efectos adversos):
- Resumen de los datos de seguridad y eficacia
- Etiquetado del paciente
- Etiquetado del médico
- Ingreso en la base de datos de la PMA