US Pharm. 2012;37(6):26-29.
Chronisk nyresygdom (CKD) defineres som vedvarende nyreskade ledsaget af en reduktion i den glomerulære filtrationsrate (GFR) og tilstedeværelsen af albuminuri. Prævalensen af CKD er steget støt i løbet af de sidste to årtier og blev rapporteret til at påvirke over 13 % af den amerikanske befolkning i 2004.1 I 2009 blev mere end 570.000 mennesker i USA klassificeret som havende endestadiet af nyresygdom (ESRD), herunder næsten 400.000 dialysepatienter og over 17.000 transplantationsmodtagere.2 Det fastslås, at en patient har ESRD, når han eller hun har brug for substitutionsbehandling, herunder dialyse eller nyretransplantation. Stigningen i forekomsten af CKD kan tilskrives en aldrende befolkning og en stigning i forhøjet blodtryk (HTN), diabetes og fedme i den amerikanske befolkning. CKD er forbundet med en lang række komplikationer, herunder elektrolytforstyrrelser, mineral- og knoglelidelser, anæmi, dyslipidæmi og forhøjet blodtryk. Det er velkendt, at CKD er en risikofaktor for kardiovaskulær sygdom (CVD), og at et nedsatGFR og albuminuri uafhængigt af hinanden er forbundet med en stigning i den kardiovaskulære dødelighed og dødeligheden af alle årsager.3,4
HTN er blevet rapporteret at forekomme hos 85 % til 95 % af patienter med CKD (stadie 3-5).5 Forholdet mellem HTN og CKD er af cyklisk karakter. Ukontrolleret HTN er en risikofaktor for udvikling af CKD, er forbundet med en hurtigere progression af CKD og er den næstførste årsag til ESRD i USA.6,7 Samtidig kan progressiv nyresygdom forværre ukontrolleret HTN på grund af volumenudvidelse og øget systemisk vaskulær modstand.Flere retningslinjer diskuterer vigtigheden af at sænke blodtrykket (BP) for at bremse progressionen af nyresygdom og reducere kardiovaskulærmorbiditet og dødelighed.8-10 For at opnå og opretholde en tilstrækkelig blodtrykskontrol kræver de fleste patienter med CKD imidlertid kombinationer af antihypertensive midler; ofte kan det være nødvendigt at anvende op til tre eller fire medicingrupper.11
Patofysiologi
Hypertension er en af de vigtigste årsager til CKD på grund af de skadelige virkninger, som et forhøjet BP har på nyrernes vaskulatur.Langvarigt, ukontrolleret, højt BP fører til et højt intraglomerulært tryk, hvilket forringer den glomerulære filtration.12,13 Skader på glomeruli fører til en forøgelse af proteinfiltreringen, hvilket resulterer i en abnormt forøget mængde protein i urinen (mikroalbuminuri eller proteinuri).12,13 Mikroalbuminuri er præsentationen af små mængder albumin i urinen og er ofte det første tegn påCKD. Proteinuri (protein/kreatinin-forhold ≥200 mg/g) udvikles, efterhånden som CKD skrider frem, og er forbundet med en dårlig prognose for både nyresygdom og CVD.3,4,14
Som tidligere omtalt er forholdet mellem CKD ogHTN cyklisk, da CKD kan bidrage til eller forårsage HTN. Forhøjet blodtryk fører til skader på blodkarrene i nyrerne og i hele kroppen. Denne skade forringer nyrernes evne til at filtrere væske og affaldsstoffer fra blodet, hvilket fører til en forøgelse af væskemængden i blodet – og dermed til en stigning i blodtrykket.
Staging af CKD
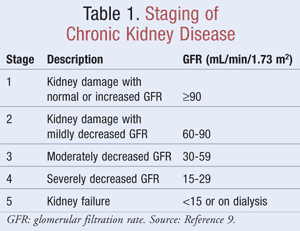
Den estimerede GFR, som hjælper klinikere med at afgøre, hvor godt nyrerne filtrerer affaldsstoffer, anvendes i stadieinddelingen af CKD. National Kidney Foundation definerer CKD som enten nyreskade, identificeret ved markører i urin eller blod eller ved billeddannelse, med eller uden ændringer i GFR, eller en GFR <60 mL/min/1,73 m2 i mindst 3 måneder9 . TABEL 1 viser stadieinddelingskriterierne som fastsat i retningslinjerne for Kidney Disease Outcomes Quality Initiative (K/DOQI).9
Terapimål
Patienter med ikke-diabetisk og diabetisk CKD bør have et mål for blodtrykket på <130/80 mmHg.8-10I sidste ende er begrundelsen for at sænke BP hos alle patienter med CKD at reducere både renal og kardiovaskulær morbiditet og mortalitet.Det er vigtigt at opretholde BP-kontrol og minimere proteinuri hos patienter med CKD og HTN for at forebygge progression af nyresygdom og udvikling eller forværring af CVD.8,9
Den seneste litteratur tyder på, at BP-målene for diabetisk og ikke-diabetisk CKD muligvis skal individualiseres på baggrund af tilstedeværelsen af proteinuri. Nogle forsøg har ikke vist en reduktion i kardiovaskulære eller nyreudfald hos diabetiske og ikke-diabetiske patienter med CKD, når der opnås et BP-mål på <130/80 mmHg sammenlignet med en sænkning af BP til <140/90 mmHg.15,16 Patienter med proteinuri er dog mindre tilbøjelige til at opleve en forringelse af nyrefunktionen, nyresvigt eller død, når det lavere BP-mål opnås.15,17Det er sandsynligt, at fremtidige retningslinjer kan omfatte et lavere BP-mål,<130/80 mmHg, for patienter med proteinuri, men fastholde et mål på<140/90 mmHg for patienter uden proteinuri.
Behandling
Midler, der ikke blot sænker blodtrykket, men også reducerer proteinuri, anbefales som førstevalgsterapi til de fleste patienter med CKD ogHTN; data tyder på, at der kan være betydelige fordele på lang sigt med hensyn til både kardiovaskulære og renale resultater, når proteinuri mindskes.9Flere klasser af antihypertensive midler kan have en rolle i behandlingen af CKD og HTN. Midler, der er rettet mod therenin-angiotensin-aldosteron-systemet (RAAS), såsom angiotensin-konverterende enzym (ACE-hæmmere) eller angiotensinreceptorblokkere (ARB’er), betragtes generelt som førstevalg af antihypertensiv behandling for denne patientpopulation.8,9,18 TABEL 2 giver vejledning om anbefalede antihypertensive midler til patienter med CKD med eller uden diabetes og med eller uden proteinuri.
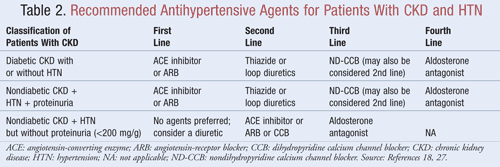
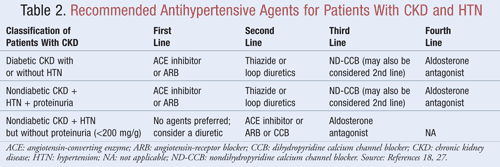
ACE-hæmmere eller ARB’er: Undersøgelser har vist, at antihypertensive midler, der er rettet mod renin-angiotensinsystemet, i højere grad end andre midler forebygger forringelse af nyrerne, selv når de opnår samme blodtryksmål.19 Disse resultater blev primært fundet hos patienter med proteinuri, mens fordelen var mindre væsentlig for patienter uden proteinuri. På baggrund af disse resultater anbefaler retningslinjerneACE-hæmmer- eller ARB-behandling som førstevalgsbehandling til personer med diabetes eller personer med ikke-diabetisk nyresygdom, HTN og proteinuri. Data tyder på, at ACE-hæmmere og ARB’er er lige effektive til at sænke blodtrykket og reducere proteinuri.20 En nyere metaanalyse tyder på, at ACE-hæmmerbehandling kan give større fordele end ARB-behandling til behandling af HTN på grund af en 10 % reduktion i dødeligheden af alle årsager.21 Disse resultater blev fastlagt for patienter med HTN og gjaldt ikke for patienter med yderligere komorbiditeter såsom CKD. Derfor vil valget af et middel frem for et andet afhænge af patientspecifikke faktorer som f.eks. potentielle bivirkninger og omkostninger. Behandling med både en ACE-hæmmer og en ARB anbefales ikke, da denne kombination har vist sig at forværre nyrefunktionen. Kombinationsbehandling med ACE-hæmmere og ARB’er reducerede ikke den kardiovaskulære mortalitet eller morbiditet i forhold til monoterapi med en ACE-hæmmer.20,21
ACE-hæmmere og ARB’er tolereres generelt godt. ACE-hæmmere kan forårsage tør hoste, hvilket desværre ofte kræver en ændring i behandlingen. ARB’er er ikke forbundet med tør hoste. Angioødem er meget sjældent; men patienter, der påbegyndes med ACE-hæmmere eller ARB’er, bør informeres om de tegn og symptomer, der kan vise sig med angioødem.Informer patienterne om, at angioødem er usandsynligt, men hvis de oplever hævelse i ansigtet (ofte inklusive øjenlåg) og/eller ekstremiteter, bør de afbryde behandlingen og straks søge læge.18
Thiazid vs. loopdiuretika: For patienter uden proteinuri er det ikke klart fastlagt, hvilken behandling der er den foretrukne som førstevalg, og andre midler, f.eks. et thiazid, kan overvejes. Patienter med CKD og HTN oplever ofte væskeretention eller væskeoverbelastning. Som følge heraf er det ofte nødvendigt med diuretika i deres behandlingsregime. Thiazider anbefales til patienter med CKD-stadie 1 til 3 (GFR ≥30 mL/min) og er blevet etableret som effektive midler til reduktion af blodtryk og CVD-risiko.22 Loop-diuretika anbefales til patienter med CKD-stadie 4 eller 5 (GFR <30 mL/min), da de har vist sig at være mere effektive til at reducere ekstracellulært væskevolumen hos patienter med stærkt reduceret GFR.18 Langtidseffekten af loopdiuretika på kardiovaskulære resultater er imidlertid ikke klart fastlagt.23
Thiaziddiuretika (chlorthalidon, hydrochlorthiazid)og loopdiuretika (bumetanid, furosemid, torsemid) forårsager allehyperurikæmi (øget vandladning). Denne stigning i væsketab kan føre til elektrolytubalance. Det er vigtigt, at patienter på disse midler får deres elektrolytter overvåget for at sikre, at de ikke oplever elektrolytforstyrrelser som f.eks. hyperkaliæmi eller hypomagnesiæmi. Orthostatisk hypotension kan forekomme som reaktion på alle antihypertensive midler; det er dog almindeligt med diuretika. Det er vigtigt at rådgive patienter, der påbegynder diuretikabehandling, om behovet for at rejse sig langsomt fra en siddende eller liggende stilling.24,25
Kalciumkanalblokkere: Kalciumkanalblokkere (CCB’er) betragtes som anden- eller tredjelinjebehandling til behandling af HTN hos patienter med CKD.8,9Mens der muligvis ikke er nogen forskel i virkningen på BP-sænkning mellemdennondihydropyridin CCB’er (ND-CCB’er; f.eks. diltiazem, verapamil) ogdihydropyridin CCB’er (f.eks, amlodipin, nifedipin) har ND-CCB’er vist sig at kunne reducere proteinuri betydeligt, enten når de anvendes alene eller i kombination med en ACE-hæmmer eller en ARB.26 På grund af deres potentiale til at reducere proteinuri, ud over deres antihypertensive virkninger, bør ND-CCB’er overvejes som anden- eller tredjelinjebehandling hos patienter med diabetisk CKD eller ikke-diabetisk CKD med proteinuri. Dihydropyridin-CCB’er kan anvendes som andenbehandlingsmidler hos patienter med ikke-diabetisk CKD uden proteinuri. Almindelige bivirkninger omfatter ødem og forstoppelse med ND-CCB’er (især verapamil) og rødme og perifere ødemer med dihydropyridinagenser.18
Aldosteronantagonister: Aldosteron spiller en alvorligt skadelig rolle i udviklingen af CKD. Aldosteronreceptorantagonister (f.eks. spironolacton, eplerenon) kan have en plads i CKD-behandlingen, når BP-målene ikke er blevet nået med første- og andenlinjebehandling. Disse midler har i humantrials vist sig at give en reduktion af proteinuri, når de tilsættes til en ACE-hæmmer eller ARB.27,28
Aldosteronantagonister er kaliumsparende diuretika, som øger risikoen for hyperkaliæmi, især hvis de tages sammen med en ACE-hæmmer eller ARB. Det er vigtigt, at patienter, der indledes med kaliumsparende diuretika, får kontrolleret deres kaliumniveau for at sikre, at de ikke får elektrolytforstyrrelser. Symptomer på hyperkaliæmi omfatter hjerterytmeforstyrrelser og alvorlig muskelsvaghed.Desværre kan hyperkaliæmi forekomme asymptomatisk, hvilket understreger vigtigheden af overvågning.18,27
Renininhibitor: Aliskiren er den eneste reninhæmmer, der i øjeblikket er på markedet. Den er indiceret til behandling af HTN som monoterapi eller som kombinationsbehandling medvalsartan. Nylige data fra ALTITUDE-forsøget har ført til kontraindikation af dets anvendelse sammen med ACE-hæmmere eller ARB’er hos patienter med diabetes eller nedsat nyrefunktion (GFR <60 mL/min) på grund af den øgede risiko for nedsat nyrefunktion, hypotension og hyperkaliæmi.29 Aliskiren kan overvejes, hvis patienten ikke kan tage en ACE-hæmmer eller en ARB; dets anvendelse kan dog ikke anbefales hos patienter med nyreinsufficiens i stadie 4 eller 5.30
Betablokker: Data, der evaluerer virkningen af betablokkere på progression af CKD og proteinuri, er begrænsede.27 Selv om betablokkere ikke er medtaget i TABEL 2, kan disse midler overvejes som anden- eller tredjelinjebehandling, hvis patienten har en tvingende indikation for en betabloker, såsom koronararteriesygdom eller kronisk hjertesvigt.18
Nonfarmakologiske anbefalinger
Khronoterapi: Denne type terapi tager hensyn til det cirkadiske blodtryksmønster og indfører administration af antihypertensiv medicin i forhold til de daglige mønstre, idet man går bort fra administration af al antihypertensiv medicin om morgenen. Forsøg har vist forbedret 24-timers BP-kontrol hos patienter, der får CCB’er om aftenen i stedet for om morgenen.31,32 Yderligere undersøgelser har påvist fordele ved natlig administration af andre antihypertensive lægemidler såsom ACE-hæmmere eller ARB’er.33,34 Kronoterapi kan være berettiget at overveje for dem, der ikke kan nå deres BP-mål, når de administrerer alle antihypertensive midler om morgenen. Hvis patienterne er på mere end to antihypertensive midler, kan det være hensigtsmæssigt at indgive to midler om morgenen og de yderligere midler om aftenen.
Livsstilsmodifikation: Øget fysisk aktivitet, vægttab og kostændringer anbefales til alle patienter med HTN.8 Livsstilsmodifikation er fortsat en afgørende komponent i behandlingen af HTN, uanset om patienterne har brug for medicin for at opnå deres BP-mål. DASH-diæten (Dietary Approaches to Stop Hypertension) lægger vægt på et øget forbrug af frugt og grøntsager, inddragelse af fedtfattige mælkeprodukter og magert protein samt begrænsning af mættet fedt; denne måltidsplan har vist sig at sænke det systoliske blodtryk betydeligt, hvilket næsten svarer til den reduktion, der opnås ved antihypertensiv monoterapi.35 Desuden er det blevet fastslået, at en reduktion af natrium- og alkoholindtaget er en effektiv intervention til at sænke blodtrykket.8Indførelse af disse sunde kostvaner, samtidig med at den daglige aktivitet øges, øger den fordel, der opnås ved antihypertensiv behandling, og kan spille en væsentlig rolle i forbindelse med opnåelse af BP-mål.
Summary
Sammenhængen mellem CKD og HTN fører til yderligere fokus på vigtigheden af at opnå BP-kontrol og mindske proteinuri, hvis den er til stede. Midler, der reducerer proteinuri ud over BP, er generelt førstevalg, men patienterne kan ofte have brug for tre til fire antihypertensive midler for at nå deres mål og minimere deres risiko for CVD og ESRD. Desuden bør sunde livsstilsændringer altid betragtes som en vigtig del af ethvert antihypertensivt behandlingsregime.
1. Coresh J, Selvin E, Stevens LA, et al. Prævalens af kronisk nyresygdom i USA. JAMA. 2007;298;298:2038-2047.
2. Collins AJ, Foley RN, Chavers B, et al. U.S. renal data system 2011 annual data report. Am J Kidney Dis. 2012;59(suppl 1):evii.
3. Matsushita K, van der Velde M, Astor BC, et al.Association of estimated glomerular filtration rate and albuminuria withall-cause and cardiovascular mortality in general population cohorts: acollaborative meta-analysis. Lancet. 2010;375;375:2073-2081.
4. Rashidi A, Sehgal AR, Rahman M, O’Connor AS. Det er tilfældet for kronisk nyresygdom, diabetes mellitus og myokardieinfarkt, der er tilsvarende risikofaktorer for kardiovaskulær dødelighed hos patienter over 65 år. Am J Cardiol. 2008;102:1668-1673.
5. Rao MV, Qiu Y, Wang C, Bakris G. Hypertension og CKD: Kidney Early Evaluation Program (KEEP) og National Health and NutritionExamination Survey (NHANES), 1999-2004. Am J Kidney Dis. 2008;51(suppl 2):S30-S37.
6. Botdorf J, Chaudhary K, Whaley-Connell A. Hypertension in cardiovascular and kidney disease. Cardiorenal Med. 2011;1:183-192.
7. Segura J, Ruilope L. Hypertension in moderate-to-severe nondiabetic CKD patients. Adv Chronic Kidney Dis. 2011;18:23-27.
8. Chobanian AV, Bakris GL, Black HR, et al. The seventhreport of the Joint National Committee on Prevention, Detection,Evaluation, and Treatment of High Blood Pressure: the JNC 7 report. JAMA. 2003;289:2560-2572.
9. National Kidney Foundation. K/DOQI clinical practiceguidelines for chronic kidney disease: evaluation, classification, andstratification (K/DOQI-retningslinjer for klinisk praksis for kronisk nyresygdom: evaluering, klassificering og stratificering). Am J Kidney Dis. 2002;39(suppl 1):S1-S266.
10. American Diabetes Association. Standards of medical care in diabetes-2012. Diabetes Care. 2012;35(suppl 1):S1-S63.
11. Bakris GL, Williams M, Dworkin L, et al. Bevarelse af binyrebarkfunktionen hos voksne med forhøjet blodtryk og diabetes: en konsensustilgang. National Kidney Foundation Hypertension and Diabetes ExecutiveCommittees Working Group. Am J Kidney Dis. 2000;36:646-661.
12. Keane WF, Eknoyan G. Proteinuria, albuminuria, risk,assessment, detection, elimination (PARADE): a position paper for theNational Kidney Foundation. Am J Kidney Dis. 1999;33:1004-1010.
13. Yoshioka T, Rennke HG, Salant DJ, et al. Rolle af et unormalt højt transmuralt tryk i den permselektivitetsdefekt i den glomerulære kapillarvæg: en undersøgelse af tidlig passiv Heymann-nefritis. Circ Res. 1987:61:61:531-538.
14. Sarnak M, Levey A, Schoolwerth A, et al. Nyresygdom som en risikofaktor for udvikling af hjerte-kar-sygdomme: en erklæring fra American Heart Association Councils on Kidney inCardiovascular Disease, High Blood Pressure Research, ClinicalCardiology, and Epidemiology and Prevention. Circulation. 2003;108:2154-2169.
15. Upadhyay A, Earley A, Haynes SM, Uhlig K. Systematicreview: blood pressure target in chronic kidney disease and proteinuriaas an effect modifier. Ann Intern Med. 2011;154:541-548.
16. Cushman C, Evan GW Byington RP, et al. The ACCORDstudy group. Intensiv blodtrykkontrol ved type 2-diabetesmellitus. N Engl J Med. 2010;363:1575-1585.
17. Brenner BM, Cooper ME, Cooper ME, De Zeeuw D, et al. Effekter aflosartan på nyre- og kardiovaskulære resultater ved type 2-diabetes og nefropati. N Engl J Med. 2001;345:861-869.
18. Kidney Disease Outcomes Quality Initiative (K/DOQI).K/DOQI clinical practice guidelines on hypertension and antihypertensiveagents in chronic kidney disease (K/DOQI kliniske retningslinjer for hypertension og antihypertensive midler ved kronisk nyresygdom). Am J Kidney Dis. 2004;43(suppl 1):S1-S290.
19. Remuzzi G, Chiurchiu C, Ruggenenti P. Proteinuria predicting outcome in renal disease: nondiabetic nephropathies (REIN). Kidney Int Suppl. 2004;66:S90-S96.
20. Sharma P, Blackburn RC, Parke CL, et al. angiotensinkonverterende enzymhæmmere og angiotensinreceptorblokkere til voksne med tidlig (stadie 1 til 3) ikke-diabetisk kronisk nyresygdom. Cochrane Database Syst Rev. 2011;(10):CD007751.
21. van Vark LC, Bertrand M, Akkerhuis KM, et al.Angiotensin-converting enzyme inhibitors reduce mortality inhypertension: a meta-analysis of randomized clinical trials ofrenin-angiotensin-aldosterone systemhibitors involving 158,998patients. Eur Heart J. 2012 Apr 17; Epub ahead of print.
22. Vigtige resultater hos hypertensive højrisikopatienter, der er randomiseret til angiotensin-konverterende enzym-hæmmer eller calciumkanalblokker vs. diuretika: Antihypertensive and Lipid-Lowering Treatmentto Prevent Heart Attack Trial (ALLHAT). JAMA. 2002;288:2981-2997.
23. Musini VM, Wright JM, Bassett K, Jauca CD. Blodtrykssænkende effekt af loopdiuretika ved primær hypertension. Cochrane Database Syst Rev. 2009;(4):CD003825.
24. Microzide (hydrochlorthiazid orale kapsler) indlægsseddel. Watson Pharma, Inc: Morristown, NJ; 2011.
25. Chlorthalidon orale tabletter indlægsseddel. Mylan Pharmaceuticals, Inc: Morgantown, WV; 2006.
26. Bakris GL, Weir MR, Secic M, et al. Differentialeffekter af calciumantagonistunderklasser på markører for nefropathiprogression. Kidney Int. 2004;65;65:1991-2002.
27. Navaneethan SD, Nigwekar SU, Sehgal AR, et al.Aldosteronantagonister til forebyggelse af progressionen af kronisk nyresygdom. Clin J Am Soc Nephrol. 2009;4:542-551.
28. Mehdi UF, Adams-Huet B, Raskin P, et al. Tilføjelse afangiotensinreceptorblokade eller mineralokortikoidantagonisme til maksimalangiotensin-konverterende enzymhæmning i diabetisk nefropati. J Am Soc Nephrol. 2009;20:2641-2650.
29. Aliskiren-holdige lægemidler: meddelelse om lægemiddelsikkerhed – ny advarsel og kontraindikation. MedWatch.20. april 2012.www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm301120.htm?source=govdelivery;4/20/2012.Besøgt 1. maj 2012.
30. Trimarchi H. Aliskirens rolle i blodtrykskontrol og renoprotektion. Int J Nephrol Renovasc Dis. 2011;4:41-48.
31. Portaluppi F, Vergnani L, Manfredini R, et al.Tidsafhængig effekt af isradipin på natlig hypertension inchronic nyresvigt. Am J Hypertens. 1995;8:719-726.
32. Hermida RC, Calvo C, Ayala DE, et al. Dosis- og administrationstidsafhængige virkninger af nifedipin GITS på det ambulante blodtryk hos hypertensive personer. Chronobiol Int. 2007;24:471-493.
33. Hermida RC, Ayala DE. Kronoterapi med denangiotensin-konverterende enzymhæmmer ramipril ved essentielhypertension: forbedret blodtrykskontrol med sengetidsdosering. Hypertension. 2009;54:40-46.
34. Hermida RC, Calvo C, Ayala DE, et al. Administrationstidsafhængige virkninger af valsartan på det ambulante blodtryk hoshypertensive personer. Hypertension. 2003;42:283-290.
35. Sacks FM, Svetkey LP, Vollmer WM, et al. Effekter på blodtrykket af reduceret natrium i kosten og DASH-diæten (Dietary Approaches to Stop Hypertension). DASH-Sodium Collaborative Research Group.N Engl J Med. 2001;344:3-10.