Tämä on lyhyt yleiskatsaus tietoihin, jotka liittyvät FDA:n hyväksyntään tämän tuotteen markkinoinnille. Katso alla olevista linkeistä Turvallisuus- ja tehokkuustietojen yhteenveto (SSED) ja tuoteseloste, josta löydät kattavammat tiedot tästä tuotteesta, sen käyttöaiheista ja FDA:n hyväksynnän perusteista.
Tuotteen nimi: Axonics Sacral Neuromodulation System
PMA Hakija: Axonics Modulation Technologies, Inc: 26 Technology Drive, Irvine, CA 92618
Hyväksyntäpäivä: November 13, 2019
Hyväksyntäkirje: Approval Order
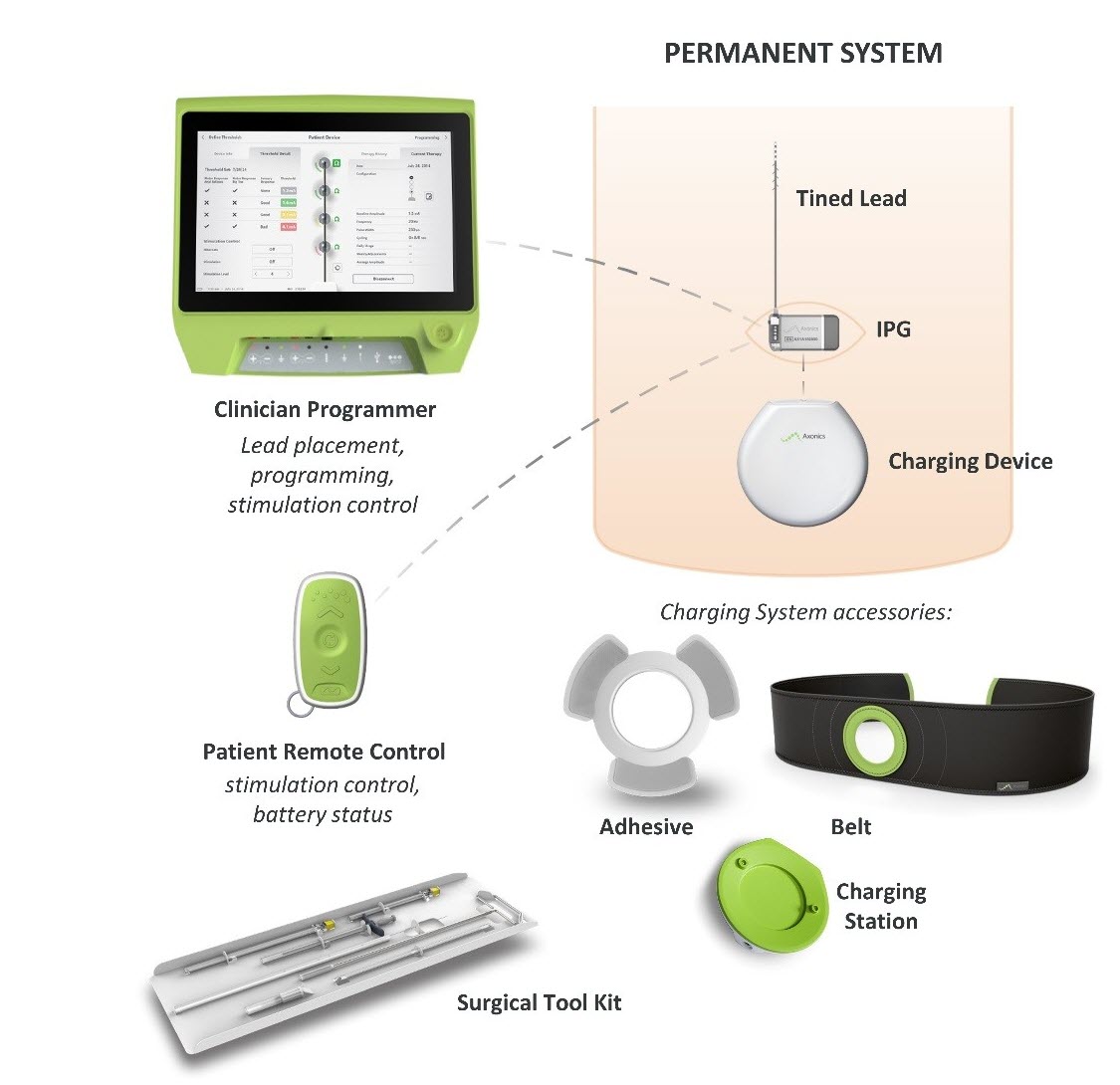
Mitä se on? Axonics Sacral Neuromodulation (SNM) System on sakraalihermon stimulaatiojärjestelmä (SNS), joka on tarkoitettu virtsanpidätyskyvyn ja yliaktiivisen rakon oireiden hoitoon. Se käyttää implantoitua stimulaattoria, joka syöttää sähköimpulsseja johtimen kautta sakraalihermon lähellä sijaitseviin elektrodeihin.
Miten se toimii? Implantoitava pulssigeneraattori (IPG) asetetaan kirurgisesti ihon alle pakaroiden yläosaan ja kiinnitetään johtojohtimeen, joka kulkee lantion lonkkaluiden välissä ja päättyy ristihermoon. IPG lähettää sähköimpulsseja johdinjohdon kautta ristimähermoon, joka kulkee selkäytimestä virtsarakkoon ja auttaa parantamaan virtsaamisen hallintaa.
Milloin sitä käytetään? Virtsankontrollin Axonics SNM -järjestelmää käytetään virtsanpidätyskyvyn ja yliaktiivisen rakon oireiden hoitoon potilailla, jotka eivät ole onnistuneet tai sietäneet muita hoitoja, kuten elämäntapamuutoksia, lantionpohjan harjoituksia tai lääkitystä. Hoitamattomana virtsaretentio ja yliaktiivinen rakko voivat heikentää potilaan elämänlaatua ja aiheuttaa merkittäviä haasteita päivittäisten elintoimintojen ylläpitämisessä.
Mitä sillä saavutetaan? Axonics SNM -järjestelmää koskevan kliinisen tutkimuksen tulokset yhdistettynä vastaavasta SNM-laitteesta saatavilla olevan kirjallisuuden systemaattisesta katsauksesta koottuihin kliinisiin lisätietoihin osoittavat, että siitä on hyötyä useimmille potilaille, joilla on virtsanpidätyskyvyttömyys ja yliaktiivisen virtsarakon oireet ja jotka eivät ole onnistuneet tai jotka eivät ole sietäneet muita hoitoja. Axonicsin kliinisessä tutkimuksessa, johon osallistui potilaita, joilla oli virtsankarkailuinkontinenssia, 90 % (116/129) potilaista, joille oli istutettu SNM-järjestelmä, saavutti vähintään 50 %:n vähennyksen virtsankarkailuvuotojen määrässä kuuden kuukauden kuluttua verrattuna virtsankarkailuvuotojen määrään ilman SNM-järjestelmää. Pitkäaikaisemmassa tutkimuksessa (van Kerrebroeck, 2007) seurattiin 152 potilasta, joille oli istutettu samanlainen SNM-laite, viiden vuoden ajan. Viiden vuoden kuluttua 58 prosentilla (56/96) potilaista, joilla oli kiireellinen virtsainkontinenssi, oli vähintään 50 prosentin parannus (mitattuna vuotojen määränä päivässä). Lisäksi viiden vuoden kuluttua 40 %:lla (10/25) potilaista, joilla oli kiireellinen virtsankarkailu, oli vähintään 50 %:n parannus (mitattuna tyhjennysten määränä päivässä), ja 58 %:lla (18/31) potilaista, joilla oli virtsanpidätyskyvyttömyys, oli vähintään 50 %:n parannus (mitattuna katetrointien määränä päivässä). Ottaen huomioon samankaltaisuudet suunnittelussa, teknologiassa, suorituskyvyssä, käyttöaiheissa, tuotosominaisuuksissa ja potilasryhmässä, jota sillä on tarkoitus hoitaa, FDA uskoo, että Axonics SNM -järjestelmän suorituskyky on samankaltainen kuin julkaistujen tutkimusten perusteella arvioitujen kaupallisesti saatavilla olevien SNM-järjestelmien suorituskyky.
Milloin sitä ei saa käyttää? Axonics SNM -järjestelmää ei saa käyttää:
- Potilaille, jotka eivät ole osoittaneet asianmukaista vastetta testistimulaatiolle; tai
- Potilaille, jotka eivät kykene käyttämään Axonics SNM -järjestelmää
Lisätiedot (mukaan lukien varoitukset, varotoimet ja haittavaikutukset):
- Yhteenveto turvallisuutta ja tehoa koskevista tiedoista
- Potilaan merkinnät
- Lääkärin merkinnät
- PMA-tietokannan merkinnät
.