Che cos’e’ il Lutezio
Il Lutezio (pronunciato come loo-TEE-shee-em) e’ un metallo argenteo, duro, denso delle terre rare classificato come lantanide e rappresentato dal simbolo chimico Lu. È l’ultimo elemento chimico appartenente alla serie dei lantanidi, e l’isotopo più abbondante e stabile in natura è il 175Lu (97,4% di abbondanza). Un altro isotopo radioattivo a lunga vita 176Lu ha un periodo di emivita di 3.78 X 1010 anni.

Lutezio Simbolo
Dove si trova il lutezio
Il lutezio, allo stesso modo degli altri lantanidi, è ottenuto commercialmente dal minerale monazite. Poiché si presenta in piccole quantità (circa 0,003%) nella monazite, la sua estrazione può essere difficile ed è fatta tramite riduzione del fluoruro anidro usando il calcio metallico. Anche se l’elemento si trova in tracce in quasi tutti i minerali che contengono ittrio, possono essere considerati come fonti naturali di lutezio. I primi 3 paesi produttori di lutezio sono la Cina, la Russia e la Malesia mentre le prime 3 nazioni detentrici di riserve includono la Cina, i paesi della CSI e gli Stati Uniti.

Lutezio
Storia
Origine del suo nome: Il nome dell’elemento deriva dalla parola romana ‘Lutetia’, l’antico nome della città francese di Parigi.
Chi l’ha scoperto: Anche se il chimico francese Georges Urbain, il chimico americano Charles James, e lo scienziato austriaco Carl Auer von Welsbach scoprirono indipendentemente l’elemento, il merito della scoperta andò a Urbain poiché fu il primo a riportare i risultati.
Quando e come fu scoperto
Il minerale gadolinite o ittrio, scoperto nel 1794, è stato la fonte di ittria, terbia, erbia, e altri elementi delle terre rare. Il chimico svizzero Jean Charles Marignac separò l’erbia in due componenti, tra cui l’itterbio e l’erbia, da cui l’itterbio si credeva fosse un composto dell’itterbio.
Nel 1907, Georges Urbain mentre sperimentava alla Sorbona di Parigi isolò con successo l’itterbio in due elementi, che chiamò lutecium e neoytterbium. Tuttavia, questi elementi furono successivamente rinominati rispettivamente lutezio e itterbio dai chimici. Carl Auer von Welsbach separò l’elemento dall’itterbio e lo chiamò cassipoium dalla costellazione circumpolare Cassiopea. Anche Charles James estrasse con successo l’elemento all’Università del New Hampshire.
Anche se è difficile da preparare, il metallo puro lutezio fu prodotto nel 1953.
Identificazione del lutezio |
|||
| Numero atomico | 71 | ||
| Numero CAS | 7439-94-3 | ||
| Posizione nella tavola periodica | Gruppo | Periodo | Blocco |
| Lantanidi | 6 | f | |

Posizione del Lutezio nella tavola periodica
Proprietà e caratteristiche del Lutezio
Proprietà generali |
||||||||||||||||
| Massa atomica | 174.967 amu | |||||||||||||||
| Massa atomica relativa | 174.967 | |||||||||||||||
Proprietà fisiche |
||||||||||||||||
| Colore | bianco argenteo | |||||||||||||||
| Punto di fusione/di congelamento | 1663 °C, 3025 °F | |||||||||||||||
| Punto di ebollizione | 3402 °C, 6156 °F | |||||||||||||||
| Densità | 9.84 g cm-3 | |||||||||||||||
| Stato della materia a temperatura ambiente (solido/liquido/gas) | Solido | |||||||||||||||
| Durezza | ||||||||||||||||
| – Brinell | 893 MPa | |||||||||||||||
| – Mohs | 2.6 | |||||||||||||||
| – Vickers | 1160 MPa | |||||||||||||||
| Conducibilità elettrica | 1.8X106 S/m | |||||||||||||||
| Conducibilità termica (calore) | 16 W/(m K) | |||||||||||||||
| Calore specifico | 154 J kg-1 K-1 | |||||||||||||||
| Modulo elastico | 47.6 GPa | |||||||||||||||
| Modulo di taglio | 27.2 GPa | |||||||||||||||
| Modulo di Young | 68.6 GPa | |||||||||||||||
| Pressione di vapore | ||||||||||||||||
| – Temperatura (K) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | |||||
| – Pressione (Pa) | – | – | – | 3.28X 10-11 | 1.59X 10-7 | 6.79X 10-5 | 6.28X 10-3 | 0.211 | 3.18 | 26.7 | – | |||||
Proprietà chimiche |
||||||||||||||||
| Stati di ossidazione | 3 | |||||||||||||||
| Isotopi | Isotopo | Massa | Abbondanza | Metàvita | Modo di decadimento | |||||||||||
| 175Lu | 174.941 | 97.40 | – | – | ||||||||||||
| 176Lu | 175.943 | 2.60 | 3.73 X 1010 anni | β-
β+ EC |
||||||||||||
Dati atomici del lutezio (elemento 71)
| Valenza elettroni | 3 | |||||||
| Numeri quantici | 2D3/2 | |||||||
| Configurazione degli elettroni (configurazione dei gas nobili) | 4f145d16s2 | |||||||
| Struttura atomica | ||||||||
| – Numero di elettroni | 71 | |||||||
| – Numero di neutroni | 104 | |||||||
| – Numero di protoni | 71 | |||||||
| >Raggio dell’atomo | ||||||||
| – Raggio atomico | 2.24 Å | |||||||
| – Raggio covalente | 1.74 Å | |||||||
| Elettronegatività (scala di Pauling) | 1.0 | |||||||
| Affinità elettronica | 32.81 kJ mol-1 | |||||||
| Energia di ionizzazione (kJ mol-1) | 1° | 2° | 3° | 4° | 5° | 6° | 7° | 8° |
| 523.516 | 1341.1 | 2022.275 | 4365.96 | 6445.2 | – | – | – | |
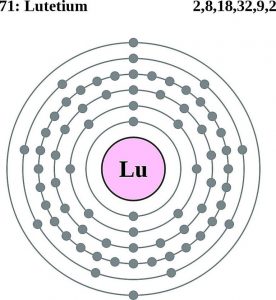
Configurazione elettronica del lutezio (modello Bohr)
A cosa serve
Ha poco uso pratico al di fuori della ricerca scientifica. Alcuni usi commerciali del lutezio sono dati qui sotto:
- Può essere usato come catalizzatore per il cracking dei prodotti petroliferi nelle raffinerie di petrolio.
- La radioimmunoterapia con lutezio-177-dotato è usata come forma di trattamento del cancro mentre il lutezio-176 è usato per la datazione radiometrica dei meteoriti.
- L’ossitrosilicato di lutezio è usato nei rivelatori PET (tomografia ad emissione di positroni) per eseguire una scansione medica per creare un’immagine 3D dell’attività cellulare nel corpo.
Possibili effetti sulla salute
Il lutezio ha una bassa tossicità e nessuna funzione biologica conosciuta nel corpo umano; anche se si pensa che possa aiutare ad aumentare il metabolismo. Si crede anche che sia un pericolo di esplosione.
Fatti interessanti
- Il lutezio è l’elemento più duro e più denso del gruppo dei lantanidi.
- Esiste in composti generalmente nel suo stato trivalente, Lu3+.
- L’elemento è a volte rappresentato visivamente da un’immagine basata sullo stemma di Parigi.
Costo del lutezio
La forma pura del lutezio costa circa 350 dollari al grammo, ma costa circa 7.000 dollari per 100 grammi all’ingrosso.
- http://www.rsc.org/periodic-table/element/71/lutetium
- https://education.jlab.org/itselemental/ele071.html
- https://www.livescience.com/38425-lutetium.html
- https://www.webelements.com/lutetium/isotopes.html
- https://www.chemicool.com/elements/lutetium.html
- http://periodictable.com/Elements/071/data.html
- http://web.newworldencyclopedia.org/entry/Lutetium
- https://hobart.k12.in.us/ksms/PeriodicTable/lutetium.htm