La sublimación es el proceso en el que un material pasa de sólido congelado a gas sin pasar por el estado líquido intermedio.
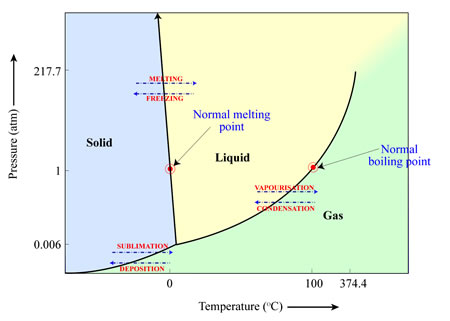
El hecho de que un material se sublime (de sólido a gas), se funda (de sólido a líquido) o se vaporice (de líquido a gas) depende de la temperatura y la presión del entorno en el que se encuentra. Esto puede ilustrarse en un “diagrama de fases” como el que se muestra a continuación para el agua. En este caso, y con las presiones (1 atmósfera) y temperaturas (25 grados Celsius) a las que estamos acostumbrados en la Tierra, el hielo del agua se fundirá para formar agua líquida, que luego se vaporizará para formar vapor de agua. Sin embargo, si las presiones son lo suficientemente bajas (por ejemplo, las presiones que encontramos en otros lugares del Sistema Solar), el hielo de agua se convertirá directamente en vapor de agua a medida que aumente la temperatura, obviando la etapa de agua líquida.
La sublimación se produce en muchos lugares del Sistema Solar. Dos ejemplos son:
- La sublimación del agua de los núcleos cometarios cuando el cometa se acerca al Sol’
- La sublimación de los casquetes polares de Marte durante el verano marciano.
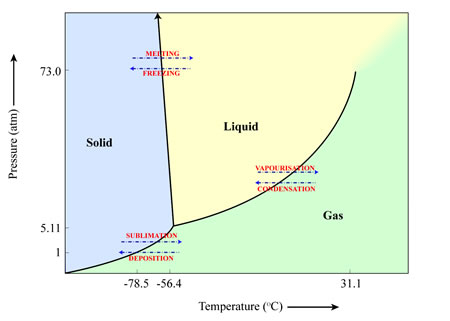
Un ejemplo de material que se sublima aquí en la Tierra es el dióxido de carbono (CO2) congelado, más conocido como “hielo seco”. Cuando se expone al aire a temperatura ambiente a presiones de 1 atmósfera, el CO2 congelado se convierte directamente en CO2 gaseoso.