Hvad er Lutetium
Lutetium (udtales som loo-TEE-shee-em) er et sølvfarvet, hårdt, tæt sjældent jordarters metal klassificeret som en lanthanid og repræsenteret ved det kemiske symbol Lu . Det er det sidste kemiske grundstof, der hører til lanthanidserien , med den mest naturligt hyppige, stabile isotop 175Lu (97,4 % hyppighed). En anden langlivet radioaktiv isotop 176Lu har en halveringstid periode på 3,78 X 1010 år .

Lutetium Symbol
Hvor findes lutetium
Lutetium, på samme måde som andre lanthanider, udvindes kommercielt fra mineralet monazit . Da det forekommer i små mængder (ca. 0,003%) i monazit , kan udvindingen være vanskelig og sker ved reduktion af vandfrit fluorid ved hjælp af calciummetal . Selv om grundstoffet findes i spormængder i næsten alle mineraler, der indeholder yttrium, kan de betragtes som naturlige kilder til lutetium . De 3 største lutetiumproducerende lande er Kina, Rusland og Malaysia, mens de 3 største reserveholdige nationer omfatter Kina, SNG-landene og USA .

Lutetium
Historie
Navnets oprindelse: Grundstoffets navn er afledt af det romerske ord “Lutetia”, det gamle navn for den franske by Paris .
Hvem opdagede det:
Hvor opdagede det: Selv om den franske kemiker Georges Urbain, den amerikanske kemiker Charles James og den østrigske videnskabsmand Carl Auer von Welsbach uafhængigt af hinanden opdagede grundstoffet, gik æren for opdagelsen til Urbain, da han var den tidligste til at rapportere resultaterne .
Hvornår og hvordan blev det opdaget
Mineralet gadolinit eller yttrium, der blev opdaget i 1794, har været kilden til yttrium, terbia, erbia og andre sjældne jordarters grundstoffer . Den schweiziske kemiker Jean Charles Marignac adskilte erbia i to komponenter, herunder ytterbia og erbia, hvoraf ytterbia blev anset for at være en forbindelse af ytterbium .
I 1907 lykkedes det Georges Urbain under sine eksperimenter på Sorbonne i Paris at isolere ytterbium i to grundstoffer, som han kaldte lute lutecium og neoytterbium . Disse grundstoffer blev dog senere omdøbt til henholdsvis lutetium og ytterbium af kemikere . Carl Auer von Welsbach adskilte grundstoffet fra ytterbia og kaldte det cassipoium efter det cirkumpolære stjernebillede Cassiopeia . Charles James har også med succes udvundet grundstoffet på University of New Hampshire .
Og selv om det er vanskeligt at fremstille, blev det rene lutetiummetal fremstillet i 1953 .
Lutetium Identifikation |
|||
| Atometrisk nummer | 71 | ||
| CAS-nummer | 7439-94-3 | ||
| Position i det periodiske system | Gruppe | Periode | Blok |
| Lanthanider | 6 | f | |

Lokalisering af lutetium i det periodiske system
Lutetiums egenskaber og karakteristika
Allmene egenskaber |
|||||||||||||||||||
| Atommasse | 174.967 amu | ||||||||||||||||||
| Relativ atommasse | 174.967 | ||||||||||||||||||
Fysiske egenskaber |
|||||||||||||||||||
| Farve | Sølvhvid | ||||||||||||||||||
| Smeltningspunkt/frysepunkt | 1663 °C, 3025 °F | ||||||||||||||||||
| Kogningspunkt | 3402 °C, 6156 °F | ||||||||||||||||||
| Densitet | 9.84 g cm-3 | ||||||||||||||||||
| Stoftilstand ved stuetemperatur (fast/flydende/gas) | Fest | ||||||||||||||||||
| Hårdhed | |||||||||||||||||||
| – Brinell | 893 MPa | ||||||||||||||||||
| – Mohs | 2.6 | ||||||||||||||||||
| – Vickers | 1160 MPa | ||||||||||||||||||
| Elektrisk ledningsevne | 1.8X106 S/m | ||||||||||||||||||
| Thermisk (varme) ledningsevne | 16 W/(m K) | ||||||||||||||||||
| Specifik varme | 154 J kg-1 K-1 | ||||||||||||||||||
| Masse-modul | 47.6 GPa | ||||||||||||||||||
| Skrængningsmodul | 27,2 GPa | ||||||||||||||||||
| Young’s modul | 68.6 GPa | ||||||||||||||||||
| Damptryk | |||||||||||||||||||
| – Temperatur (K) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | ||||||||
| – Tryk (Pa) | – | – | – | – | 3.28X 10-11 | 1,59X 10-7 | 6,79X 10-5 | 6,28X 10-3 | 0,211 | 3,18 | 26.7 | – | |||||||
Kemiske egenskaber |
|||||||||||||||||||
| Oxidationstilstande | 3 | ||||||||||||||||||
| Isotoper | Isotop | Masse | Mængde | Fordeling | Halv-levetid | Afbrydningsmåde | |||||||||||||
| 175Lu | 174.941 | 97,40 | – | – | |||||||||||||||
| 176Lu | 175,943 | 2,60 | 3.73 X 1010 år | β-
β+ EC |
|||||||||||||||
Atomdata for lutetium (grundstof 71)
| Valence elektroner | 3 | ||||||||
| Kvantumtal | 2D3/2 | ||||||||
| Elektronkonfiguration (ædelgaskonfiguration) | 4f145d16s2 | ||||||||
| Atomstruktur | |||||||||
| – Antal elektroner | 71 | ||||||||
| – Antal neutroner | 104 | ||||||||
| – Antal protoner | 71 | ||||||||
| Atomets radius | |||||||||
| – Atomets radius | 2.24 Å | ||||||||
| – Kovalent radius | 1,74 Å | ||||||||
| Elektronegativitet (Pauling-skala) | 1,0 | ||||||||
| Elektronaffinitet | 32.81 kJ mol-1 | ||||||||
| Ioniseringsenergi (kJ mol-1) | 1st | 2nd | 3rd | 4th | 5th | 6th | 6th | 7th | 8th |
| 523.516 | 1341.1 | 2022.275 | 4365.96 | 6445.2 | – | – | – | ||
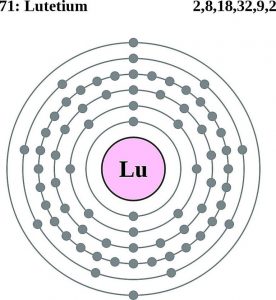
Lutetium-elektronkonfiguration (Bohr-model)
Hvad bruges den til
Den har kun lidt praktisk anvendelse uden for videnskabelig forskning . Et par kommercielle anvendelser af lutetium er angivet nedenfor:
- Det kan anvendes som katalysator til krakning af olieprodukter i olieraffinaderier .
- Radioimmunoterapi med lutetium-177-dotatat anvendes som en form for kræftbehandling, mens lutetium-176 anvendes til radiometrisk datering af meteoritter .
- Lutetiumoxyorthosilikat bruges i PET-detektorer (positronemissionstomografi) til at udføre en medicinsk scanning for at skabe et 3D-billede af celleaktiviteten i kroppen.
Mulige sundhedsmæssige virkninger
Lutetium har lav toksicitet og ingen kendte biologiske funktioner i menneskekroppen ; men det menes dog at kunne bidrage til at øge stofskiftet. Det menes også at være en eksplosionsfare .
Interessante fakta
- Lutetium er det hårdeste og tætteste grundstof i lanthanidgruppen .
- Det findes i forbindelser generelt i sin trivalente tilstand, Lu3+ .
- Elementet er undertiden visuelt afbildet ved et billede baseret på Paris’ våbenskjold .
Kostpris for lutetium
Den rene form af lutetium koster omkring 350 dollars pr. gram , men det koster omkring 7.000 dollars pr. 100 gram i bulk .
- http://www.rsc.org/periodic-table/element/71/lutetium
- https://education.jlab.org/itselemental/ele071.html
- https://www.livescience.com/38425-lutetium.html
- https://www.webelements.com/lutetium/isotopes.html
- https://www.chemicool.com/elements/lutetium.html
- http://periodictable.com/Elements/071/data.html
- http://web.newworldencyclopedia.org/entry/Lutetium
- https://hobart.k12.in.us/ksms/PeriodicTable/lutetium.htm