- Deel C: Bouwen van koolstofverbindingen
- Laboratoriumonderzoek 1: Bewijs voor een chemische verandering
- Checking In
- Discussie
- Laboratoriumonderzoek 2: Modelleren van fotosynthese en celademhaling
- Checking In
- Laboratoriumonderzoek 3: Biosynthese van nieuwe biomoleculen uit glucose
- Discussie
- Inchecken
- Stop en denk na:
- Optionele uitbreidingen
Deel C: Bouwen van koolstofverbindingen


In de koolstofkringloop zijn koolstofatomen voortdurend in beweging, cyclisch in en uit verschillende componenten van de biosfeer en de geosfeer. Koolstofatomen bewegen niet als afzonderlijke atomen, maar als onderdeel van koolstofverbindingen, sommige klein en eenvoudig en andere groot en zeer complex. De koolstofcyclus is nauw verbonden met andere biogeochemische cycli cycli van andere chemische elementen zoals stikstof, fosfor, zwavel en ijzer, die naar en uit verschillende componenten van de geosfeer en de biosfeer stromen. . Veel koolstofverbindingen die door levende organismen worden geproduceerd, bevatten bijvoorbeeld stikstof- en fosforatomen.
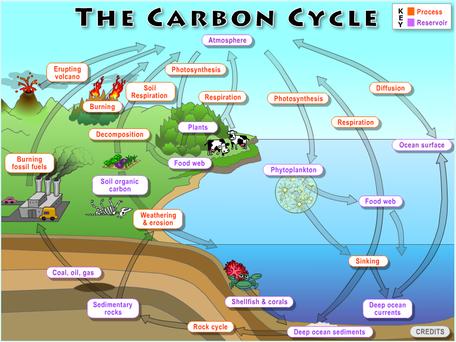
De wereldwijde koolstofcyclus toont de paden (pijlen) van koolstofatomen van het ene deel van de koolstofcyclus naar het andere. Paarse letters verwijzen naar de plaatsen waar koolstofverbindingen voorkomen en oranje letters verwijzen naar processen die ervoor zorgen dat koolstof langs de paden wordt verplaatst.
Bekijk de afbeelding van de wereldwijde koolstofcyclus rechts, (klik om de afbeelding te vergroten). Elke pijl stelt een pad voor dat koolstofatomen nemen als zij zich door de Geosfeer en de Biosfeer bewegen. Sommige van deze koolstofverbindingen verplaatsen zich snel van het ene deel van de koolstofcyclus naar het andere, terwijl andere miljoenen en miljoenen jaren worden opgeslagen. Terwijl koolstofverbindingen zich door de geosfeer en de biosfeer verplaatsen, ondergaan zij veel verschillende chemische veranderingen. Deze chemische veranderingen (transformaties) vereisen het breken en opbouwen van chemische bindingen tussen de atomen. Sommige van deze chemische veranderingen lijken vrij klein, maar kunnen grote invloed hebben op de koolstofcyclus, het klimaat en het milieu. Wanneer planten bijvoorbeeld anorganisch CO2 omzetten in organische suikers (C6H12C6), leveren zij voedsel voor dieren en andere heterotrofen organismen die hun eigen voedsel niet kunnen produceren en in plaats daarvan hun voedsel en energie verkrijgen door het opnemen van organische stoffen, meestal plantaardig of dierlijk materiaal; dieren, protozoën, schimmels en de meeste bacteriën zijn heterotrofen. Wanneer bodembacteriën koolstofverbindingen in de bodem afbreken, laten zij kooldioxide (CO2) of methaan (CO4) vrijkomen. Beide gassen zijn broeikasgassen en worden in verband gebracht met de klimaatverandering.
Wetenschappers voorspellen dat er vandaag de dag meer dan tien miljoen verschillende koolstofverbindingen op aarde bestaan. In dit deel ga je vier korte onderzoeken uitvoeren om te ontdekken hoe koolstofatomen zich kunnen verbinden met andere soorten atomen om de miljoenen verschillende soorten koolstofverbindingen te vormen die in de geosfeer en biosfeer te vinden zijn. Om je aan het denken te zetten over het vermogen van koolstof om zoveel verschillende soorten koolstofverbindingen te vormen, kun je deze korte NPR-videoclip bekijken, It’s All About Carbon: Episode 1.
NOOT: Als de video niet wordt geladen, kun je de video hier bekijken: Episode 1: Global Warming, It’s All About Carbon – YouTube U kunt ook deze link volgen waar u andere afleveringen van deze NPR-serie kunt bekijken.
Laboratoriumonderzoek 1: Bewijs voor een chemische verandering

Koralen en andere organismen die schelpen bouwen, zoals kokkels, oesters en kreeften, zijn afhankelijk van calciumcarbonaat om hun schelpen en skeletten te bouwen.
In de video die je zojuist hebt bekeken, heb je geleerd dat koolstofatomen zich gemakkelijk en sterk binden met andere atomen om veel verschillende soorten koolstofverbindingen te vormen. In dit onderzoek ga je op zoek naar bewijzen voor de vorming van een nieuwe koolstofverbinding wanneer twee koolstofverbindingen worden samengebracht: het CO2 uit je eigen adem en een oplossing van calciumhydroxide Ca(OH)2.
- Verandering van geur (bijvoorbeeld – zwavelgeur bij verbranding van een mat)
- Verandering van kleur (bijvoorbeeld – zilver naar roodbruin bij roestend ijzer).
- Wijziging van temperatuur
- Wijziging van samenstelling (b.v. – papier verandert in as bij verbranding)
- Verstraling van licht en/of warmte
- Vorming van gassen, vaak optredend als bellen in vloeistoffen
- Vorming van een neerslag (vaste onoplosbare deeltjes) die in oplossing verschijnen
- De afbraak van organisch materiaal (bijvoorbeeld rottend voedsel)
- De verandering is moeilijk of niet meer terug te draaien
Voor de klas:
- Een stuk krijt
- Witte azijn
- oogdruppelaar
Voor elk groepje:
- heldere plastic beker gedeeltelijk gevuld met kalkwater
- heldere plastic beker gedeeltelijk gevuld met water
- lege heldere plastic beker
- twee drinkrietjes
- klein (#2) koffiefilter
- water
- witte azijn
- oogdruppelaar
- (Klassendemonstratie) Krijt is gemaakt van calciumcarbonaat (CaCO3). Wanneer azijn aan krijt wordt toegevoegd, gaat het bruisen, wat erop wijst dat krijt van calciumcarbonaat is gemaakt. Je gaat de azijnproef gebruiken om de aanwezigheid van calciumcarbonaat aan te tonen.
- Bekijk het kalkwater en beschrijf het uiterlijk. Kalkwater is de gewone naam voor verzadigde calciumhydroxideoplossing, Ca(OH)2 (aq).
- Plaats een van de drinkrietjes in het kalkwater en blaas voorzichtig in de vloeistof. NIET INHALEREN OF TE HARD BLAZEN. Blijf uitademen door het rietje totdat zich een wit neerslag (vaste stof) vormt. De oplossing moet er zeer melkachtig uitzien met kleine deeltjes.
- Plaats het koffiefilter over het lege kopje. Giet het kalkwater voorzichtig door het filter in het kopje om het neerslag van de vloeistof te scheiden.
- Leg het filter met het witte neerslag opzij en laat het drogen en stollen.
- Plaats een rietje in een kopje gewoon water (in plaats van kalkwater) en blaas er zachtjes op. Observeer wat er gebeurt. Dit dient als experimentele controle.
- Om te bewijzen dat de stof die je uit het kalkwater hebt gefilterd inderdaad calciumcarbonaat is, voeg je met de oogdruppelaar een kleine hoeveelheid witte azijn toe aan het neerslag.
Checking In
Beschrijf hoe kalkwater en gewoon water verschillend reageren wanneer kooldioxidegas aan beide wordt toegevoegd.
Discussie
- Welke aanwijzingen heb je waargenomen dat er bij dit onderzoek een nieuw soort koolstofverbinding is gevormd.
- Beschrijf wat er met de koolstofatomen in koolstofdioxide (CO2) gebeurt als je CO2 in het kalkwater blaast?
- Waarom dient dit onderzoek als model voor het begrijpen van chemische verandering als een belangrijk onderdeel van de koolstofkringloop.
 Kooldioxide- en watermoleculen.
Kooldioxide- en watermoleculen. Laboratoriumonderzoek 2: Modelleren van fotosynthese en celademhaling
In dit onderzoek gebruik je een “ball and stick” moleculaire modelkit om te onderzoeken hoe de twee belangrijkste biosfeerprocessen fotosynthese en celademhaling nieuwe koolstofverbindingen maken. Verzamel je materiaal en volg de instructies voor het modelleren van fotosynthese en celademhaling hieronder:
6 bal-en-stok koolstofdioxidemoleculen – (6 koolstofatomen, 12 zuurstofatomen, 24 elektronenbindingsstaafjes)
6 bal-en-stok watermoleculen – (6 waterstofatomen, 12 zuurstofatomen, 12 elektronenbindingsstaafjes )
De afbeelding hiernaast illustreert hoe elk eruitziet.
- Koolstofatomen zijn zwart (of grijs) en hebben elk vier “pinnen”. Elk van deze tanden staat voor een elektronenverbinding tussen atomen.
- Waterstofatomen zijn wit. Waterstof heeft maar één tand en kan dus maar één elektronenverbinding met een ander atoom maken.
- Zuurstofatomen zijn rood en hebben twee tandjes. Zuurstofatomen kunnen dus twee elektronenbindingen aangaan met andere atomen, waaronder een ander zuurstofatoom.
- Elk wit of grijs stokje staat voor één elektronenbinding tussen twee atomen. OPMERKING: Soms kunnen koolstof en zuurstof dubbele bindingen vormen.
CO2-moleculen komen via de bladeren de planten binnen. H2O-moleculen komen de planten binnen vanuit de plantenwortels.
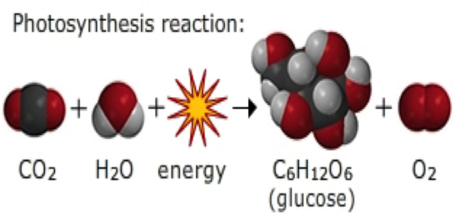
Gebruik de zes kooldioxide- en zes watermoleculen om de fotosynthese te modelleren. Hier is de chemische vergelijking voor fotosynthese.
6CO2 + 6H2O ==> C6H12O6 + 6O2

1. Begin met de koolstofdioxide- en watermoleculen uit elkaar te halen.
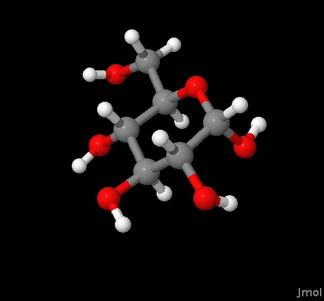
2. Bouw je glucosemolecuul met behulp van de afbeelding van een glucosemolecuul hiernaast als leidraad. Als je klikt om de afbeelding te vergroten, kun je goed zien hoe de koolstof-, waterstof- en zuurstofatomen aan elkaar gebonden zijn. OPMERKING: Haal de glucosemolecule pas uit elkaar als je begint met Onderzoek 3:
3. Gebruik de overgebleven zuurstofatomen en bindingen om zes O2-moleculen te bouwen (O=O). Deze zuurstofgasmoleculen worden aan de lucht afgegeven en leveren een deel van de benodigde zuurstof voor het leven op aarde.

Het proces van ademhaling breekt de chemische bindingen in het glucosemolecuul af, waardoor energie beschikbaar komt voor celfuncties. Atomen uit het glucosemolecuul worden ook gebruikt om biomassa op te bouwen. De bij deze reactie geproduceerde CO2- en O2-moleculen bewegen zich uit het blad in de omringende lucht.
4. Bestudeer de vergelijking voor de celademhaling die hiernaast is afgebeeld. De chemische vergelijking voor de celademhaling is:
C6H12O6 + 6O2==> 6CO2 + 6H2O + energie voor celfuncties
Beantwoord vervolgens de Checking In-vragen hieronder:
Checking In
Laboratoriumonderzoek 3: Biosynthese van nieuwe biomoleculen uit glucose
- Neem je glucosemolecuul en voeg je bij ten minste één ander team.
- Haal de glucosemoleculen uit elkaar. OPMERKING: Je hoeft niet alle bindingen van de atomen los te maken.
- Gebruik de atomen en bindingen van beide teams om een nieuw biomolecuul te bouwen organische koolstofverbindingen die in levende wezens worden geproduceerd; voorbeelden zijn koolhydraten, lipiden (vetten, bodems, wassen), en DNA. . Je biomolecuul kan elke vorm aannemen die je maar wilt. De enige regel die je moet volgen is dat geen enkel “elektronenbruggetje” onverbonden blijft met een ander atoom. Het is mogelijk dat er een paar atomen en bindingen overblijven als je je biomolecuul bouwt. OPMERKING: Je docent kan besluiten om je stikstofatomen te geven. Als je deze atomen gebruikt, kun je eiwitmoleculen bouwen.
- Wanneer je klaar bent met het bouwen van je nieuwe biomoleculen, vergelijk ze dan met andere biomoleculen die door andere teams zijn gemaakt.
Discussie
Kijk naar de andere biomoleculen die de klas heeft gemaakt op basis van de oorspronkelijke glucose-biomoleculen.
- Hoe zijn ze vergelijkbaar? Hoe zijn ze verschillend?
- Als je duizend glucose-biomoleculen had, hoeveel verschillende soorten biomoleculen denk je dat je dan zou kunnen maken? Waarom?
- Stel je voor dat koolstof maar één elektronenverbinding kan vormen, in plaats van vier. Welk effect zou dit hebben op de grootte en diversiteit van de moleculen die je tot nu toe hebt kunnen maken?
De biomassa van alle organismen bestaat voornamelijk uit eiwitten, koolhydraten, nucleïnezuren (DNA, RNA), en lipiden (vetten, oliën en wassen). Glucose en andere koolhydraten bevatten koolstof-, waterstof- en zuurstofatomen. Organismen in de biosfeer bouwen echter miljoenen verschillende biomoleculen die stikstof, fosfor en zwavel bevatten. In feite bestaat 97% van een levend organisme uit slechts zes elementen: koolstof, waterstof, stikstof, zuurstof, fosfor en zwavel of kortweg CHNOPS. Andere elementen zoals magnesium en ijzer zijn ook belangrijk, maar in zeer kleine hoeveelheden. Een gebrek aan een van deze voedingsstoffen in de bodem, die essentieel zijn voor de groei van planten; de belangrijkste bodemvoedingsstoffen zijn stikstof, fosfor, magnesium en zwavel. zal de groei van planten en de opslag van koolstof beperken. In dit onderzoek bestudeer je verschillende Jmol-afbeeldingen van biomoleculen en identificeer je de soorten elementen (atomen) in elk.
- Papier of labnotitieboek
- Jmol-kleurcoderingskaart
- Optioneel: Met de webapp MolView visualisatie kunt u roteren, inzoomen en achtergrondinformatie over biomoleculen vinden.
- Koolstof (zwart of grijs)
- Waterstof (wit)
- Stikstof (blauw)
- Zuurstof (rood)
- Fosfor (oranje)
- Zwavel (geel)
- Magnesium (groen)
- IJzer (brons/koper)
- Maak een grafiek met drie kolommen in je labnotitieboekje of op een apart vel papier. Geef je schema de volgende kopjes:
- Kolom A = Naam van het biomolecuul (bijv. DNA, fructose enz.);
- Kolom B = Type biomolecuul (bijv. koolhydraten, eiwitten enz.);
- Kolom C = Soorten atomen (elementen). Gebruik de eerste letters (C H N O P S Mg I);
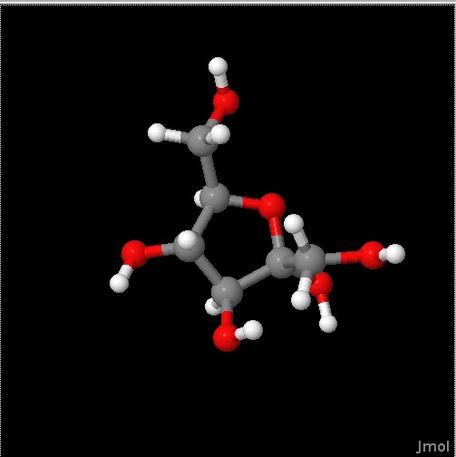
Fructose, een koolhydraat fruitsuiker. Als je fruit eet, zoals appels en sinaasappels, eet je fructose.

DNA, een nucleïnezuur. DNA wordt vaak de blauwdruk van het leven genoemd omdat het de genetische instructies bevat waarmee organismen zichzelf kunnen bouwen en al hun levensactiviteiten kunnen uitvoeren. Zonder DNA wordt een organisme niet gebouwd. Deze visualisatie van DNA vertegenwoordigt slechts een zeer klein segment van een volledige DNA-molecule.
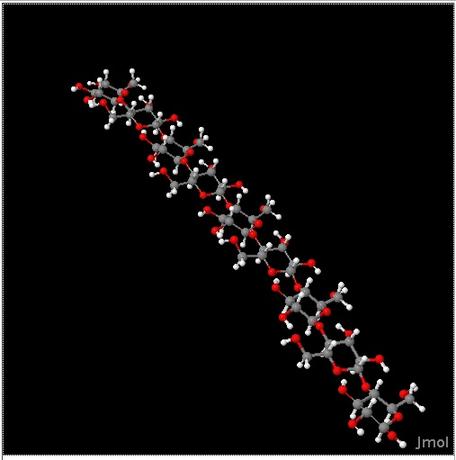
Cellulose, een koolhydraat. De vezelige en houtachtige delen van planten bestaan uit cellulosemoleculen die in lange ketens met elkaar zijn verbonden. Het vezelachtige karakter van cellulose zorgt voor de structuur waardoor planten rechtop kunnen staan. Bomen bestaan voor ongeveer 50% tot 53% uit cellulose, afhankelijk van de boomsoort.

Chlorofyl, een groen pigmentmolecuul. Planten gebruiken dit pigment om energie van de zon te absorberen voor fotosynthese. Chlorofyl is een voorbeeld van een biomolecuul dat niet tot een specifieke groep behoort (d.w.z. koolhydraten, nucleïnezuren, eiwitten, lipiden) Kun je het magnesiumatoom vinden?

Cytochroom C, een plantaardig eiwit. Eiwitten zijn macromoleculen die door alle levende organismen biosynthetisch worden gemaakt en diverse functies hebben die van cruciaal belang zijn voor het leven. Cytochroom c is bijvoorbeeld een eiwit dat planten en andere organismen nodig hebben om de celademhaling uit te voeren. Kun je de zwavelatomen en de twee ijzeratomen in dit cytochroom-eiwitmolecuul vinden?
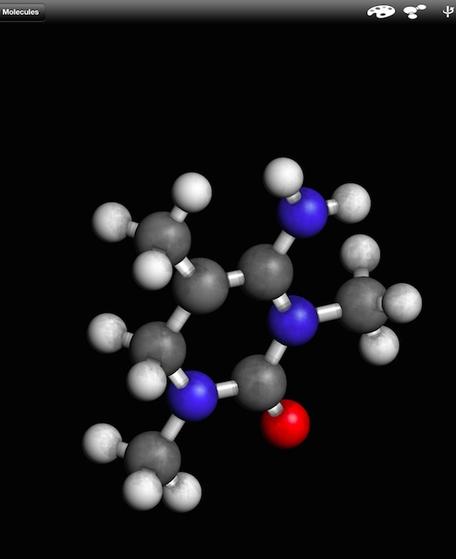
Een aminozuur-onderdeel van een eiwit. Organismen bouwen complete eiwitten op uit honderden aminozuren. Het cytochrome c-molecuul dat hiernaast is afgebeeld, is een compleet eiwit dat is opgebouwd uit vele aminozuren.
Inchecken
Stop en denk na:
1: Leg uit waarom de koolstofatomen in koolstofverbindingen zoals eiwitten en DNA oorspronkelijk afkomstig zijn van CO2-moleculen in de atmosfeer.
2: Leg uit waarom een gebrek aan voedingsstoffen in de bodem (bijv. stikstof, fosfor, zwavel en magnesium) het vermogen van een boom beperkt om te groeien en koolstof op te slaan.
3: Leg uit hoe bomen en alle andere organismen in de biosfeer in staat zijn om miljoenen verschillende configuraties van koolstofverbindingen te maken.
Optionele uitbreidingen
Wil je meer leren over koolstofverbindingen, biomoleculen, CHNOPS, voedingsstoffen in de bodem en meer? Bekijk deze bronnen.
- Onderzoek het nieuwste onderzoek! Er wordt voortdurend nieuw onderzoek gedaan naar de koolstofcyclus, het klimaat en het milieu. U kunt ScienceDaily en Phys.org gebruiken om recent onderzoek te doen naar het verband tussen de koolstofcyclus en andere biochemische cycli door combinaties van de volgende tags te gebruiken: koolstofcyclus, koolstofopslag/sequestratie, CO2-bemesting, bomen, bossen, bodemvoedingsstoffen. Hier is een voorbeeld: Bodemvoedingstoffen beperken vermogen van planten om klimaatverandering te vertragen
- Gebruik MolView om Jmol biomoleculen gemaakt door veel verschillende soorten organismen te onderzoeken.