
Die Ausfällung von Kalziumkarbonat (Kalk) ist ein häufiges Verstopfungsproblem in Mikrobewässerungssystemen. Wasser mit einem pH-Wert von 7,5 oder höher und einem Bikarbonatgehalt von mindestens 2 meq/l (120 ppm) ist anfällig für die Ausfällung von Kalziumkarbonat, wenn vergleichbare Mengen an Kalzium natürlich im System vorhanden sind oder wenn eine kalziumhaltige Verbindung in das System eingespritzt wird.
Ursachen für die Ausfällung von Kalziumkarbonat
Das Ausmaß, in dem Kalziumkarbonat in Wasser bei atmosphärischem Druck auftritt, hängt vom pH-Wert und der Temperatur des Wassers ab. Bei einem pH-Wert von weniger als etwa 6 ist im Wasser hauptsächlich gelöstes Kohlendioxid und eine geringe Menge Kohlensäure vorhanden. Bei pH-Werten zwischen etwa 6,5 und 10 überwiegt Bikarbonat. Bei einem pH-Wert von mehr als 10,5 dominiert das Karbonat-Ion. Zu den Ursachen für Ausfällungen gehören folgende.
- Beim Grundwasser wird durch das Abpumpen der Druck des in den Brunnen fließenden Wassers verringert. Durch diese Verringerung wird gelöstes Kohlendioxidgas freigesetzt, wodurch der pH-Wert des Grundwassers ansteigt, was wiederum zu Kalziumkarbonatausfällungen führen kann.
- Durch Verdunstung erhöht sich die Konzentration von Chemikalien, die in dem im Emittenten verbleibenden Wasser gelöst sind. Wegen seiner geringen Löslichkeit in Wasser fällt Kalziumkarbonat bei der Verdunstung leicht aus.
- Der Grad der Löslichkeit von Kalziumkarbonat nimmt mit steigender Wassertemperatur ab. Die Temperatur des Wassers in Oberflächen-Mikrobewässerungssystemen kann ansteigen, wenn das Wasser durch die Leitungen fließt.
- Die Injektion bestimmter Chemikalien wie Aqua-Ammoniak und Bleichmittel oder die Injektion von kalziumhaltigen Düngemitteln oder Materialien wie Gips kann zu Ausfällungen führen.
Vorbeugung und Behebung von Verstopfungsproblemen
Die Senkung des pH-Werts des Wassers löst vorhandene Ausfällungen von Kalziumkarbonat auf und verhindert die Bildung zusätzlicher Karbonatsalze. Die übliche Behandlung von Kalziumkarbonatausfällungen besteht in der Injektion von Säure, um das Wasser anzusäuern und den pH-Wert auf 7 oder weniger zu senken. Zu den üblichen Säuren, die zu diesem Zweck verwendet werden, gehören Schwefelsäure, Weinsäure und Salzsäure. Andere Säuren wie Zitronensäure und Salpetersäure können ebenfalls verwendet werden, sind aber teurer.
Eine Säure-Dünger-Verbindung wie Harnstoff-Schwefelsäure ist sicherer als eine reine Säure. Die kontinuierliche Injektion von stickstoffhaltigen Säureprodukten kann jedoch im Laufe einer Saison zu Problemen bei Kulturen führen, die empfindlich auf übermäßigen Stickstoffeinsatz reagieren, wie z. B. Äpfel und Weintrauben.
Forscher haben andere Verbindungen wie Phosphonate und Phosphonsäuren untersucht und festgestellt, dass sie die Ausfällung von Calciumcarbonat wirksam verhindern.
Die empfohlenen Behandlungen zur Verhinderung von Verstopfungen sind wie folgt.
- Säure kontinuierlich einspritzen, um den pH-Wert des Wassers zwischen 5 und 7 zu halten.
- Säure intermittierend einspritzen, um den pH-Wert des Wassers für mindestens 30 bis 60 Minuten unter 4 zu halten. Die Häufigkeit der Injektion hängt von der Geschwindigkeit der Karbonatausfällung ab. Bei der Verwendung von druckkompensierenden Emittern sollten Sie sich mit dem Hersteller in Verbindung setzen, bevor Sie den pH-Wert auf 4 oder weniger absenken. Messing und andere nicht rostfreie Metallarmaturen können angefressen werden.
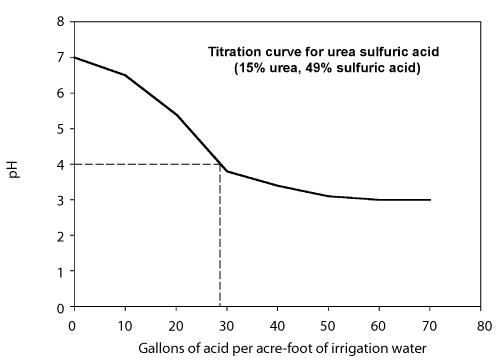
Die Menge an Säure, die benötigt wird, um den pH-Wert auf den gewünschten Wert zu senken, hängt von der Alkalinität des Wassers und dem Ziel-pH-Wert ab. Es gibt zwei Möglichkeiten, die benötigte Säuremenge zu bestimmen. - Erstellen Sie eine Titrationskurve, die zeigt, welche Säuremenge benötigt wird, um den pH-Wert des Wassers auf den gewünschten Wert für ein bestimmtes Bewässerungswasser zu senken. Dies wird normalerweise von einem Labor durchgeführt und erfordert, dass Sie Proben des Wassers und der Säure zur Verfügung stellen. Das Verhalten der Titration hängt von der Alkalinität des Bewässerungswassers ab, so dass die Titrationskurve von einer Wasserquelle zur nächsten variieren kann. Abbildung 8 zeigt eine Titrationskurve unter Verwendung einer Harnstoff-Schwefelsäure-Lösung, die 49 Prozent Schwefelsäure enthält.
- Verwenden Sie einen Versuch-und-Irrtum-Ansatz, indem Sie dem Wasser schrittweise Säure hinzufügen und den pH-Wert messen, und wiederholen Sie den Vorgang, bis Sie den gewünschten pH-Wert erreichen. Lackmuspapier, farbmetrische Testkits für Aquarien und Schwimmbäder und tragbare pH-Meter können zur Bestimmung des pH-Werts des Wassers verwendet werden. Zahlreiche Quellen verkaufen Taschen-pH-Meter; sie erfordern eine regelmäßige Kalibrierung mit Standardlösungen, die ebenfalls gekauft werden können.
Abbildung 8. Titrationskurve für Harnstoff-Schwefelsäure mit 49%iger Schwefelsäure.
Berechnung der Injektionsrate
Wenn Sie die benötigte Säuremenge bestimmt haben, können Sie die Säureinjektionsrate mit Hilfe der folgenden Gleichung berechnen:
IR = (A × Q × 60) ÷ 326.000
wobei
IR = die Injektionsrate in Gallonen pro Stunde (gph)
A = die Gallonen Säure pro acre-foot Wasser, die benötigt werden, um den pH-Wert zu senken
Q = die Durchflussrate des Bewässerungssystems in Gallonen pro Minute (gpm)
Die acre-feet Wasser können durch die Formel Q × T × 60 ÷ 326,000, wobei T die Bewässerungszeit in Stunden ist.
Beobachten Sie den pH-Wert des Wassers während des Injektionsvorgangs, um sicherzustellen, dass er nicht wesentlich unter 4 sinkt. Alle Wässer werden durch die darin enthaltenen Salze unterschiedlich “gepuffert”; ein Wasser kann 10 gph benötigen, während ein anderes nur 2 gph benötigt.
Beispiel
Berechnen Sie die Injektionsrate, die erforderlich ist, um den pH-Wert mit einer Harnstoff-Schwefelsäure (49%) auf 4 zu senken. Die Abbildung oben zeigt die Titrationskurve. Die Durchflussmenge des Systems beträgt 1.000 Gallonen pro Minute.
Schritt 1. Aus der Titrationskurve geht hervor, dass 26 Gallonen Harnstoff-Schwefelsäure pro acre-foot Wasser benötigt werden, um den pH-Wert auf 4 zu senken.
Schritt 2.
IR = (26 × 1.000 × 60) ÷ 326.000 = 4,8 gph
Sicherheitsmaßnahmen
- Sie dürfen Säure und Chlor nicht direkt mischen. Dadurch bildet sich giftiges Chlorgas.
- Fügen Sie der Säure kein Wasser hinzu. Fügen Sie stattdessen immer Säure zu Wasser hinzu.