- Wat is Lutetium
- Waar wordt lutetium gevonden
- Geschiedenis
- Lutetium Identificatie
- Eigenschappen en kenmerken van lutetium
- Algemene eigenschappen
- Fysische eigenschappen
- Chemische eigenschappen
- Atomaire gegevens van lutetium (element 71)
- Waarvoor wordt het gebruikt
- Mogelijke gevolgen voor de gezondheid
- Belangrijke feiten
- Kostprijs van Lutetium
Wat is Lutetium
Lutetium (uitgesproken als loo-TEE-shee-em) is een zilverachtig, hard, dicht zeldzaam aardmetaal geclassificeerd als een lanthanide en weergegeven door het chemische symbool Lu . Het is het laatste chemische element dat tot de lanthanidereeks behoort, met als meest natuurlijk voorkomende stabiele isotoop 175Lu (97,4% abundantie). Een andere langlevende radioactieve isotoop 176Lu heeft een halveringstijd van 3,78 X 1010 jaar.

Lutetium Symbool
Waar wordt lutetium gevonden
Lutetium wordt, net als andere lanthaniden, commercieel gewonnen uit het mineraal monaziet . Aangezien het in kleine hoeveelheden (ongeveer 0,003%) in monaziet voorkomt, kan de extractie ervan moeilijk zijn en wordt gedaan door reductie van watervrij fluoride met behulp van calciummetaal. Hoewel het element wordt gevonden in sporenhoeveelheden in bijna alle mineralen die yttrium bevatten, kunnen ze worden beschouwd als natuurlijke bronnen van lutetium . De top 3 van landen die lutetium produceren zijn China, Rusland en Maleisië, terwijl de top 3 van landen die reserves hebben China, GOS-landen en de VS zijn.

Lutetium
Geschiedenis
Oorsprong van zijn naam: De naam van het element is afgeleid van het Romeinse woord ‘Lutetia’, de oude naam voor de Franse stad Parijs .
Wie ontdekte het: Hoewel de Franse scheikundige Georges Urbain, de Amerikaanse scheikundige Charles James, en de Oostenrijkse wetenschapper Carl Auer von Welsbach onafhankelijk van elkaar het element ontdekten, ging de eer van de ontdekking naar Urbain aangezien hij de eerste was die de resultaten rapporteerde .
Wanneer en hoe werd het ontdekt
Het mineraal gadoliniet of yttrium, ontdekt in 1794, is de bron geweest van yttria, terbia, erbia, en andere zeldzame aardmetalen . De Zwitserse chemicus Jean Charles Marignac scheidde erbia in twee componenten waaronder ytterbia en erbia, waarvan ytterbia werd verondersteld een verbinding van ytterbium .
In 1907, Georges Urbain tijdens het experimenteren aan de Sorbonne in Parijs met succes geïsoleerd ytterbium in twee elementen, die hij de naam lutecium en neoytterbium . Deze elementen werden echter later door chemici omgedoopt tot respectievelijk lutetium en ytterbium . Carl Auer von Welsbach scheidde het element van ytterbia en noemde het cassipoium naar het circumpolaire sterrenbeeld Cassiopeia . Charles James ook met succes gewonnen het element aan de Universiteit van New Hampshire .
Hoewel het moeilijk te bereiden is, werd het zuivere lutetium metaal geproduceerd in 1953 .
Lutetium Identificatie |
|||
| Atoomnummer | 71 | ||
| CAS nummer | 7439-94-.3 | ||
| Positie in het periodiek systeem | Groep | Periode | Blok |
| Lanthaniden | 6 | f | |

Locatie van lutetium in het periodiek systeem
Eigenschappen en kenmerken van lutetium
Algemene eigenschappen |
||||||||||||||||
| Atomaire massa | 174.967 amu | |||||||||||||||
| Relatieve atoommassa | 174.967 | |||||||||||||||
Fysische eigenschappen |
||||||||||||||||
| Kleur | Zilverwit | |||||||||||||||
| Smeltpunt/vriespunt | 1663 °C, 3025 °F | |||||||||||||||
| kookpunt | 3402 °C, 6156 °F | |||||||||||||||
| dichtheid | 9.84 g cm-3 | |||||||||||||||
| Staat van de materie bij kamertemperatuur (vast/vloeibaar/gas) | Vast | |||||||||||||||
| Hardheid | ||||||||||||||||
| – Brinell | 893 MPa | |||||||||||||||
| – Mohs | 2.6 | |||||||||||||||
| – Vickers | 1160 MPa | |||||||||||||||
| Elektrisch geleidingsvermogen | 1.8X106 S/m | |||||||||||||||
| Thermische (warmte) geleidbaarheid | 16 W/(m K) | |||||||||||||||
| Specifieke warmte | 154 J kg-1 K-1 | |||||||||||||||
| Bulk modulus | 47.6 GPa | |||||||||||||||
| Shear modulus | 27.2 GPa | |||||||||||||||
| Young’s modulus | 68.6 GPa | |||||||||||||||
| Dampdruk | ||||||||||||||||
| – Temperatuur (K) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | |||||
| – Druk (Pa) | – | – | – | 3.28X 10-11 | 1.59X 10-7 | 6.79X 10-5 | 6.28X 10-3 | 0.211 | 3.18 | 26.7 | – | |||||
Chemische eigenschappen |
||||||||||||||||
| Oxidatietoestanden | 3 | |||||||||||||||
| Isotopen | Isotoop | Massa | Beschikbaarheid | Half-leven | Vervalwijze | |||||||||||
| 175Lu | 174.941 | 97,40 | – | – | ||||||||||||
| 176Lu | 175,943 | 2,60 | 3.73 X 1010 jaar | β-
β+ EC |
||||||||||||
Atomaire gegevens van lutetium (element 71)
| Valentie elektronen | 3 | |||||||
| kwantumgetallen | 2D3/2 | |||||||
| Elektronenconfiguratie (edelgasconfiguratie) | 4f145d16s2 | |||||||
| Atomische structuur | ||||||||
| – Aantal elektronen | 71 | |||||||
| – Aantal neutronen | 104 | |||||||
| – Aantal protonen | 71 | |||||||
| – Atoomstraal | ||||||||
| – Atoomstraal | 2.24 Å | |||||||
| – Covalente straal | 1.74 Å | |||||||
| Electronegativiteit (Pauling-schaal) | 1.0 | |||||||
| Electronenaffiniteit | 32.81 kJ mol-1 | |||||||
| Ionisatie-energie (kJ mol-1) | 1e | 2e | 3e | 4e | 5e | 6e | 7e | 8e |
| 523.516 | 1341.1 | 2022.275 | 4365.96 | 6445.2 | – | – | – | |
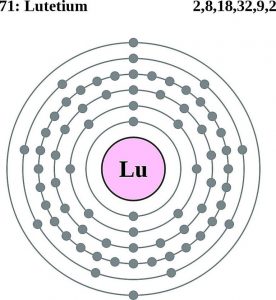
Lutetium elektronenconfiguratie (Bohr model)
Waarvoor wordt het gebruikt
Het heeft weinig praktisch nut buiten wetenschappelijk onderzoek. Hieronder volgen enkele commerciële toepassingen van lutetium:
- Het kan worden gebruikt als katalysator voor het kraken van aardolieproducten in olieraffinaderijen.
- Radio-immunotherapie met lutetium-177-dotataat wordt gebruikt als een vorm van kankerbehandeling terwijl lutetium-176 wordt gebruikt voor radiometrische datering van meteorieten.
- Lutetiumoxyorthosilicaat wordt gebruikt in PET (positron emissie tomografie) detectoren voor het uitvoeren van een medische scan om een 3D-beeld van de cellulaire activiteit in het lichaam te creëren.
Mogelijke gevolgen voor de gezondheid
Lutetium heeft een lage toxiciteit en geen bekende biologische functies in het menselijk lichaam ; hoewel men denkt dat het de stofwisseling kan helpen stimuleren. Het wordt ook verondersteld een explosiegevaar te zijn.
Belangrijke feiten
- Lutetium is het hardste en dichtste element in de lanthanidegroep.
- Het bestaat in verbindingen over het algemeen in zijn driewaardige toestand, Lu3+.
- Het element wordt soms visueel afgebeeld door een afbeelding op basis van het wapen van Parijs.
Kostprijs van Lutetium
De zuivere vorm van lutetium kost ongeveer $350 per gram , maar het kost ongeveer $7.000 per 100 gram in bulk .
- http://www.rsc.org/periodic-table/element/71/lutetium
- https://education.jlab.org/itselemental/ele071.html
- https://www.livescience.com/38425-lutetium.html
- https://www.webelements.com/lutetium/isotopes.html
- https://www.chemicool.com/elements/lutetium.html
- http://periodictable.com/Elements/071/data.html
- http://web.newworldencyclopedia.org/entry/Lutetium
- https://hobart.k12.in.us/ksms/PeriodicTable/lutetium.htm