Vad är Curium
Curium (uttalat som KYOOR-ee-em) är en radioaktiv metall som tillhör familjen av aktinidmetaller och betecknas med den kemiska symbolen Cm .

Kuriumsymbol
Kuriumisotoper
Den har 15 isotoper varav den mest stabila är Curium-247 med en halveringstid på cirka 15 600 000 år som genomgår alfa- sönderfall för att bilda plutonium-243 .
Historia
Namnets ursprung: Det är uppkallat efter de välkända vetenskapsmännen Pierre Curie och Marie Curie, som upptäckte radium.
Vem upptäckte det: Pierre Curie och Marie Curie: Elementet syntetiserades av forskargruppen Glenn Seaborg, Albert Ghiorso och Ralph James .

Curium
Var upptäcktes curium
1944 bombarderade Seaborg, Ghiorso och James plutonium 239 med alfapartiklar i en cyklotron i Berkeley, Kalifornien. Det skickades sedan till Metallurgical Laboratory vid University of Chicago för att isolera och analysera det nya grundämnet. Den 11 november 1945, efter andra världskrigets slut, avslöjades upptäckten av Seaborg i ett radioprogram där han hade bjudits in som gästforskare. Den blev officiell veckan därpå.
Elementets klassificering och position i det periodiska systemet
| Gruppnummer | Okänd |
| Period | 7 |
| Block | f |
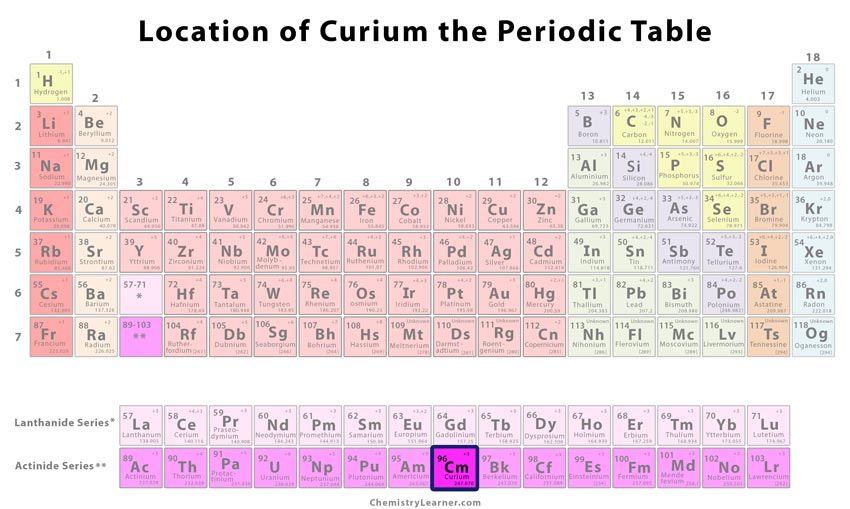
Curiums placering i det periodiska systemet
Curiums egenskaper
Allmänna egenskaper |
|||
| Relativ atommassa | 247 | ||
| Atomvikt | 247 atommasseenheter | ||
Fysikaliska egenskaper |
|||
| Färg/utseende | Silvervitt | ||
| Glans | Okänd | ||
| Göringsgrad | Okänd | ||
| Smältpunkt/fryspunkt | 1345 °C (2453°F) | ||
| Kokpunkt | Okänd | ||
| Täthet | 13.51 g/cm3 | ||
| Materialtillstånd vid rumstemperatur (fast/flytande/gas) | Fasta | ||
| Hårdhet | Okänd | ||
| Elektrisk ledningsförmåga | Okänd | ||
| Termal (värme)konduktivitet | Okänd | ||
| Specifik värme | Okänd | ||
Kemiska egenskaper |
|||
| Brandfarlighet | Okänd | ||
| Oxidationstillstånd | 4 | 3 | |
Atomdata för Curium
| Atomnummer | 96 | ||||||
| Valenceelektroner | 2 | ||||||
| Kvantantal | |||||||
| – n | 5 | ||||||
| – ℓ | 3 | ||||||
| – m ℓ | -3 | ||||||
| – m s | -1/2 | ||||||
| Elektronkonfiguration (ädelgaskonfiguration) | 5f76d17s2 | ||||||
| Atomstruktur | |||||||
| – Antal elektroner | 99 | ||||||
| – Antal neutroner | 151 | ||||||
| – Antal protoner | 99 | ||||||
| Atomens radie | |||||||
| – Atomens radie | 2.45 Å | ||||||
| – Kovalent radie | 1.68 Å | ||||||
| Elektronegativitet | Okänd | ||||||
| Ioniseringsenergi
(kJmol-)1) |
1st | 2nd | 3rd | 4th | 5th | 6th | 7th |
| 578.082 | – | – | – | – | – | – | |
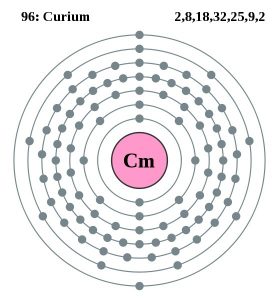
Curium Bohr-modellen
Vad används curium till
Då det inte finns naturligt i jordskorpan, har det radioaktiva grundämnet endast använts i grundforskningsstudier på grund av dess begränsade laboratorieproduktion. Dessutom reagerar det inte med andra föreningar. Curium-244 kan dock vara tillämpligt som en kraftkälla för att driva radioisotopiska termoelektriska generatorer som används i rymdfarkoster .
Interessanta fakta om curium
- Curium-244 har använts i Alpha Proton X-ray Spectrometer för att detektera närvaron av kemiska element i atmosfären och föreningar på stenytan på Mars
- Elementet tros glöda rött i mörkret på grund av sin radioaktiva natur
Hur mycket kostar curium
Det radioaktiva elementet är inte kommersiellt tillgängligt utanför laboratorieproduktionen.