Hvad er Curium
Curium (udtales som KYOOR-ee-em) er et radioaktivt metal, der tilhører familien af actinidmetaller og betegnes med det kemiske symbol Cm .

Curium Symbol
Curium Isotoper
Det har 15 isotoper, hvoraf den mest stabile er Curium-247 med en halveringstid på ca. 15.600.000 år, der undergår alfa-henfald til plutonium-243 .
Historie
Original af dets navn: Det er opkaldt efter de kendte videnskabsmænd Pierre Curie og Marie Curie, der opdagede radium.
Hvem opdagede det: Grundstoffet blev syntetiseret af forskerholdet Glenn Seaborg, Albert Ghiorso og Ralph James.

Curium
Hvor blev Curium opdaget
I 1944 bombarderede Seaborg, Ghiorso og James plutonium-239 med alfapartikler i en cyklotron i Berkeley, Californien. Derefter blev det sendt til det metallurgiske laboratorium på University of Chicago for at isolere og analysere det nye grundstof. Den 11. november 1945, efter afslutningen af 2. verdenskrig, blev opdagelsen afsløret af Seaborg i et radioprogram, hvor han var blevet inviteret som gæsteforsker. Det blev officielt bekendtgjort i den følgende uge.
Elementets klassificering og placering i det periodiske system
| Gruppenummer | Ukendt |
| Periode | 7 |
| Blok | f |
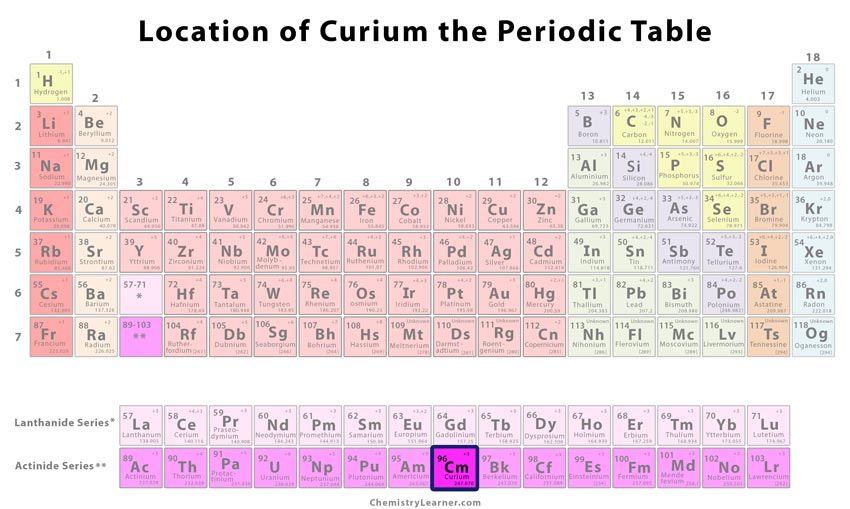
Curiums placering i det periodiske system
Egenskaber for curium
Almene egenskaber |
|||
| Relativ atommasse | 247 | ||
| Atommasse | 247 atommasseenheder | ||
Fysiske egenskaber |
|||
| Farve/udseende | Sølvhvid | ||
| Glans | Ukendt | ||
| Glødning | Ukendt | ||
| Smeltepunkt/frysepunkt | 1345 °C (2453°F) | ||
| Kogningspunkt | Ukendt | ||
| Densitet | 13.51 g/cm3 | ||
| Materietilstand ved stuetemperatur (fast/flydende/gas) | Fast | ||
| Hårdhed | Ukendt | ||
| Elektrisk ledningsevne | Ukendt | ||
| Termisk (varme) ledningsevne | Ukendt | ||
| Specifik varme | Ukendt | ||
Kemiske egenskaber |
|||
| Brandfarlighed | Ukendt | ||
| Oxidationstilstande | 4 | 3 | |
Atomdata for Curium
| Atometrisk nummer | 96 | ||||||
| Valenceelektroner | 2 | ||||||
| Kvantital | |||||||
| – n | 5 | ||||||
| – ℓ | 3 | ||||||
| – m ℓ | -3 | ||||||
| – m s | -1/2 | ||||||
| Elektronkonfiguration (ædelgaskonfiguration) | 5f76d17s2 | ||||||
| Atomstruktur | |||||||
| – Antal elektroner | 99 | ||||||
| – Antal neutroner | 151 | ||||||
| – Antal protoner | 99 | ||||||
| Atomets radius | |||||||
| – Atomets radius | 2.45 Å | ||||||
| – Kovalent radius | 1.68 Å | ||||||
| Elektronegativitet | Ukendt | ||||||
| Ioniseringsenergi
(kJmol-1) |
1st | 2nd | 3rd | 4th | 5th | 6th | 7th |
| 578.082 | – | – | – | – | – | – | |
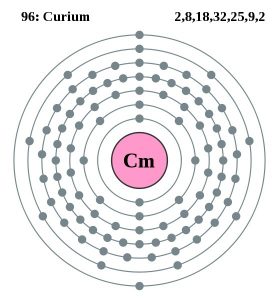
Curium Bohr-modellen
Hvad bruges curium til
Da det ikke findes naturligt i jordskorpen, er det radioaktive grundstof kun blevet anvendt i grundforskningsundersøgelser på grund af dets begrænsede laboratorieproduktion. Desuden reagerer det ikke med andre forbindelser. Curium-244 kan imidlertid være anvendeligt som energikilde til drift af radioisotopiske termoelektriske generatorer, der anvendes i rumfartøjer .
Interessante fakta om curium
- Curium-244 er blevet brugt i Alpha Proton X-ray Spectrometer til at påvise tilstedeværelsen af kemiske elementer i atmosfæren og stenoverfladens forbindelser på Mars
- Elementet menes at gløde rødt i mørket på grund af dets radioaktive natur
Hvor meget koster curium
Det radioaktive element er ikke kommercielt tilgængeligt uden for laboratorieproduktion.