
Precipitatie van calciumcarbonaat (kalk) is een veel voorkomend verstoppingsprobleem in microirrigatiesystemen. Water met een pH van 7,5 of hoger en een bicarbonaatgehalte van ten minste 2 meq/l (120 ppm) is gevoelig voor calciumcarbonaatneerslag als vergelijkbare calciumgehaltes van nature in het systeem aanwezig zijn of als een verbinding die calcium bevat in het systeem wordt geïnjecteerd.
Oorzaken van calciumcarbonaatneerslag
De mate waarin calciumcarbonaat bij atmosferische druk in water voorkomt, hangt af van de pH en de temperatuur van het water. Bij pH-waarden van minder dan ongeveer 6 komen in water vooral opgelost kooldioxide en een kleine hoeveelheid koolzuur voor. Bij pH-waarden tussen ongeveer 6,5 en 10 is bicarbonaat dominant. Bij pH-waarden groter dan ongeveer 10,5, overheerst het carbonaation. De oorzaken van neerslag zijn onder meer de volgende.
- Voor grondwater vermindert door pompen de druk van het water als het in de put stroomt. Door deze verlaging komt opgelost kooldioxidegas vrij, waardoor de pH van het grondwater stijgt, en dat kan op zijn beurt calciumcarbonaatneerslag veroorzaken.
- Doordamping verhoogt de concentratie van chemicaliën die zijn opgelost in het water dat in de uitstromer achterblijft. Door zijn geringe oplosbaarheid in water slaat calciumcarbonaat tijdens de verdamping gemakkelijk neer.
- De mate van oplosbaarheid van calciumcarbonaat daalt naarmate de watertemperatuur stijgt. De temperatuur van het water in oppervlakte micro-irrigatiesystemen kan stijgen naarmate het water door de lateralen stroomt.
- De injectie van bepaalde chemicaliën zoals aqua-ammoniak en bleekwater of de injectie van calciumhoudende meststoffen of materialen zoals gips kan neerslag veroorzaken.
Voorkomen en verhelpen van verstoppingsproblemen
Verlaging van de pH-waarde van het water lost eventuele bestaande neerslagen van calciumcarbonaat op en voorkomt de vorming van extra carbonaatzouten. De gebruikelijke behandeling voor calciumcarbonaatneerslag is het inspuiten van zuur om het water aan te zuren, waarbij de pH tot 7 of minder wordt verlaagd. Veel gebruikte zuren voor dit doel zijn zwavelzuur, zoutzuur, en zoutzuur. Andere zuren zoals citroenzuur en salpeterzuur kunnen worden gebruikt, maar zij zijn duurder.
Een zuur-meststofverbinding zoals ureum-zwavelzuur is veiliger om te gebruiken dan een zuiver zuur. De voortdurende injectie van stikstofhoudende zure producten kan echter in de loop van een seizoen problemen veroorzaken voor gewassen die gevoelig zijn voor overmatige stikstoftoepassingen, zoals appels en wijndruiven.
Onderzoekers hebben andere verbindingen geëvalueerd, zoals een fosfonaat en fosfonzuurmaterialen, en hebben vastgesteld dat ze effectief zijn in het voorkomen van calciumcarbonaatneerslag.
De aanbevolen behandelingen voor het voorkomen van verstopping zijn als volgt.
- Injecteer continu zuur om de pH van het water tussen 5 en 7 te houden.
- Injecteer zuur met tussenpozen om de pH van het water gedurende ten minste 30 tot 60 minuten onder 4 te houden. De injectiefrequentie is afhankelijk van de snelheid waarmee carbonaatneerslag optreedt. Wanneer u drukcompenserende emitters gebruikt, dient u contact op te nemen met de fabrikant voordat u de pH verlaagt tot 4 of minder. Messing en alle andere niet roestvrije metalen fittingen kunnen gaan pitten.
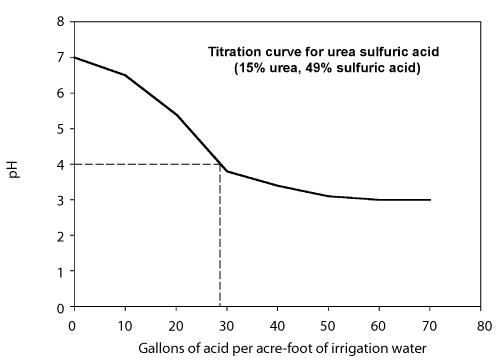
De hoeveelheid zuur die nodig is om de pH te verlagen tot het gewenste niveau hangt af van de alkaliteit van het water en de beoogde pH. Twee benaderingen kunnen worden gebruikt om de benodigde hoeveelheid zuur te bepalen. - Ontwikkel een titratiecurve die de hoeveelheid zuur laat zien die nodig is om de pH van het water te verlagen tot een gewenste waarde voor een bepaald irrigatiewater. Dit wordt gewoonlijk door een laboratorium gedaan en vereist dat u monsters van het water en het zuur levert. Het gedrag van de titratie is afhankelijk van de alkaliteit van het irrigatiewater, zodat de titratiecurve van waterbron tot waterbron kan verschillen. Figuur 8 toont een titratiecurve met behulp van een ureum-zwavelzuuroplossing met 49 procent zwavelzuur.
- Gebruik een trial-and-error-benadering door in stappen zuur aan het water toe te voegen en de pH te meten, en dit te herhalen tot u de gewenste pH-waarde hebt bereikt. Lakmoespapier, colormetrische testkits voor aquaria en zwembaden, en draagbare pH-meters kunnen worden gebruikt om de pH-waarde van het water te bepalen. Talrijke bronnen verkopen zak pH-meters; zij vereisen periodieke kalibratie met behulp van standaardoplossingen die ook kunnen worden gekocht.
Figuur 8. Titratiecurve voor ureumzwavelzuur met 49% zwavelzuur.
Berekening van de injectiesnelheid
Als u eenmaal hebt bepaald hoeveel zuur u nodig hebt, kunt u de injectiesnelheid van het zuur berekenen met behulp van de volgende vergelijking:
IR = (A × Q × 60) ÷ 326.000
waar
IR = de injectiesnelheid in gallons per uur (gph)
A = de gallons zuur per acre-foot water die nodig zijn om de pH te verlagen
Q = het debiet van het irrigatiesysteem in gallons per minuut (gpm)
De acre-feet water kan worden bepaald met de formule Q × T × 60 ÷ 326,000, waarbij T de ingestelde irrigatietijd in uren is.
Controleer de pH van het water tijdens het inspuitproces om ervoor te zorgen dat deze niet veel onder 4 komt. Alle wateren worden verschillend “gebufferd” door de zouten die zij bevatten; voor het ene water kan 10 gph nodig zijn, terwijl voor het andere slechts 2 gph nodig is.
Voorbeeld
Bereken de injectiesnelheid die nodig is om de pH te verlagen tot 4 met behulp van een ureum-zwavelzuur (49%). Bovenstaande figuur is de titratiecurve. Het debiet van het systeem is 1.000 gallons per minuut.
Stap 1. Uit de titratiecurve blijkt dat 26 gallon ureum-zwavelzuur per acre-voet water nodig is om de pH tot 4 te verlagen.
Stap 2.
IR = (26 × 1.000 × 60) ÷ 326.000 = 4,8 gph
Veiligheidsmaatregelen
- Zuur en chloor niet rechtstreeks mengen. Dit veroorzaakt de vorming van giftig chloorgas.
- Voeg geen water bij zuur. Voeg in plaats daarvan altijd zuur aan water toe.