Più che semplici flash e floaters
Autori: Nicole C. Morrow BS, Anthony T. Chung, MD, Michael Wall, MD
Posted June 24, 2019
Introduzione
Le fotopsie (cioè i flash) sono un comune sintomo di presentazione nella clinica oftalmologica. Anche se la maggior parte delle fotopsie sono di origine retinica, caratterizzare l’aspetto, l’insorgenza e le caratteristiche associate è fondamentale per determinare la causa di queste importanti ma diverse descrizioni di “luci lampeggianti”. Il seguente tutorial discute le varie fonti di fotopsia: trazione vitreoretinica, emicranie oculari, degenerazione maculare legata all’età, diabete, flusso sanguigno cerebrale, allucinazioni visive, retinopatia associata al cancro, fenomeno entoptico, fosfeni e disfotopsie associate a lenti.
Discussione
Distacco del vitreo posteriore, lacerazioni retiniche e/o distacco della retina
Il distacco del vitreo posteriore (PVD) è una causa comune di floaters e fotopsie nella popolazione generale, rappresentando circa il 40% dei pazienti che presentano questi sintomi. I floaters (Figura 1) sono tipicamente dovuti a cellule o detriti che galleggiano nel vitreo e che proiettano ombre sulla retina. I pazienti spesso descrivono anche di vedere un grande floater opaco come il vitreo si separa da intorno alla testa del nervo ottico. All’esame clinico, questa separazione del vitreo dal nervo ottico circolare può essere vista come un anello di Weiss.
Le fotopsie si verificano quando il vitreo tira sulla retina. La tensione del vitreo sulla retina provoca l’incendio delle cellule retiniche e porta alla percezione di lampi di luce. Questi lampi durano tipicamente meno di un secondo e sono descritti come una striscia di luce o un flash di macchina fotografica nella periferia. La forma del lampo è solitamente curvilinea a causa del bordo della trazione vitreoretinica. Le fotopsie possono verificarsi unilateralmente o bilateralmente, ma i flash bilaterali si verificano tipicamente in momenti diversi in ciascun occhio.
Le lacerazioni retiniche possono anche causare floaters e lampi di luce in periferia. Le lacerazioni retiniche dovute a trazione da trauma o PVD sono tipicamente a ferro di cavallo e, se abbastanza grandi, il vitreo entra nello spazio sottoretinico causando un distacco retinico regmatogeno (RRD). L’intervento chirurgico è necessario per gli RRD, che sono associati a una diminuzione persistente e progressiva della visione che i pazienti hanno tipicamente descritto come una tenda o un velo nel loro campo visivo. Differenziare tra un PVD acuto e le lacerazioni retiniche può essere difficile basandosi solo sulla storia. Hollands et al. hanno scoperto che il 14% dei pazienti che presentano floaters e/o flash e una diagnosi di PVD hanno anche una lacerazione retinica; tuttavia, se non c’è un declino soggettivo dell’acuità visiva, questo rischio diminuisce all’8,9%. Al contrario, se il paziente riferisce una diminuzione soggettiva dell’acuità visiva o si vede un’emorragia vitreale, allora il rischio di una lacerazione aumenta al 45% e al 62%, rispettivamente. Se si nota un pigmento vitreo (cioè il segno di Shafer), allora il rischio di una lacerazione retinica arriva all’88%. Nei pazienti con diagnosi di PVD senza una lacerazione retinica, il 3,4% ha avuto una lacerazione retinica entro sei settimane dalla loro presentazione iniziale. Pertanto, tutti i pazienti dovrebbero ripetere l’esame del fondo dilatato entro 4-6 settimane dalla presentazione iniziale.

Figura 1. Illustrazione di floaters tipici di un distacco posteriore del vitreo
Emicrania oculare
L’emicrania è una sindrome di mal di testa ricorrente, frequentemente unilaterale, spesso con un prodromo di fenomeni visivi positivi bilaterali. Una “emicrania classica” è descritto da avere questo prodromo (cioè, aura) che dura circa 15 a 30 minuti e seguita da un mal di testa e sintomi correlati che possono persistere per ore. Anche se il fenomeno visivo si verifica tipicamente bilateralmente, le fotopsie possono apparire più grandi in un occhio che nell’altro. I sintomi visivi possono verificarsi con ogni emicrania un individuo ha o può accadere solo una volta. L’emicrania e le auree non sono completamente compresi, e c’è molto dibattito intorno ai loro meccanismi sottostanti. Una teoria principale è che le emicranie sono causate da disturbi nel flusso sanguigno cerebrale e un’onda di attività neuronale depressa si muove lentamente attraverso il cervello; questo processo di solito inizia nel lobo occipitale e si diffonde anteriormente. Un’aura emicranica è probabilmente il risultato dell’onda iniziale di alta attività neuronale legata alla depressione di diffusione precedentemente descritta, seguita da un’inibizione dell’attività. Le aure possono manifestarsi come piccole luci luminose, punti ciechi, visione statica/nebbiosa, e/o disturbi visivi complessi. In genere, le aure iniziano prima del mal di testa come uno scotoma scintillante centrale a forma di mezzaluna che si espande verso l’esterno ed è circondato da lampi o zigzag di luce. In un’emicrania retinica, il paziente sperimenta una diminuzione della vista o una completa cecità in un occhio senza uno scotoma scintillante; questo è dovuto al vasospasmo della circolazione retinica o dell’arteria oftalmica. La vista in un’emicrania retinica ritorna prontamente alla normalità. Una forma molto rara di emicrania è l’emicrania oftalmoplegica, che può causare una paralisi temporanea di uno dei tre nervi cranici coinvolti nel movimento oculare (CN III, CN IV e CN VI) ma non è associata a fotopsie.


Figura 2. Illustrazioni di scotomi scintillanti tipici delle emicranie oculari. Questi possono produrre una varietà di fenomeni visivi tra cui zig zag e/o immagini colorate “statiche”.
Degenerazione maculare senile
La degenerazione maculare senile (AMD) non essudativa (cioè secca) causa una graduale perdita visiva centrale bilaterale senza dolore correlato. I pazienti riferiscono una diminuzione della visione centrale e metamorfopsia, ma di solito non hanno fotopsie associate alla AMD secca. AMD essudativa (cioè neovascolare o umida), tuttavia, è un’altra causa comune di fotopsie e la seconda causa più comune in una serie di casi riportati. Circa il 50% degli individui con AMD essudativa riferiscono di sperimentare ripetuti flash localizzati al centro che durano da alcuni secondi a pochi minuti. Questi flash sono tipicamente descritti come tremolii, pulsazioni, luci scintillanti, luci simili a serpenti, luci rotanti, girandole o cerchi. Queste luci sono più comunemente di colore bianco, ma le persone hanno riferito di aver visto luci blu, argento, oro o di più colori. La probabilità delle fotopsie riportate aumenta con l’aumentare dell’area delle membrane neovascolari. A differenza delle fotopsie di PVD, che sono stimolate dall’interfaccia retina-vitreo interno, le fotopsie da AMD essudativa si verificano dall’accumulo di liquido che stimola gli strati esterni della retina. Differenziare tra i due può a volte essere difficile prima dell’esame; tuttavia, i flash centrali sono molto più comuni con AMD e i flash periferici sono più comuni con PVD
Diabete
Il diabete può causare una moltitudine di cambiamenti visivi. La progressione della malattia può portare alla retinopatia diabetica proliferativa o non proliferativa. I pazienti diabetici con uno stretto controllo dei loro livelli di glucosio nel sangue possono ridurre significativamente il loro rischio di sviluppare la retinopatia diabetica. Tuttavia, la maggior parte dei pazienti svilupperà la retinopatia diabetica dopo 15 anni con la malattia. La retinopatia diabetica non proliferativa è caratterizzata da microaneurismi, emorragie puntiformi, essudati duri, macchie di cotone idrofilo ed edema maculare. I pazienti con edema maculare si presentano comunemente con una diminuzione dell’acuità visiva. Tuttavia, la maggior parte dei pazienti rimarrà asintomatica fino a raggiungere la fase proliferativa. La retinopatia diabetica proliferativa si verifica quando l’ischemia prolungata della retina innesca la formazione di nuovi vasi e di tessuto fibroso. La nuova crescita fibrosa forma una cicatrice contratta all’interfaccia vitreoretinica e può causare fotopsie poiché il tessuto si contrae. Questa contrazione può portare a distacchi retinici trazionali (TRD) con una potenziale emorragia vitreale a causa della fragilità di questi nuovi vasi. I pazienti con TRD possono segnalare floaters, photopsias, e/o una tenda sul loro campo visivo che è simile ai distacchi retinici regmatogeni. Le complicazioni della retinopatia diabetica proliferativa possono provocare una perdita permanente della vista. In un piccolo studio, i pazienti con ipoglicemia che erano diabetici insulino-dipendenti hanno riportato fotopsie bilaterali che sono cessate quando il loro glucosio è tornato a livelli normali. Si sono verificati in ambienti chiari o scuri e sono stati descritti come sfarfallii bianchi o cerchi.
Insufficienza basilare vertebrale
L’insufficienza basilare vertebrale causa un ridotto flusso di sangue alla parte posteriore del cervello ed è associata all’invecchiamento. Questa diminuzione del flusso sanguigno causa un’ischemia in quest’area e porta a fotopsie bilaterali, che sono descritte come lampi interrotti che durano da secondi a minuti. Inoltre, l’insufficienza basale vertebrale è associata a vertigini, capogiri, diplopia, cecità, debolezza e atassia. I pazienti possono avere simili lampi di luce e appannamento della vista, simili a un’emicrania visiva; tuttavia, questi sintomi non continuano per così tanto tempo e non si verificano prima di un mal di testa.
Allucinazioni di rilascio (sindrome di Charles Bonnet)
Le allucinazioni di rilascio sono caratterizzate come allucinazioni visive derivanti da danni alle vie visive, unilateralmente o bilateralmente, in individui con cognizione intatta. I pazienti descrivono di vedere forme multicolori, griglie, volti, persone e fiori che durano da secondi a minuti. Il meccanismo sottostante è poco compreso. La teoria più ampiamente accettata è la teoria della deprivazione sensoriale, che afferma che la perdita di stimoli visivi alla corteccia visiva aumenta l’eccitabilità dei neuroni. Questo aumento dell’attività neuronale porta all’accensione casuale dei neuroni con poco o nessun stimolo, da cui il nome allucinazioni di rilascio . Questo è supportato dall’alta prevalenza negli individui con acuità visiva più scarsa e dopo il patch post-operatorio dell’occhio. La prevalenza della sindrome di Charles Bonnet aumenta negli individui con acuità visiva più scarsa bilateralmente .
Retinopatia associata al cancro
La retinopatia associata al cancro è una rara malattia autoimmune in cui il corpo sviluppa autoanticorpi contro antigeni retinici . Recoverin e a-enolase sono gli antigeni retinici più comuni verso i quali si sviluppano gli autoanticorpi. Questi anticorpi si sviluppano tipicamente in presenza di malignità, più frequentemente il cancro del polmone a piccole cellule. I pazienti che sviluppano questa malattia spesso presentano una diminuzione dell’acuità visiva secondaria alla disfunzione dei fotorecettori. Gli individui possono sperimentare fotosensibilità, aumento dell’abbagliamento dopo l’esposizione alla luce, diminuzione della visione a colori, e/o scotomi centrali e scotomi arcuati a forma di salsiccia (Bjerrum) dovuti alla disfunzione dei coni. La cecità notturna, gli scotomi periferici ad anello o un calo significativo della visione periferica possono essere osservati con la disfunzione dei bastoncelli. Le fotopsie si vedono anche con la retinopatia associata al cancro circa il 7-15% del tempo. Sono descritte come luci tremolanti o scintillanti e si pensa che siano causate dalla degenerazione retinica. Uno studio ha scoperto che i sintomi visivi possono precedere una diagnosi di cancro.
Fenomeno entoptico
Quando gli individui percepiscono un’immagine che ha origine all’interno dei loro stessi occhi, questa è conosciuta come un’immagine entoptica (Figura 3). Questo fenomeno può derivare dal far brillare una luce di una penna a contatto con le palpebre chiuse di un individuo e poi muovere la luce della penna. Le immagini che appaiono con questo sono descritte come un modello ramificato di linee dovuto all’ombra proiettata dai vasi retinici su altre aree della retina. A volte, l’immagine può lampeggiare e pulsare con il battito cardiaco e rimarrà per alcuni secondi come la fonte di luce continua a muoversi. In passato, questo fenomeno è stato utilizzato come un test alternativo di acuità visiva. Se un individuo era in grado di vedere il modello di ramificazione in un occhio ma non nell’altro, l’occhio che non vedeva l’immagine era determinato ad avere una funzione maculare più povera.
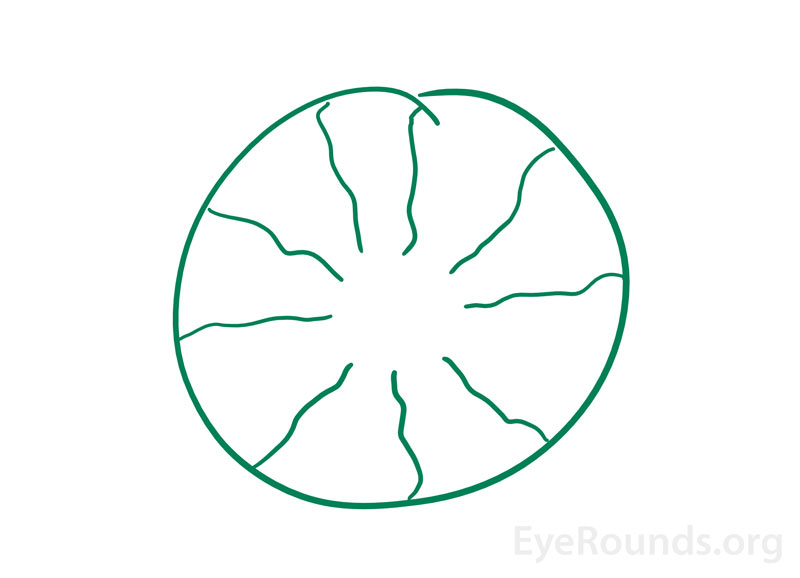
Figura 3. Illustrazione di un fenomeno entoptico fornito da un paziente molto astuto nella clinica neuro-oftalmologica. Ha riferito l’insorgenza di “un’immagine verde come una ciambella con linee grigie radiali” al risveglio negli ultimi 6-12 mesi. Gli esami oculistici precedenti a livello locale erano irrilevanti. Si pensava che questo fosse dovuto a un’immagine posteriore della sua zona foveale avascolare (buco nella ciambella) e dei vasi sanguigni radiali.
Fosfeni
I fosfeni sono una fotopsia positiva che si vede senza una fonte di luce. Sono descritti come lampi di luce, barre/spot di luce o macchie colorate. Possono essere provocati dallo sfregamento degli occhi, dalla tosse, da un trauma cranico o da altre cause patologiche. Si pensa che la produzione di fosfeni da questi meccanismi sia dovuta all’eccitazione dei fotorecettori nella retina attraverso la pressione meccanica. Gli altri meccanismi sottostanti variano a seconda della patologia osservata nell’occhio. La trazione retinica, i distacchi retinici, la retinopatia associata al cancro e l’allucinazione da rilascio sono tutte cause patologiche di fosfeni e si verificano come discusso sopra. I fosfeni sono anche sperimentati con intossicazioni da sostanze o irradiazioni all’occhio.
Disfotopsie positive e negative
Disfotopsie positive e negative sono eventi comuni dopo l’estrazione della cataratta con posizionamento di una lente intraoculare. La descrizione tipica data delle disfotopsie positive sono lampi di luce, bagliori o aloni presenti in periferia. Questi si verificano quando gli occhi sono aperti e variano in diverse impostazioni di luce, più comunemente si verificano quando un individuo entra in una stanza illuminata dal buio quando le pupille sono dilatate. Questi sono in contrasto con le fotopsie dovute alla trazione del vitreo, che sono tipicamente suscitate al buio e innescate dai movimenti dell’occhio. A differenza dei distacchi di retina, le disfotopsie positive non sono persistenti e non aumentano di dimensioni. Il meccanismo alla base delle disfotopsie positive è il risultato di riflessioni aberranti della luce dal bordo della lente intraoculare.
Al contrario, le disfotopsie negative sono comunemente descritte come archi, o a forma di mezzaluna, ombre in periferia. Il meccanismo alla base delle disfotopsie negative è dovuto alla frazione di luce che riflette via dall’occhio causando una piccola area in cui la luce non raggiunge la retina. Le disfotopsie negative si risolvono comunemente quando il paziente è dilatato. Sia le disfotopsie positive che quelle negative sono più comuni con le piccole IOL a spigoli vivi. Le IOL multifocali sono anche associate ad un aumento dell’abbagliamento e delle fotopsie rispetto alle IOL monofocali. Questi sintomi sono più comuni nel primo periodo post-operatorio, ma in genere si attenuano man mano che la capsula subisce la fibrosi. Anche se relativamente infrequenti, alcuni pazienti possono trovare queste distrazioni abbastanza da richiedere il riposizionamento o il posizionamento secondario della lente intraoculare.
- Brown GC, Brown MM, Fischer DH. Fotopsie: Una chiave per la diagnosi. Ophthalmology 2015;122(10):2084-2094. https://PubMed.gov/26249730. DOI: 10.1016/j.ophtha.2015.06.025
- Sharma P, Sridhar J, Mehta S. Flashes and Floaters. Prim Care 2015;42(3):425-435. https://PubMed.gov/26319347. DOI: 10.1016/j.pop.2015.05.011
- Horton JC. Disturbi dell’occhio. In: Kasper D, Fauci A, Hauser S, Longo D, Jameson JL, Loscalzo J, editors. Principi di medicina interna di Harrison, 19e. New York, NY: McGraw-Hill Education; 2014.
- Hollands H, Johnson D, Brox AC, Almeida D, Simel DL, Sharma S. Acute-onset floaters e flash: è questo paziente a rischio di distacco della retina? Jama 2009;302(20):2243-2249. https://PubMed.gov/19934426. DOI: 10.1001/jama.2009.1714
- Aminoff MJ, Greenberg DA, Simon RP. Mal di testa & dolore facciale. Neurologia clinica, 9e. New York, NY: McGraw-Hill Education; 2015.
- Vincent MB. Visione ed emicrania. Mal di testa 2015;55(4):595-599. https://PubMed.gov/25758366. DOI: 10.1111/head.12531
- Marzoli SB, Criscuoli A. Il ruolo del sistema visivo nell’emicrania. Neurol Sci 2017;38(Suppl 1):99-102. https://PubMed.gov/28527076. DOI: 10.1007/s10072-017-2890-0
- Pelletier AL, Rojas-Roldan L, Coffin J. Vision Loss in Older Adults. Am Fam Physician 2016;94(3):219-226. https://PubMed.gov/27479624
- Masharani U. Diabete mellito & Ipoglicemia. In: Papadakis MA, McPhee SJ, Rabow MW, editors. Current Medical Diagnosis & Treatment 2018. New York, NY: McGraw-Hill Education; 2018.
- Zhao Q, Zhou F, Zhang Y, Zhou X, Ying C. Fasting Plasma Glucose Variability Levels and Risk of Adverse Outcomes Among Patients with Type 2 Diabetes: A Systematic Review and Meta-analysis. Diabetes Res Clin Pract 2018;10.1016/j.diabres.2018.12.010. https://PubMed.gov/30583033. DOI: 10.1016/j.diabres.2018.12.010
- Klein R, Klein BE, Moss SE, Davis MD, DeMets DL. Lo studio epidemiologico del Wisconsin sulla retinopatia diabetica. II. Prevalenza e rischio di retinopatia diabetica quando l’età alla diagnosi è inferiore a 30 anni. Arch Ophthalmol 1984;102(4):520-526. https://PubMed.gov/6367724
- Klein R, Klein BE, Moss SE, Davis MD, DeMets DL. Lo studio epidemiologico del Wisconsin della retinopatia diabetica. III. Prevalenza e rischio di retinopatia diabetica quando l’età alla diagnosi è 30 o più anni. Arch Ophthalmol 1984;102(4):527-532. https://PubMed.gov/6367725
- Oftalmologia di base: elementi essenziali per gli studenti di medicina. 10° ed: American Academy of Ophthalmology, 2016.
- Lima Neto AC, Bittar R, Gattas GS, Bor-Seng-Shu E, Oliveira ML, Monsanto RDC, Bittar LF. Fisiopatologia e diagnosi di insufficienza vertebrobasilare: Una revisione della letteratura. Int Arch Otorhinolaryngol 2017;21(3):302-307. https://PubMed.gov/28680502. DOI: 10.1055/s-0036-1593448
- Pang L. Allucinazioni sperimentate da ipovedenti: Sindrome di Charles Bonnet. Optom Vis Sci 2016;93(12):1466-1478. https://PubMed.gov/27529611. DOI: 10.1097/opx.0000000000000959
- Vahdani K, Poon JS, Antoniou E, Giasin O, Makrygiannis G. Charles Bonnet Syndrome Following Eyelid Reconstruction Surgery. Ophthalmic Plast Reconstr Surg 2017;33(3):229-230. https://PubMed.gov/28475529. DOI: 10.1097/iop.0000000000000892
- Beaulieu RA, Tamboli DA, Armstrong BK, Hogan RN, Mancini R. Reversible Charles Bonnet Syndrome After Oculoplastic Procedures. J Neuroophthalmol 2018;38(3):334-336. https://PubMed.gov/27984353. DOI: 10.1097/wno.0000000000000477
- Moyer K, DeWilde A, Law C. Edema maculare cistoide da retinopatia associata al cancro. Optom Vis Sci 2014;91(4 Suppl 1):S66-70. https://PubMed.gov/24531653. DOI: 10.1097/opx.00000000000184
- Grange L, Dalal M, Nussenblatt RB, Sen HN. Retinopatia autoimmune. Am J Ophthalmol 2014;157(2):266-272.e261. https://PubMed.gov/24315290. DOI: 10.1016/j.ajo.2013.09.019
- Grewal DS, Fishman GA, Jampol LM. Retinopatia autoimmune e anticorpi antiretinici: una revisione. Retina 2014;34(5):827-845. https://PubMed.gov/24646664. DOI: 10.1097/iae.00000000000119
- Adamus G. Bersagli autoanticorpali e la loro relazione di cancro nella patogenicità della retinopatia paraneoplastica. Autoimmun Rev 2009;8(5):410-414. https://PubMed.gov/19168157. DOI: 10.1016/j.autrev.2009.01.002
- Chang DF. Capitolo 2. Esame oftalmologico. In: Riordan-Eva P, Cunningham ET, editors. Vaughan & Asbury’s General Ophthalmology, 18e. New York, NY: The McGraw-Hill Companies; 2011.
- Coppola D, Purves D. La scomparsa straordinariamente rapida delle immagini entoptiche. Proc Natl Acad Sci U S A 1996;93(15):8001-8004. https://PubMed.gov/8755592
- Mark HH. La visione entoptica dei vasi retinici. Acta Ophthalmol 2014;92(3):e237-240. https://PubMed.gov/23890291. DOI: 10.1111/aos.12192
- Ropper AH, Samuels MA, Klein JP. Capitolo 13. Disturbi della visione. Principi di neurologia di Adams e Victor, 10e. New York, NY: The McGraw-Hill Companies; 2014.
- Salari V, Scholkmann F, Vimal RLP, Csaszar N, Aslani M, Bokkon I. Fosfeni, rumore scuro discreto retinico, afterimages negativi e proiezioni retinogenicolate: Un nuovo quadro esplicativo basato sulla luminescenza oculare endogena. Prog Retin Eye Res 2017;60:101-119. https://PubMed.gov/28729002. DOI: 10.1016/j.preteyeres.2017.07.001
- Mathis T, Vignot S, Leal C, Caujolle JP, Maschi C, Mauget-Faysse M, Kodjikian L, Baillif S, Herault J, Thariat J. Meccanismi dei fosfeni nei pazienti irradiati. Oncotarget 2017;8(38):64579-64590. https://PubMed.gov/28969095. DOI: 10.18632/oncotarget.18719
- Bournas P, Drazinos S, Kanellas D, Arvanitis M, Vaikoussis E. Disfotopsia dopo chirurgia della cataratta: confronto tra quattro diverse lenti intraoculari. Ophthalmologica 2007;221(6):378-383. https://PubMed.gov/17947823. DOI: 10.1159/000107496
- Davison JA. Disfotopsia positiva e negativa in pazienti con lenti intraoculari acriliche. J Cataract Refract Surg 2000;26(9):1346-1355. https://PubMed.gov/11020620
- Hu J, Sella R, Afshari NA. Disfotopsia: un fenomeno ottico multiforme. Curr Opin Ophthalmol 2018;29(1):61-68. https://PubMed.gov/29084005. DOI: 10.1097/icu.0000000000000447
- Wang SY, Stem MS, Oren G, Shtein R, Lichter PR. Risultati incentrati sul paziente e sulla qualità visiva della chirurgia della cataratta premium: una revisione sistematica. Eur J Ophthalmol 2017;27(4):387-401. https://PubMed.gov/28574135. DOI: 10.5301/ejo.5000978
Suggested Citation Format
Morrow N, Chung AT, Wall M. Photopsias. EyeRounds.org. 24 giugno 2019; Disponibile da https://EyeRounds.org/tutorials/photopsias/index.htm