Współczynnik podziału
Współczynnik podziału to równowagowy rozkład analitu pomiędzy fazą próbki a fazą gazową.
Próbki muszą być przygotowane w taki sposób, aby zmaksymalizować stężenie składników lotnych w przestrzeni nadpowierzchniowej i zminimalizować niepożądane zanieczyszczenie innymi związkami w matrycy próbki. Aby pomóc w określeniu stężenia analitu w przestrzeni nadpowierzchniowej, należy obliczyć współczynnik podziału (K).
| Wartości K powszechnych rozpuszczalników w układach powietrze-woda w temperaturze 40°C | ||||||||
| Rozpuszczalnik | Cykloheksan | n-Heksan | Tetrachloroetylen | 1,1,1-Trichlormetan | O-Xylen | Toluen | Benzen | Dichlormetan |
| Wartość K | 0.077 | 0.14 | 1.48 | 1.65 | 2.44 | 2.82 | 2.90 | 5.65 |
| Solwent | n-Butylooctan | Etylooctan | Metyloetyloketon | n-.Butanol | Izopropanol | Etanol | Dioksan | |
| Wartość K | 31.4 | 62.4 | 139.5 | 647 | 825 | 1355 | 1618 | |
Obliczanie współczynnika podziału
Współczynnik podziału (K) = Cs/Cg
gdzie:
Cs to stężenie analitu w fazie próbki;
Cg to stężenie analitu w fazie gazowej
Współczynniki podziału typowych związków
Związki, które mają niskie wartości K będą miały tendencję do łatwiejszego podziału do fazy gazowej i będą miały stosunkowo wysokie odpowiedzi i niskie granice wykrywalności. Przykładem tego może być heksan w wodzie: w temperaturze 40°C, heksan ma wartość K równą 0,14 w układzie powietrze-woda.
Związki, które mają wysokie wartości K będą miały tendencję do mniej łatwego podziału do fazy gazowej i będą miały stosunkowo niskie odpowiedzi i wysokie limity wykrywania.
Przykładem tego może być etanol w wodzie: w temperaturze 40°C, etanol ma wartość K równą 1355 w układzie powietrze-woda.
Wartości współczynnika podziału dla innych powszechnie występujących związków przedstawiono w tabeli powyżej.
Zmiana współczynnika podziału
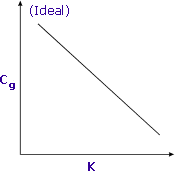 |
Czułość wzrasta, gdy K jest zminimalizowane |
Dodawanie soli nieorganicznych
Wysokie stężenia soli w próbkach wodnych zmniejszają rozpuszczalność polarnych lotnych związków organicznych w matrycy próbki i promują ich przenoszenie do przestrzeni nadfazowej, co skutkuje niższymi wartościami K. Wielkość wpływu soli na K nie jest jednak taka sama dla wszystkich związków.
Związki o wartościach K, które są już stosunkowo niskie, doświadczą bardzo małej zmiany współczynnika podziału po dodaniu soli do wodnej matrycy próbki.
Generalnie, lotne związki polarne w matrycach polarnych (próbki wodne) doświadczą największych zmian w K i będą miały wyższe odpowiedzi po dodaniu soli do matrycy próbki.
Powszechnie stosowane sole w celu zmniejszenia efektów matrycy:
- Chlorek amonu
- Siarczan amonu
- Chlorek sodu
- Cytrynian sodu
- Siarczan sodu
- Węglan potasu
Wartość K zależy również od Stosunku Fazowego. Jest to omówione w następnej sekcji.
Stosunek faz
Stosunek faz (β) jest zdefiniowany jako względna objętość przestrzeni nadfazowej w porównaniu z objętością próbki w fiolce z próbką.
| Obliczanie stosunku fazowego Stosunek fazowy (β) = Vg / Vs gdzie: Vs jest objętością fazy próbki |
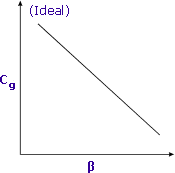 |
| Czułość wzrasta, gdy β jest zminimalizowane |
Niższe wartości β (tj.tj. większy rozmiar próbki) przyniosą wyższe odpowiedzi dla związków lotnych.
Zmniejszenie wartości β nie zawsze przyniesie wzrost odpowiedzi potrzebny do poprawy czułości.
Gdy β jest zmniejszone poprzez zwiększenie rozmiaru próbki, związki o wysokich wartościach K w mniejszym stopniu rozdzielają się do przestrzeni nad głową w porównaniu do związków o niskich wartościach K i dają odpowiednio mniejsze zmiany w Cg.
Próbki, które zawierają związki o wysokich wartościach K, muszą być zoptymalizowane w celu zapewnienia najniższej wartości K przed dokonaniem zmian w stosunku faz.
Połączenie współczynnika podziału i stosunku faz
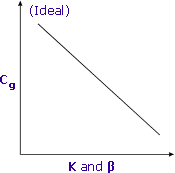
Niższe K i β skutkują wyższym Cg i lepszą czułością
Współczynniki podziału i stosunki faz współpracują ze sobą w celu określenia końcowego stężenia lotnych związków w przestrzeni głównej fiolek z próbkami.
Stężenie lotnych związków w fazie gazowej można wyrazić jako:
Cg = Co / (K + β)
gdzie
Cg jest stężeniem lotnych analitów w fazie gazowej
i
Co jest pierwotnym stężeniem lotnych analitów w próbce.
Dążenie do najniższych wartości zarówno dla K, jak i β spowoduje wyższe stężenie lotnych analitów w fazie gazowej, a zatem lepszą czułość.
.