Generaattinen nimi: neostigmiinibromidi
annosmuoto: tabletti
Lääketieteellisesti tarkistanut Drugs.com. Viimeksi päivitetty 21. huhtikuuta 2020.
- Haittavaikutukset
- annostus
- Professori
- Vuorovaikutukset
- Raskaus
- Lisätiedot
Vahinkovapauslauseke: FDA ei ole todennut tätä lääkettä turvalliseksi ja tehokkaaksi, eikä FDA ole hyväksynyt tätä lääkkeen merkintää. Lisätietoja hyväksymättömistä lääkkeistä saat täältä.
Prostigmin-tavaramerkki on lopetettu Yhdysvalloissa.
- Prostigmin Kuvaus
- Prostigmiini – Kliininen farmakologia
- Prostigmiinin käyttöaiheet ja käyttö
- Vasta-aiheet
- Varoitukset
- Varotoimet
- Yleistä:
- Lääkeinteraktiot:
- Karsinogeneesi, mutageenisuus ja hedelmällisyyden heikentyminen:
- Raskaus:
- Imettävät äidit:
- Pediatrinen käyttö:
- Haittavaikutukset
- Yliannostus
- Prostigmiinin annostus ja antotapa
- Miten Prostigminia toimitetaan
- PÄÄNÄYTTÖPANEELI – 15 mg etiketti
- Lisää tietoa prostigmiinista. (neostigmiini)
- Seuraavat hoito-oppaat
Prostigmin Kuvaus
Prostigmin (neostigmiinibromidi), antikolinesteraasi aine, on saatavana suun kautta annettavana 15 mg:n tablettina. Jokainen tabletti sisältää myös gelatiinia, laktoosia, maissitärkkelystä, steariinihappoa, sokeria ja talkkia.
Kemiallisesti neostigmiinibromidi on (m-hydroksifenyyli)trimetyyliammoniumbromidimetyylikarbamaatti. Se on valkoinen, kiteinen, kitkerä jauhe, joka liukenee 1:1 veteen, jonka molekyylipaino on 303,20 ja jonka rakennekaava on seuraava:
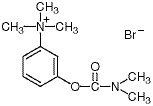
Prostigmiini – Kliininen farmakologia
Neostigmiini estää asetyylikoliinin hydrolyysiä kilpailemalla asetyylikoliinin kanssa asetyylikoliiniesteraasiin kiinnittymisestä kolinergisen välityksen paikoissa. Se tehostaa kolinergistä vaikutusta helpottamalla impulssien välittymistä hermo-lihasliitosten kautta. Sillä on myös suora kolinomimeettinen vaikutus luurankolihakseen ja mahdollisesti autonomisiin gangliosoluihin ja keskushermoston hermosoluihin. Neostigmiini hydrolysoituu koliiniesteraasin avulla ja metaboloituu myös maksan mikrosomaalisten entsyymien avulla. Proteiinisidos ihmisen seerumin albumiiniin on 15-25 prosenttia.
Neostigmiinibromidi imeytyy huonosti ruoansulatuskanavasta suun kautta annettuna. Yleensä 15 mg neostigmiinibromidia suun kautta vastaa 0,5 mg neostigmiinimetyylisulfaattia parenteraalisesti, johtuen tabletin huonosta imeytymisestä suolistosta. Paastoavilla myasteenikoilla tehdyssä tutkimuksessa imeytymisen laajuudeksi arvioitiin 1-2 prosenttia nautitusta 30 mg:n oraalisesta kerta-annoksesta. Huippupitoisuudet plasmassa esiintyivät 1 – 2 tuntia lääkkeen nauttimisen jälkeen, ja yksilölliset vaihtelut olivat huomattavat. Puoliintumisaika vaihteli 42 minuutista 60 minuuttiin keskimääräisen puoliintumisajan ollessa 52 minuuttia.
Prostigmiinin käyttöaiheet ja käyttö
Prostigmiini on tarkoitettu myasthenia graviksen oireenmukaiseen hoitoon. Sen suurin hyöty on pitkäkestoisessa hoidossa, jossa ei ole nielemisvaikeuksia. Akuutissa myasteenisessa kriisissä, jossa esiintyy hengitys- ja nielemisvaikeuksia, on käytettävä parenteraalista muotoa (neostigmiinimetyylisulfaatti). Potilas voidaan siirtää oraaliseen muotoon heti, kun se on siedettävissä.
Vasta-aiheet
Prostigmiini on vasta-aiheinen potilaille, joilla on tunnettu yliherkkyys lääkkeelle. Bromidi-ionin esiintymisen vuoksi sitä ei saa käyttää potilaille, joilla on aiemmin ollut reaktio bromideille. Se on vasta-aiheinen potilaille, joilla on vatsakalvotulehdus tai suoliston tai virtsateiden mekaaninen tukos.
Varoitukset
Prostigmiinia tulee käyttää varoen potilaille, joilla on epilepsia, keuhkoastma, bradykardia, äskettäinen sepelvaltimotukos, vagotonia, kilpirauhasen liikatoiminta, sydämen rytmihäiriöt tai mahahaava. Yleensä 15 mg neostigmiinibromidia suun kautta vastaa 0,5 mg neostigmiinimetyylisulfaattia parenteraalisesti, koska tabletti imeytyy huonosti suolistosta. Suuria annoksia on vältettävä tilanteissa, joissa imeytymisnopeus suolistosta saattaa lisääntyä. Sitä on käytettävä varoen, kun sitä annetaan samanaikaisesti antikolinergisten lääkkeiden kanssa, jotta vältetään suoliston liikkuvuuden väheneminen.
Varotoimet
Yleistä:
On tärkeää erottaa toisistaan Prostigminin yliannostuksen aiheuttama myasteninen kriisi ja kolinerginen kriisi. Molemmat tilat johtavat äärimmäiseen lihasheikkouteen, mutta vaativat radikaalisti erilaista hoitoa. (Ks. kohta YLIANNOSTELU.)
Lääkeinteraktiot:
Tietyillä antibiooteilla, erityisesti neomysiinillä, streptomysiinillä ja kanamysiinillä, on lievä, mutta selvä ei-depolarisoiva estovaikutus, joka voi voimistaa neuromuskulaarista estoa. Näitä antibiootteja tulisi käyttää myasteenipotilaalle vain, jos se on ehdottomasti aiheellista, ja silloin antikoliiniesteraasiannostusta on säädettävä huolellisesti.
Paikallispuudutteita ja joitakin yleisanestesia-aineita, rytmihäiriölääkkeitä ja muita lääkkeitä, jotka häiritsevät neuromuskulaarista transmissiota, tulisi käyttää varovaisesti, jos ollenkaan, potilailla, jotka sairastavat myastenia gravista; Prostigminin annostusta saatetaan joutua suurentamaan vastaavasti.
Karsinogeneesi, mutageenisuus ja hedelmällisyyden heikentyminen:
Prostigmiinilla ei ole tehty tutkimuksia, joiden perusteella voitaisiin arvioida sen karsinogeenista tai mutageenista potentiaalia. Tutkimuksia prostigmiinin vaikutuksesta hedelmällisyyteen ja lisääntymiseen ei ole tehty.
Raskaus:
Teratogeeniset vaikutukset: Raskauskategoria C
Prostigmiinilla ei ole tehty riittäviä tai hyvin kontrolloituja tutkimuksia koe-eläimillä eikä raskaana olevilla naisilla. Ei tiedetä, voiko Prostigmin aiheuttaa sikiövaurioita, kun sitä annetaan raskaana olevalle naiselle, tai voiko se vaikuttaa lisääntymiskykyyn. Prostigmiinia tulee antaa raskaana olevalle naiselle vain, jos se on selvästi tarpeen.
Ei-teratogeeniset vaikutukset:
Antikolinesteraasilääkkeet voivat aiheuttaa kohdun ärtyneisyyttä ja käynnistää ennenaikaisen synnytyksen, kun niitä annetaan laskimoon raskaana oleville naisille lähellä synnytystä.
Imettävät äidit:
Ei tiedetä, erittyykö prostigmiini ihmismaitoon. Koska monet lääkkeet erittyvät ihmismaitoon ja koska Prostigmin voi aiheuttaa vakavia haittavaikutuksia imettäville imeväisille, on päätettävä imetyksen keskeyttämisestä tai lääkkeen lopettamisesta ottaen huomioon lääkkeen merkitys äidille.
Pediatrinen käyttö:
Turvallisuutta ja tehoa lapsilla ei ole varmistettu.
Haittavaikutukset
Haittavaikutukset johtuvat yleensä farmakologisten vaikutusten liioittelusta, joista syljeneritys ja faskikulaatio ovat yleisimpiä. Myös suolikouristuksia ja ripulia voi esiintyä.
Joko neostigmiinibromidin tai neostigmiinimetyylisulfaatin käytön jälkeen on raportoitu seuraavia muita haittavaikutuksia:
Allergia: Allergiset reaktiot ja anafylaksia.
Neurologiset: Huimaus, kouristukset, tajunnan menetys, uneliaisuus, päänsärky, dysartria, miosis ja näkömuutokset.
Kardiovaskulaarinen: Sydämen rytmihäiriöitä (mukaan lukien bradykardia, takykardia, A-V-blokki ja nodaalinen rytmi) ja epäspesifisiä EKG-muutoksia on raportoitu, samoin kuin sydänpysähdystä, synkopeeta ja hypotensiota. Näitä on havaittu pääasiassa Prostigminin injektoitavan muodon käytön jälkeen.
Hengitys: Lisääntynyt suun, nielun ja brokiaalinen eritys ja hengenahdistus. Hengityslamaa, hengityksen pysähtymistä ja bronkospasmia on raportoitu Prostigmin injektoitavan muodon käytön jälkeen.
Dermatologiset: Ihottuma ja nokkosihottuma.
Ruuansulatuskanava: Pahoinvointi, oksentelu, ilmavaivat ja lisääntynyt peristaltiikka.
Virtsaneritys: Virtsaamistiheys.
Hermo- ja liikuntaelimistö: Lihaskrampit ja -kouristukset, niveltulehdus.
Muut: Diaforeesi, punoitus ja heikkous.
Yliannostus
Prostigmiinin yliannostus voi aiheuttaa kolinergisen kriisin, jolle on ominaista lisääntyvä lihasheikkous ja joka hengityslihasten osallistumisen kautta voi johtaa kuolemaan. Myasteeniseen kriisiin, joka johtuu taudin vaikeusasteen lisääntymisestä, liittyy myös äärimmäistä lihasheikkoutta, ja sitä voi olla vaikea erottaa kolinergisestä kriisistä oireiden perusteella. Tällainen erottelu on kuitenkin erittäin tärkeää, koska prostigmiinin tai muiden tähän luokkaan kuuluvien lääkkeiden annoksen suurentamisella kolinergisen kriisin tai refraktorisen tai “epäherkän” tilan vallitessa voi olla vakavia seurauksia. Nämä kaksi kriisityyppiä voidaan erottaa toisistaan Tensilon®:n (edrofoniumkloridi) käytön sekä kliinisen harkinnan perusteella.
Kahden tilan hoito eroaa radikaalisti toisistaan. Siinä missä myasteeninen kriisi edellyttää intensiivisempää antikolinesteraasihoitoa, kolinerginen kriisi edellyttää kaikkien tämäntyyppisten lääkkeiden pikaista lopettamista. Myös atropiinin välitöntä käyttöä kolinergisessä kriisissä suositellaan.
Atropiinia voidaan käyttää myös maha-suolikanavan haittavaikutusten tai muiden muskariinireaktioiden poistamiseksi tai minimoimiseksi; mutta tällainen käyttö voi peittämällä yliannostuksen merkit johtaa kolinergisen kriisin tahattomaan induktioon.
Neostigmiinimetyylisulfaatin LD50-arvo hiirillä on 0,3±0,02 mg/kg laskimonsisäisesti 0,54±0.03 mg/kg ihonalaisesti ja 0,395±0,025 mg/kg lihaksensisäisesti; rotilla LD50 on 0,315±0,019 mg/kg laskimoon, 0,445±0,032 mg/kg ihonalaisesti ja 0,423±0,032 mg/kg lihaksensisäisesti.
Prostigmiinin annostus ja antotapa
Suun kautta annetun prostigmiinin vaikutuksen alkaminen on hitaampaa kuin parenteraalisesti annettuna, mutta vaikutuksen kesto on pidempi ja vaikutuksen voimakkuus tasaisempi. Annostusvaatimukset optimaalisten tulosten saavuttamiseksi vaihtelevat 15 mg:sta 375 mg:aan päivässä. Joissakin tapauksissa voi olla tarpeen ylittää nämä annokset, mutta kolinergisen kriisin mahdollisuus on otettava huomioon. Keskimääräinen annos on 10 tablettia (150 mg), jotka annetaan 24 tunnin aikana. Annosten välinen aika on ensiarvoisen tärkeä. Annosteluaikataulu on sovitettava kullekin potilaalle ja sitä on muutettava tarpeen mukaan. Usein hoitoa tarvitaan yötä päivää. Suurempia annoksia päivittäisestä kokonaisannoksesta voidaan antaa aikoina, jolloin potilas on alttiimpi väsymykselle (iltapäivällä, aterioiden aikana jne.). Potilasta on rohkaistava pitämään päivittäin kirjaa voinnistaan, jotta lääkärin on helpompi määrittää optimaalinen hoito-ohjelma.
Miten Prostigminia toimitetaan
Värjättyjä, valkoisia tabletteja, jotka sisältävät 15 mg neostigmiinibromidia, 100 kpl:n pulloja (NDC 0187-3100-10). Jälki tabletissa: (edessä) Prostigmin 15; (takana) V.
Valeant Pharmaceuticals North America
One Enterprise
Aliso Viejo, CA 92656 USA
(949) 461-6000
Rev. 02/08
PÄÄNÄYTTÖPANEELI – 15 mg etiketti
NDC 0187-3100-10
Rx Only
Prostigmin®
(neostigmiinibromidi)
15 mg
100 tablettia
Jokainen tabletti sisältää 15 mg neostigmiinibromidia
VALEANT™

| Prostigmin neostigmiinibromiditabletti |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Merkintä – Valeant Pharmaceuticals North America LLC (042230623)
Lisää tietoa prostigmiinista. (neostigmiini)
- Haittavaikutukset
- Raskauden tai imetyksen aikana
- Asetustiedot
- Lääkeinteraktiot
- Lääkeryhmä: Neostigmiinimetyylisulfaatti-injektio (FDA)
- Neostigmiinimetyylisulfaatti-injektio (FDA)
- Neostigmiinimetyylisulfaatti-injektio (FDA)
Neostigmiinimetyylisulfaatti-injektio (FDA) Ei ole.
Muut tuotemerkit Bloxiverz
Seuraavat hoito-oppaat
- Myasthenia Gravis
- Virtsankarkailun pidätyskyky
Lääketieteellinen vastuuvapauslauseke