Więcej niż tylko błyski i pływaki
Autorzy: Nicole C. Morrow BS, Anthony T. Chung, MD, Michael Wall, MD
Posted June 24, 2019
Introduction
Fotopsje (tj. błyski) są częstym objawem prezentującym się w klinice okulistycznej. Chociaż większość fotopsji ma pochodzenie siatkówkowe, charakterystyka wyglądu, początku i towarzyszących cech jest krytyczna w ustaleniu przyczyny tych wybitnych, ale różnorodnych opisów “błyskających świateł”. Poniższy tutorial omawia różne źródła fotopsji: trakcja witreoretinalna, migreny oczne, zwyrodnienie plamki związane z wiekiem, cukrzyca, mózgowy przepływ krwi, halucynacje wzrokowe, retinopatia związana z nowotworem, zjawisko entoptyczne, fosfeny i dysfotopsje związane z soczewką.
Dyskusja
Odwarstwienie ciała szklistego, rozdarcie siatkówki, i/lub odwarstwienie siatkówki
Odwarstwienie ciała szklistego (PVD) jest częstą przyczyną floaterów i fotopsji w populacji ogólnej, stanowiąc około 40% pacjentów prezentujących te objawy. Pływaki (Rycina 1) są zwykle spowodowane przez komórki lub resztki pływające w szklistce, które rzucają cienie na siatkówkę. Pacjenci często opisują również widzenie dużego nieprzezroczystego pływaka, który oddziela się od ciała szklistego wokół głowy nerwu wzrokowego. W badaniu klinicznym, to oddzielenie ciała szklistego od okrągłego nerwu wzrokowego może być widoczne jako pierścień Weissa.
Fotopsje występują jako pociąganie ciała szklistego na siatkówce. Napięcie od ciała szklistego na siatkówce powoduje, że komórki siatkówki zapalają się i prowadzi do percepcji błysków światła. Błyski te trwają zwykle krócej niż jedną sekundę i są opisywane jako smuga błyskawicy lub błysk aparatu fotograficznego na peryferiach. Kształt smugi świetlnej jest zwykle krzywoliniowy ze względu na krawędź trakcji szklistkowo-siatkówkowej. Fotopsje mogą występować jednostronnie lub obustronnie, ale obustronne błyski występują zwykle w różnym czasie w każdym oku.
Retinal łzy mogą również powodować floaters i błyski światła na peryferiach . Rozdarcia siatkówki spowodowane trakcją spowodowaną urazem lub PVD mają zwykle kształt podkowy i, jeśli są wystarczająco duże, szkliwo przedostaje się do przestrzeni podsiatkówkowej, powodując rehematogenne odwarstwienie siatkówki (RRD). W przypadku RRD konieczna jest interwencja chirurgiczna, która wiąże się z trwałym i postępującym pogorszeniem widzenia, które pacjenci zwykle opisują jako zasłonę w polu widzenia. Rozróżnienie pomiędzy ostrym PVD a przedarciem siatkówki może być trudne jedynie na podstawie wywiadu. Hollands i wsp. stwierdzili, że u 14% pacjentów, u których występują łzawienia i/lub błyski i u których rozpoznano PVD, występuje również przedarcie siatkówki; jeśli jednak nie występuje subiektywne pogorszenie ostrości wzroku, ryzyko to spada do 8,9%. I odwrotnie, jeśli pacjent zgłasza subiektywne pogorszenie ostrości wzroku lub widoczny jest krwotok do ciała szklistego, wówczas ryzyko przedarcia wzrasta odpowiednio do 45% i 62%. Jeśli zauważony zostanie pigment szklistkowy (np. objaw Shafera), wówczas ryzyko przedarcia siatkówki wynosi aż 88%. U pacjentów, u których zdiagnozowano PVD bez przedarcia siatkówki, 3,4% miało przedarcie siatkówki w ciągu sześciu tygodni od pierwotnej prezentacji. Dlatego wszyscy pacjenci powinni mieć powtórzone poszerzone badanie dna oka w ciągu 4-6 tygodni od pierwszej prezentacji.

Ryc. 1. Illustration of floaters typical of a posterior vitreous detachment
Migrena oczna
Migrena jest nawracającym, często jednostronnym, zespołem bólu głowy, często z prodromem obustronnych pozytywnych zjawisk wzrokowych. Klasyczna migrena” jest opisana przez posiadanie tego prodromu (tj. aury) trwającego około 15 do 30 minut, po którym następuje ból głowy i związane z nim objawy, które mogą utrzymywać się przez wiele godzin. Chociaż zjawisko wizualne zazwyczaj występuje obustronnie, fotopsje mogą wydawać się większe w jednym oku niż w drugim. Objawy wizualne mogą wystąpić z każdym migrenowym bólem głowy osoba ma lub może się zdarzyć tylko raz . Migrena i aury nie są w pełni zrozumiałe i istnieje wiele dyskusji na temat ich mechanizmów leżących u podstaw. Wiodącą teorią jest to, że migreny są spowodowane przez zaburzenia w mózgowym przepływie krwi i fala depresji aktywności neuronów porusza się powoli w całym mózgu; proces ten zwykle zaczyna się w płacie potylicznym i rozprzestrzenia się w kierunku przednim. Aura migrenowa jest prawdopodobnie wynikiem początkowej fali wysokiej aktywności neuronalnej związanej z wcześniej opisaną rozprzestrzeniającą się depresją, po której następuje zahamowanie aktywności. Aury mogą manifestować się jako małe jasne światła, martwe punkty, statyczne/mgliste widzenie, i/lub złożone zaburzenia widzenia. Zazwyczaj, aury zaczynają się przed bólem głowy jako centralna, półksiężycowata, scyntylacyjna skotoma, która rozszerza się na zewnątrz i jest otoczona przez błyski lub zygzaki światła. W migrenie siatkówkowej, pacjent doświadcza zmniejszenia widzenia lub całkowitej ślepoty w jednym oku bez migotania scotoma; jest to spowodowane skurczem naczyniowym krążenia siatkówki lub tętnicy okulistycznej. Widzenie w migrenie siatkówkowej szybko wraca do normy. Bardzo rzadką postacią migreny jest migrena oftalmoplegiczna, która może powodować przejściowe porażenie jednego z trzech nerwów czaszkowych zaangażowanych w ruch gałki ocznej (CN III, CN IV, i CN VI), ale nie jest związana z fotopsjami.


Ryc. 2. Ilustracje scyntylacyjnych scotomas typowych dla migreny ocznej. Te mogą produkować różnorodne zjawiska wizualne, w tym zig zags i/lub kolorowe “statyczne-podobne” obrazy.
Zwyrodnienie plamki związane z wiekiem
Niewysiękowe (tj. suche) zwyrodnienie plamki związane z wiekiem (AMD) powoduje stopniową obustronną centralną utratę wzroku bez powiązanego bólu. Pacjenci zgłaszają zmniejszone widzenie centralne i metamorfopsję, ale zazwyczaj nie mają fotopsji związanych z suchą postacią AMD. Wysiękowe (tj. neowaskularne lub mokre) AMD jest jednak kolejną częstą przyczyną fotopsji i drugą co do częstości przyczyną w jednej z opisanych serii przypadków. Około 50% osób z wysiękową postacią AMD zgłasza występowanie powtarzających się, centralnie zlokalizowanych błysków trwających od kilku sekund do kilku minut. Błyski te są zwykle opisywane jako migotanie, pulsowanie, migoczące światła, światła podobne do węża, światła wirujące, wiatraczki lub koła. Światła te są najczęściej koloru białego, ale ludzie zgłaszali widzenie niebieskich, srebrnych, złotych lub różnokolorowych świateł. Prawdopodobieństwo wystąpienia fotopsji wzrasta wraz ze wzrostem powierzchni błon neowaskularnych. W przeciwieństwie do fotopsji w PVD, które są stymulowane przez wewnętrzny interfejs siatkówka-witrena, fotopsje w wysiękowej AMD występują z powodu gromadzenia się płynu stymulującego zewnętrzne warstwy siatkówki. Rozróżnienie między nimi może być czasami trudne przed badaniem; jednak centralne błyski są znacznie częstsze w AMD, a błyski obwodowe są częstsze w PVD .
Cukrzyca
Cukrzyca może powodować wiele zmian wzrokowych. Progresja choroby może prowadzić do proliferacyjnej lub nieproliferacyjnej retinopatii cukrzycowej. Pacjenci z cukrzycą, którzy ściśle kontrolują poziom glukozy we krwi, mogą znacznie zmniejszyć ryzyko rozwoju retinopatii cukrzycowej. Jednak większość pacjentów będzie rozwijać retinopatię cukrzycową po 15 latach z chorobą . Retinopatia cukrzycowa nieproliferacyjna charakteryzuje się mikrotętniakami, krwotokami kropkowo-plamkowymi, twardymi wysiękami, plamami waty i obrzękiem plamki. U pacjentów z obrzękiem plamki powszechnie występuje obniżenie ostrości wzroku. Jednakże, większość pacjentów pozostaje bezobjawowa do momentu osiągnięcia fazy proliferacyjnej. Retinopatia cukrzycowa proliferacyjna pojawia się, gdy przedłużające się niedokrwienie siatkówki wyzwala tworzenie nowych naczyń i tkanki włóknistej. Nowy włóknisty wzrost tworzy skurczoną bliznę na granicy szklistkowo-siatkówkowej i może powodować fotopsje, ponieważ tkanka kurczy się. Skurcz ten może prowadzić do trakcyjnego odwarstwienia siatkówki (TRD) z potencjalnym krwotokiem do ciała szklistego, ponieważ nowe naczynia są kruche. Pacjenci z TRD mogą zgłaszać pływające plamki, fotopsje i/lub zasłonę nad polem widzenia, która jest podobna do rehematogennego odwarstwienia siatkówki. Powikłania retinopatii cukrzycowej proliferacyjnej mogą prowadzić do trwałej utraty wzroku. W niewielkim badaniu pacjenci z hipoglikemią, którzy byli insulinozależnymi diabetykami, zgłaszali obustronne fotopsje, które ustępowały, gdy poziom glukozy wracał do normy. Występowały one w jasnym lub ciemnym otoczeniu i były opisywane jako białe migotania lub okręgi.
Niedobór tętnicy międzykręgowej
Niedobór tętnicy międzykręgowej powoduje zmniejszony przepływ krwi do tylnego aspektu mózgu i jest związany ze starzeniem się. Ten zmniejszony przepływ krwi powoduje niedokrwienie tego obszaru i prowadzi do obustronnych fotopsji, które są opisywane jako przerywane błyski trwające od sekund do minut. Ponadto, niewydolność kręgowo-podstawna związana jest z zawrotami głowy, diplopią, ślepotą, osłabieniem i ataksją. Pacjenci mogą mieć podobne błyski światła i zamglenia widzenia, podobne do migreny wzrokowej; jednak objawy te nie trwają tak długo i nie występują przed bólem głowy.
Halucynacje uwalniające (zespół Charlesa Bonneta)
Halucynacje uwalniające są charakteryzowane jako halucynacje wzrokowe wynikające z uszkodzenia drogi wzrokowej, jednostronnie lub obustronnie, u osób z nienaruszonym poznaniem . Pacjenci opisują widzenie wielobarwnych kształtów, siatek, twarzy, ludzi i kwiatów, trwające od sekund do minut. Mechanizm leżący u podstaw tego zaburzenia jest słabo poznany. Najbardziej powszechnie akceptowaną teorią jest teoria deprywacji sensorycznej, która stwierdza, że utrata bodźców wzrokowych do kory wzrokowej zwiększa pobudliwość neuronów. Ta zwiększona aktywność neuronów prowadzi do przypadkowego odpalania neuronów przy niewielkiej ilości lub braku bodźców, stąd nazwa halucynacje uwalniające. Jest to wspierane przez wysoką częstość występowania u osób z gorszą ostrością widzenia i po pooperacyjnej łaty oczu . Częstość występowania zespołu Charlesa Bonneta wzrasta u osób z gorszą ostrością wzroku obustronnie .
Retinopatia związana z nowotworem
Retinopatia związana z nowotworem jest rzadką chorobą autoimmunologiczną, w której organizm rozwija autoprzeciwciała do antygenów siatkówki . Recoverin i a-enolase są najczęstszymi antygenami siatkówki, do których rozwijają się autoprzeciwciała. Przeciwciała te zazwyczaj rozwijają się w obecności nowotworu złośliwego, najczęściej drobnokomórkowego raka płuc. Pacjenci, u których rozwija się ta choroba, często prezentują obniżenie ostrości wzroku wtórne do dysfunkcji fotoreceptorów. Osoby mogą doświadczać nadwrażliwości na światło, zwiększonego olśnienia po ekspozycji na światło, zmniejszenia widzenia barwnego, i/lub centralnych skotomii oraz skotomii łukowatych w kształcie kiełbasy (Bjerrum) spowodowanych dysfunkcją czopków. Ślepota nocna, obwodowe plamy pierścieniowe lub znaczne pogorszenie widzenia obwodowego mogą być widoczne przy dysfunkcji pręcików. Fotopsje są również obserwowane w retinopatii związanej z nowotworem w około 7-15% przypadków. Są one opisywane jako migoczące lub migotliwe światła i uważa się, że są spowodowane zwyrodnieniem siatkówki. W jednym z badań stwierdzono, że objawy wzrokowe mogą poprzedzać rozpoznanie raka.
Zjawisko entoptyczne
Kiedy osoby postrzegają obraz, który powstaje w ich własnych oczach, jest to znane jako obraz entoptyczny (rysunek 3). Zjawisko to może powstać w wyniku świecenia światłem pióra w kontakcie z zamkniętymi powiekami osoby, a następnie poruszania światłem pióra. Obrazy, które pojawiają się z tym są opisane jako rozgałęziający się wzór linii ze względu na cień rzucany przez naczynia siatkówki na inne obszary siatkówki . Czasami, obraz może migać i pulsować z biciem serca i pozostanie na kilka sekund, jak źródło światła nadal się porusza . W przeszłości, zjawisko to było używane jako alternatywny test ostrości widzenia. Jeśli osoba była w stanie zobaczyć rozgałęziający się wzór w jednym oku, ale nie w drugim, oko, które nie widziało obrazu, było określane jako mające gorszą funkcję plamki żółtej .
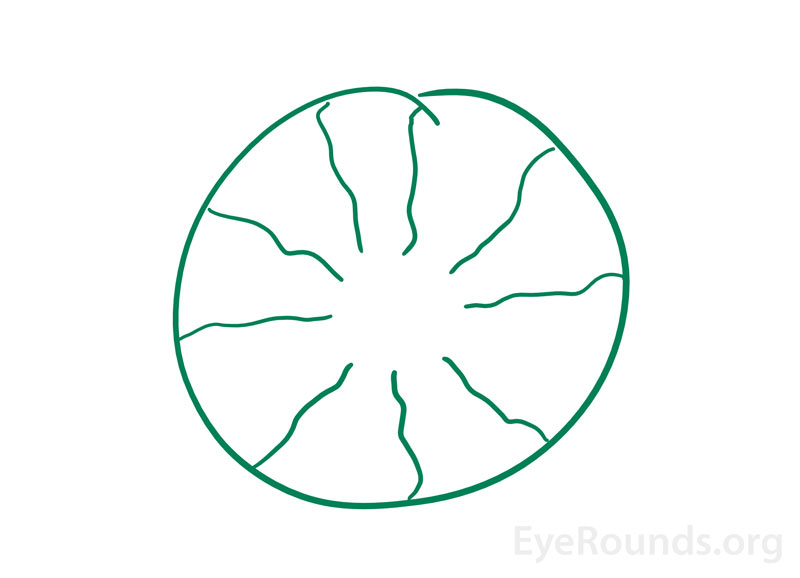
Rysunek 3. Ilustracja zjawiska entoptycznego przedstawiona przez bardzo bystrego pacjenta w klinice neurooftalmologii. Zgłosił on pojawienie się “zielonego obrazu jak pączek z promienistymi kwadratowymi liniami” po przebudzeniu w ciągu ostatnich 6-12 miesięcy. Poprzednie badania okulistyczne były bez zastrzeżeń. Uznano, że przyczyną jest powidok awaskularnej strefy nerwu wzrokowego (dziura w pączku) i promienistych naczyń krwionośnych.
Fosfeny
Fosfeny są pozytywną fotopsją , które są widziane bez źródła światła . Opisywane są jako błyski światła, paski/plamki światła lub kolorowe plamki. Mogą one być wywołane przez pocieranie oczu, kaszel, uraz głowy lub z innych przyczyn patologicznych. Wytwarzanie fosfenów przez te mechanizmy uważa się za spowodowane pobudzeniem fotoreceptorów w siatkówce przez nacisk mechaniczny . Inne mechanizmy leżące u podstaw różnią się w zależności od patologii widocznej w oku. Trakcja siatkówki, odwarstwienia siatkówki, retinopatia związana z nowotworem i halucynacje uwalniające są wszystkie patologiczne przyczyny fosfenów i występują w sposób omówiony powyżej. Fosfeny są również doświadczane z zatruciami substancjami lub napromieniowaniem oka .
Dysphotopsias dodatnie i ujemne
Dysphotopsias dodatnie i ujemne są częstym zjawiskiem po ekstrakcji zaćmy z umieszczeniem soczewki wewnątrzgałkowej. Typowym opisem dodatnich dysfotopsji są błyski światła, odblaski lub aureole obecne na peryferiach. Występują one, gdy oczy są otwarte i różnią się w różnych ustawieniach światła, najczęściej pojawiają się, gdy osoba wchodzi z ciemności do oświetlonego pomieszczenia, gdy źrenice są rozszerzone. Są one w przeciwieństwie do fotopsji spowodowanych trakcją szklistki, które są zwykle wywoływane w ciemności i wyzwalane przez ruchy oka. W przeciwieństwie do odwarstwienia siatkówki, dodatnie dysfotopsje nie są trwałe i nie powiększają się. Mechanizm leżący u podstaw dysphotopsji dodatnich jest wynikiem nieprawidłowych odbić światła od krawędzi soczewki wewnątrzgałkowej .
W przeciwieństwie do tego, dysphotopsje ujemne są powszechnie opisywane jako łuki, lub w kształcie półksiężyca, cienie na obwodzie . Podstawowy mechanizm negatywnych dysphotopsias jest ze względu na frakcję światła, które odbija się od oka, powodując mały obszar, w którym światło nie dociera do siatkówki . Ujemne dysphotopsje zwykle ustępują po rozszerzeniu soczewki. Zarówno dodatnie jak i ujemne dysphotopsje występują częściej w przypadku małych IOL o ostrych krawędziach. Wieloogniskowe IOL są również związane ze wzrostem olśnienia i fotopsji w porównaniu do jednoogniskowych IOL. Objawy te są najbardziej powszechne we wczesnym okresie pooperacyjnym, ale zazwyczaj ustępują w miarę włóknienia torebki. Chociaż stosunkowo rzadko, niektórzy pacjenci mogą uznać je za wystarczająco rozpraszające, aby wymagać repozycji lub wtórnego umieszczenia soczewki wewnątrzgałkowej.
- Brown GC, Brown MM, Fischer DH. Photopsias: A Key to Diagnosis. Ophthalmology 2015;122(10):2084-2094. https://PubMed.gov/26249730. DOI: 10.1016/j.ophtha.2015.06.025
- Sharma P, Sridhar J, Mehta S. Flashes and Floaters. Prim Care 2015;42(3):425-435. https://PubMed.gov/26319347. DOI: 10.1016/j.pop.2015.05.011
- Horton JC. Disorders of the Eye. In: Kasper D, Fauci A, Hauser S, Longo D, Jameson JL, Loscalzo J, editors. Harrison’s Principles of Internal Medicine, 19e. New York, NY: McGraw-Hill Education; 2014.
- Hollands H, Johnson D, Brox AC, Almeida D, Simel DL, Sharma S. Acute-onset floaters and flashes: is this patient at risk for retinal detachment? Jama 2009;302(20):2243-2249. https://PubMed.gov/19934426. DOI: 10.1001/jama.2009.1714
- Aminoff MJ, Greenberg DA, Simon RP. Headache & Facial Pain. Clinical Neurology, 9e. New York, NY: McGraw-Hill Education; 2015.
- Vincent MB. Vision and migraine. Headache 2015;55(4):595-599. https://PubMed.gov/25758366. DOI: 10.1111/head.12531
- Marzoli SB, Criscuoli A. The role of visual system in migraine. Neurol Sci 2017;38(Suppl 1):99-102. https://PubMed.gov/28527076. DOI: 10.1007/s10072-017-2890-0
- Pelletier AL, Rojas-Roldan L, Coffin J. Vision Loss in Older Adults. Am Fam Physician 2016;94(3):219-226. https://PubMed.gov/27479624
- Masharani U. Diabetes Mellitus & Hypoglycemia. In: Papadakis MA, McPhee SJ, Rabow MW, editors. Current Medical Diagnosis & Treatment 2018. New York, NY: McGraw-Hill Education; 2018.
- Zhao Q, Zhou F, Zhang Y, Zhou X, Ying C. Fasting Plasma Glucose Variability Levels and Risk of Adverse Outcomes Among Patients with Type 2 Diabetes: A Systematic Review and Meta-analysis. Diabetes Res Clin Pract 2018;10.1016/j.diabres.2018.12.010. https://PubMed.gov/30583033. DOI: 10.1016/j.diabres.2018.12.010
- Klein R, Klein BE, Moss SE, Davis MD, DeMets DL. The Wisconsin epidemiologic study of diabetic retinopathy. II. Prevalence and risk of diabetic retinopathy when age at diagnosis is less than 30 years. Arch Ophthalmol 1984;102(4):520-526. https://PubMed.gov/6367724
- Klein R, Klein BE, Moss SE, Davis MD, DeMets DL. The Wisconsin epidemiologic study of diabetic retinopathy. III. Prevalence and risk of diabetic retinopathy when age at diagnosis is 30 or more years. Arch Ophthalmol 1984;102(4):527-532. https://PubMed.gov/6367725
- Podstawy okulistyki: niezbędne dla studentów medycyny. 10th ed: American Academy of Ophthalmology, 2016.
- Lima Neto AC, Bittar R, Gattas GS, Bor-Seng-Shu E, Oliveira ML, Monsanto RDC, Bittar LF. Pathophysiology and Diagnosis of Vertebrobasilar Insufficiency: A Review of the Literature. Int Arch Otorhinolaryngol 2017;21(3):302-307. https://PubMed.gov/28680502. DOI: 10.1055/s-0036-1593448
- Pang L. Hallucinations Experienced by Visually Impaired: Charles Bonnet Syndrome. Optom Vis Sci 2016;93(12):1466-1478. https://PubMed.gov/27529611. DOI: 10.1097/opx.00000000000959
- Vahdani K, Poon JS, Antoniou E, Giasin O, Makrygiannis G. Charles Bonnet Syndrome Following Eyelid Reconstruction Surgery. Ophthalmic Plast Reconstr Surg 2017;33(3):229-230. https://PubMed.gov/28475529. DOI: 10.1097/iop.00000000000892
- Beaulieu RA, Tamboli DA, Armstrong BK, Hogan RN, Mancini R. Reversible Charles Bonnet Syndrome After Oculoplastic Procedures. J Neuroophthalmol 2018;38(3):334-336. https://PubMed.gov/27984353. DOI: 10.1097/wno.00000000000477
- Moyer K, DeWilde A, Law C. Cystoid macular edema from cancer-associated retinopathy. Optom Vis Sci 2014;91(4 Suppl 1):S66-70. https://PubMed.gov/24531653. DOI: 10.1097/opx.000000000184
- Grange L, Dalal M, Nussenblatt RB, Sen HN. Autoimmune retinopathy. Am J Ophthalmol 2014;157(2):266-272.e261. https://PubMed.gov/24315290. DOI: 10.1016/j.ajo.2013.09.019
- Grewal DS, Fishman GA, Jampol LM. Retinopatia autoimmunologiczna i przeciwciała antyretinalne: przegląd. Retina 2014;34(5):827-845. https://PubMed.gov/24646664. DOI: 10.1097/iae.000000000119
- Adamczyk G. Autoantibody targets and their cancer relationship in the pathogenicity of paraneoplastic retinopathy. Autoimmun Rev 2009;8(5):410-414. https://PubMed.gov/19168157. DOI: 10.1016/j.autrev.2009.01.002
- Chang DF. Chapter 2. Ophthalmologic Examination. In: Riordan-Eva P, Cunningham ET, editors. Vaughan & Asbury’s General Ophthalmology, 18e. New York, NY: The McGraw-Hill Companies; 2011.
- Coppola D, Purves D. The extraordinarily rapid disappearance of entoptic images. Proc Natl Acad Sci U S A 1996;93(15):8001-8004. https://PubMed.gov/8755592
- Mark HH. Entoptyczne spojrzenie na naczynia siatkówki. Acta Ophthalmol 2014;92(3):e237-240. https://PubMed.gov/23890291. DOI: 10.1111/aos.12192
- Ropper AH, Samuels MA, Klein JP. Chapter 13. Disturbances of Vision. Adams and Victor’s Principles of Neurology, 10e. New York, NY: The McGraw-Hill Companies; 2014.
- Salari V, Scholkmann F, Vimal RLP, Csaszar N, Aslani M, Bokkon I. Phosphenes, retinal discrete dark noise, negative afterimages and retinogeniculate projections: Nowe ramy wyjaśniające oparte na endogennej luminescencji ocznej. Prog Retin Eye Res 2017;60:101-119. https://PubMed.gov/28729002. DOI: 10.1016/j.preteyeres.2017.07.001
- Mathis T, Vignot S, Leal C, Caujolle JP, Maschi C, Mauget-Faysse M, Kodjikian L, Baillif S, Herault J, Thariat J. Mechanisms of phosphenes in irradiated patients. Oncotarget 2017;8(38):64579-64590. https://PubMed.gov/28969095. DOI: 10.18632/oncotarget.18719
- Bournas P, Drazinos S, Kanellas D, Arvanitis M, Vaikoussis E. Dysphotopsia after cataract surgery: comparison of four different intraocular lenses. Ophthalmologica 2007;221(6):378-383. https://PubMed.gov/17947823. DOI: 10.1159/000107496
- Davison JA. Positive and negative dysphotopsia in patients with acrylic intraocular lenses. J Cataract Refract Surg 2000;26(9):1346-1355. https://PubMed.gov/11020620
- Hu J, Sella R, Afshari NA. Dysphotopsia: a multifaceted optic phenomenon. Curr Opin Ophthalmol 2018;29(1):61-68. https://PubMed.gov/29084005. DOI: 10.1097/icu.00000000000447
- Wang SY, Stem MS, Oren G, Shtein R, Lichter PR. Patient-centered and visual quality outcomes of premium cataract surgery: a systematic review. Eur J Ophthalmol 2017;27(4):387-401. https://PubMed.gov/28574135. DOI: 10.5301/ejo.5000978
Suggested Citation Format
Morrow N, Chung AT, Wall M. Photopsias. EyeRounds.org. June 24, 2019; Available from https://EyeRounds.org/tutorials/photopsias/index.htm